
碱基编辑技术最早由哈佛大学David R. Liu团队开发,胞嘧啶碱基编辑器(CBE)与腺嘌呤碱基编辑器(ABE)虽已在多个物种中得到广泛应用,但目前研究表明它们仍存在严重的随机脱靶现象,未得到完全解决。
10月14日,邦耀生物宣布,与华东师范大学李大力教授及刘明耀教授团队合作开发并命名了一种精准且安全的新型腺嘌呤碱基编辑器——“ABE9”,能够有效解决ABE临床应用存在的各类脱靶隐患和安全性问题,理论上将为近50%遗传致病性SNVs的纠正提供了新的精准靶向工具。该项研究成果于10月13日在Nature Chemical Biology上发表。

这一发现对提升ABE工具的安全性,拓宽其适用范围,推动其在基因治疗中的应用及后续的临床转化均具有重要意义。ABE9作为新一代最具有临床适用性的产品,已提前完成核心专利申请,未来专利布局将覆盖全球主流市场。
该研究首先证明了高活性的ABE8e引发了更严重的旁观者效应以及Cas9非依赖的DNA和RNA脱靶,而且对于胞嘧啶的编辑效率显著提高。为了解决ABE8e的精准性问题,该研究基于ABE8e的冷冻电镜结构进行理性设计和筛选,发现在TadA-8e脱氨酶的活性口袋引入关键突变L145T和N108Q(ABE9)可在保留高编辑活性的同时,显著缩小编辑窗口到sgRNA的第5-6位的腺嘌呤,消除对胞嘧啶的编辑活性(图1)。
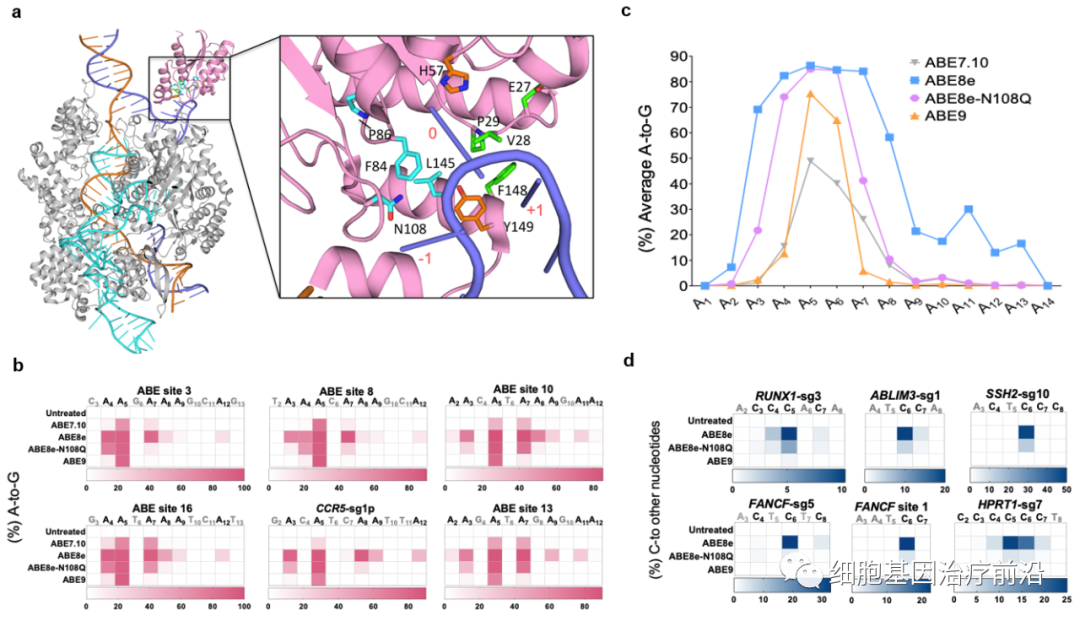
图1:TadA-8e蛋白结构及ABE9编辑特性评价
通过鉴定Cas9非依赖性脱靶的R-Loop检测以及RNA脱靶的转录组深度测序,发现ABE9几乎不引起随机的DNA和RNA脱靶编辑(图2),展示出了极高的应用安全性。此外,ABE9在小鼠和大鼠胚胎中展示了极高的体内编辑精度和活性。在所有的F0代小鼠中,对照组ABE8e在编辑A5目标位点的同时引起了大量的A8位的旁观者编辑(18/19只),精确编辑A5位的小鼠仅占5.1%。而ABE9可以精准编辑A5(14/16只),其中25%小鼠的编辑效率超过80%, 所有F0小鼠的平均效率达到54.3%。同样,ABE9在大鼠中能够靶向Gaa基因精准产生D645G突变而诱发庞贝氏病,F0代大鼠中仅含目的位点A6-to-G突变的达到48.41%,而ABE7.10的精准编辑只占2.76%。啮齿类动物的体内实验再次证明了ABE9高精度特性,也凸显了其在精准构建动物模型的潜力(图3)。
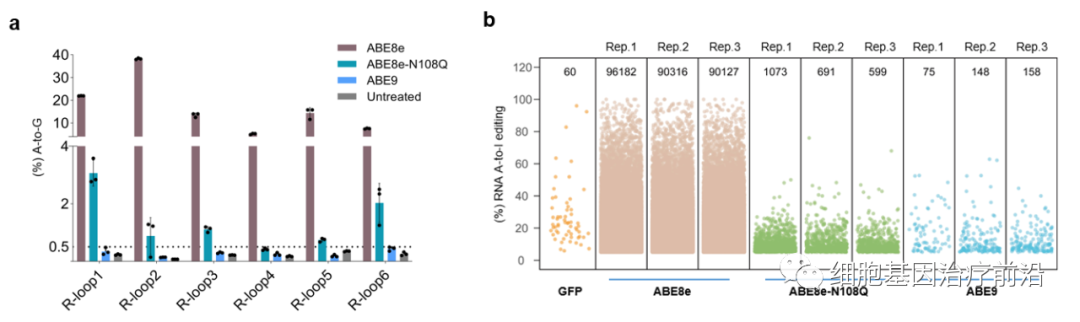
图2:Cas9非依赖DNA 脱靶和RNA脱靶评价
另外,为进一步评估ABE基因治疗的潜能,研究者构建含有人类致病性SNVs的细胞系,且需纠正的腺苷处于sgRNA第五位且处于多个连续腺苷中。结果表明,即使面对这样极端富含旁观者碱基的序列中,ABE9也能精准编辑sgRNA第五位产生A-to-G的转换,精确纠正能力相较于ABE8e最大提高了342.5倍(图3)。
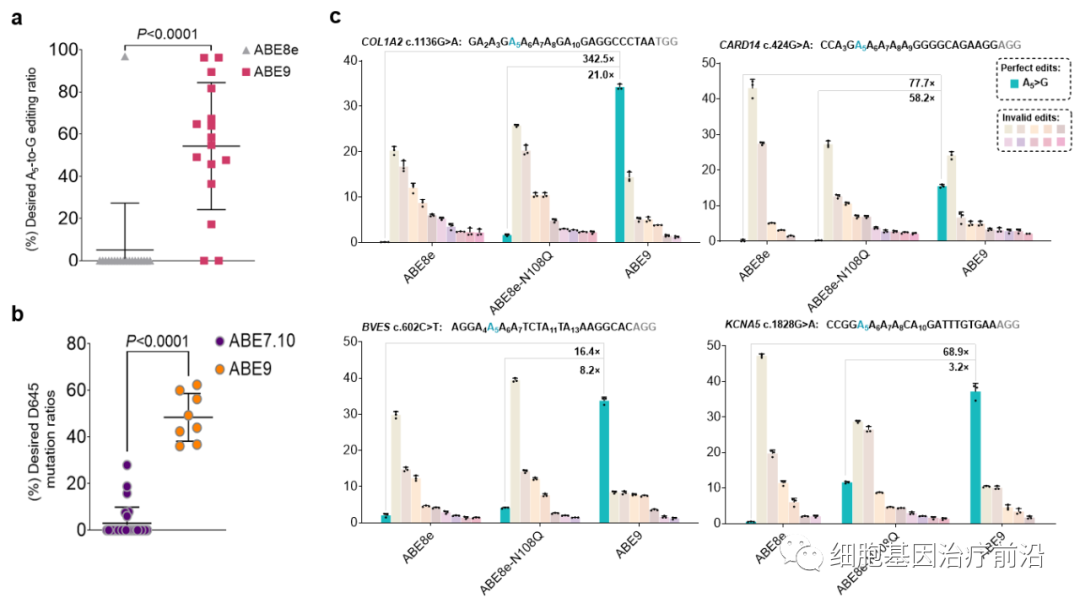
图3:ABE9动物体内编辑及纠正人类致病性的SNVs
论文共同通讯作者,邦耀生物联合创始人&副总裁李大力教授表示:“在本次研究中,为了无差别的分析海量靶点中ABE9的精准编辑特性,采用8000多条sgRNA与靶点配对的文库进行编辑窗口的分析,发现ABE9非常精准且无序列偏好地主要编辑A5-A6两位碱基,证明其广泛地精准编辑特性。总的来说,ABE9将编辑窗口缩窄至1-2nt,几乎完全消除了对胞嘧啶的脱靶编辑,更重要的是将DNA /RNA脱靶事件降低到背景水平,实现了高精度、低脱靶的碱基编辑,将来还可以与识别不同PAM的Cas变体融合,进一步扩大靶向范围,不仅为基础研究带来新的碱基编辑工具,更为重要的是有望极大提高将来临床应用的安全性。”
邦耀生物产品管线:《邦耀生物管线梳理!100多项专利成果收入囊中,多个新药项目进入申报》
参考资料:
https://www.brlmed.com/
<END>






















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论