
据药融云中国药品审评数据库统计,9月15日,CDE承办化药新药临床申请已受理号计共5个,涉及三个品种,分别是亚盛药业的APG-115胶囊(化药1类)、智康弘义的SC0062胶囊(化药1类)、以及瑞克卫的瑞加诺生注射液(化药2.4类)。
9月15日CDE受理品种目录(微信搜索"药融云小程序"进行相关更多数据查询)
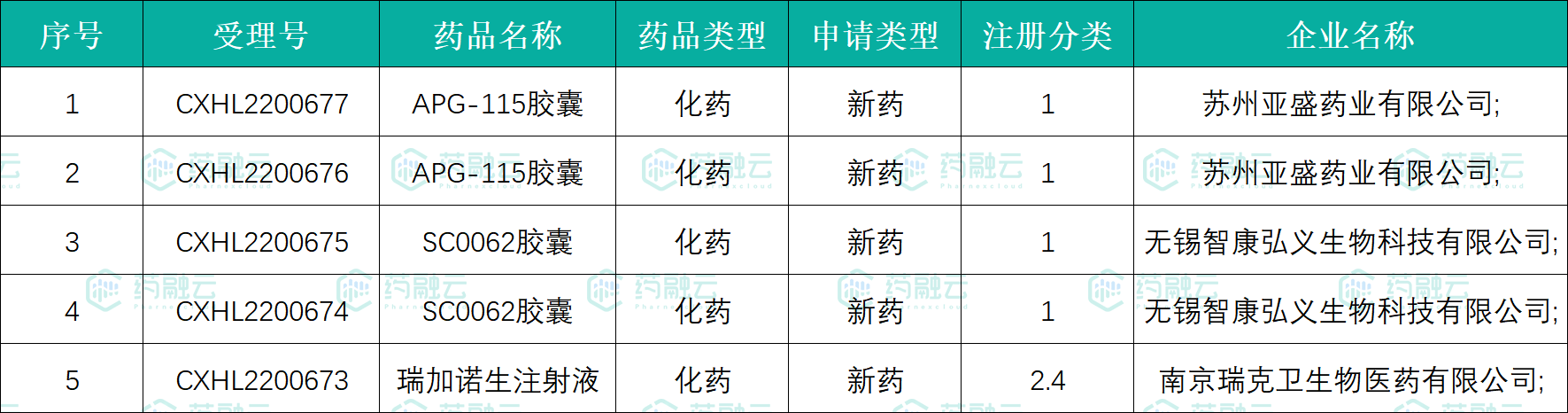
数据来源:药融云中国药品审评数据库
1.APG-115胶囊
APG-115是亚盛医药(6855.HK)自主研发的一种口服、高选择性的MDM2-p53抑制剂,对MDM2具有高度结合亲和力,通过阻断MDM2-p53相互作用从而恢复p53肿瘤抑制活性。
目前,APG-115已经在体外和体内神经母细胞瘤模型中证明了单药治疗的抗肿瘤活性,该作用机制的明确为该药物治疗神经母细胞瘤的临床探索提供了良好的基础。其研发成功,将会填补国内在MDM2-p53靶点领域内的药物空白。
p53基因是最广泛研究的肿瘤抑制基因,p53基因的失活对肿瘤形成起重要作用,而MDM2是p53的一个最重要的抑制因子,当两者结合的时候,会使p53蛋白降解,活性降低,抑癌作用减弱。以MDM2-p53为靶点设计开发全新机制的抗肿瘤药物,也是当下全球肿瘤药物研发领域热点之一。
APG-115适应症及治疗领域
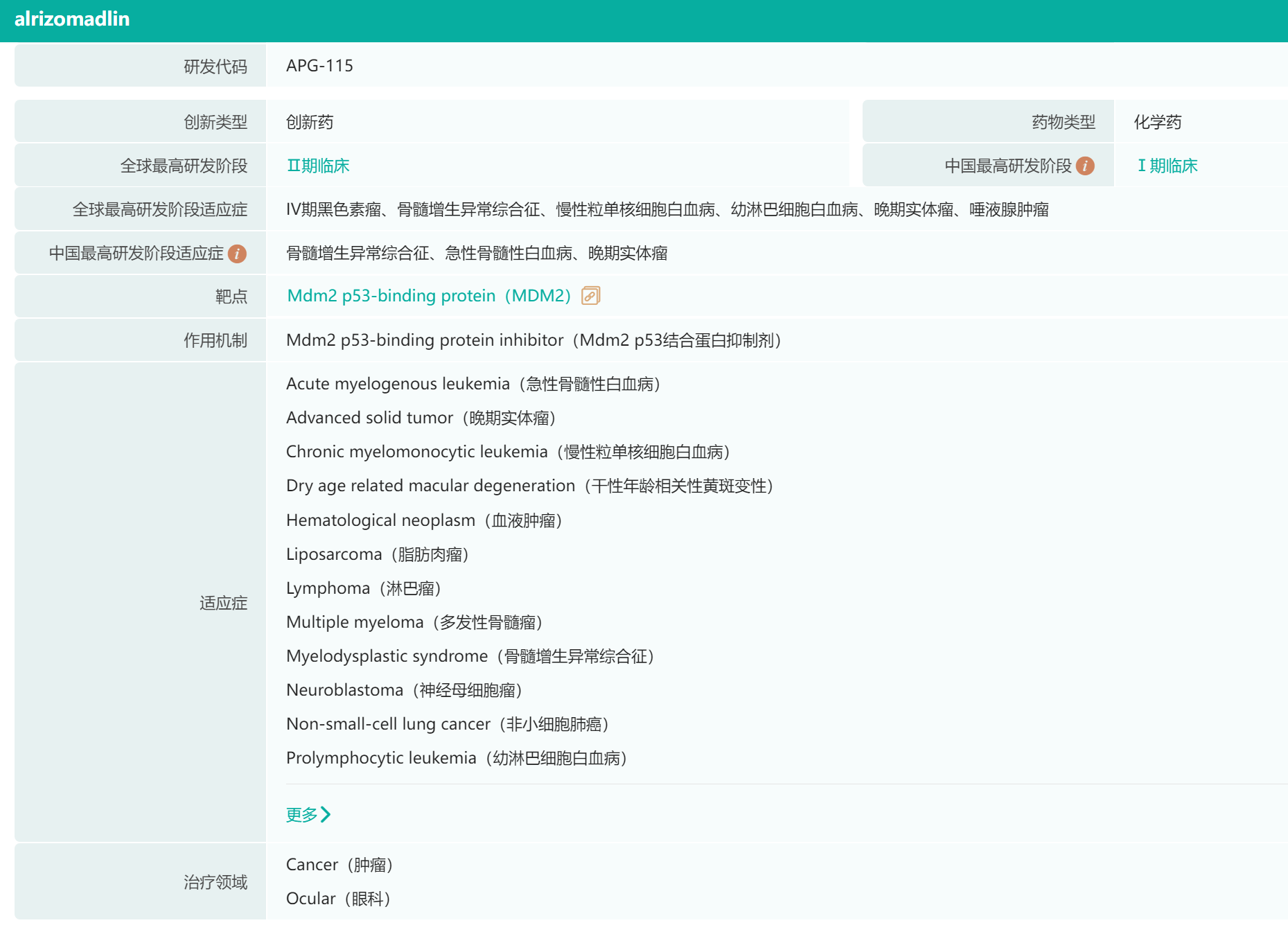
图片来源:药融云全球药物研发数据库
2021年7月,FDA 授予MDM2抑制剂Alrizomadlin (APG-115)孤儿药资格,用于治疗IIB-IV期黑色素瘤患者。这是APG-115继胃癌、急性髓系白血病、软组织肉瘤、视网膜母细胞瘤后,获得的第5项FDA授予的孤儿药资格认定。
2022年3月,APG-115又获得FDA授予的儿童罕见病资格认证(Rare Pediatric Disease,RPD),为儿童神经母细胞瘤患者提供更多治疗选择。至此,APG-115已获得FDA授予的六项孤儿药资格认证(ODD)、两项RPD。
APG-115不同适应症研发状态(部分)
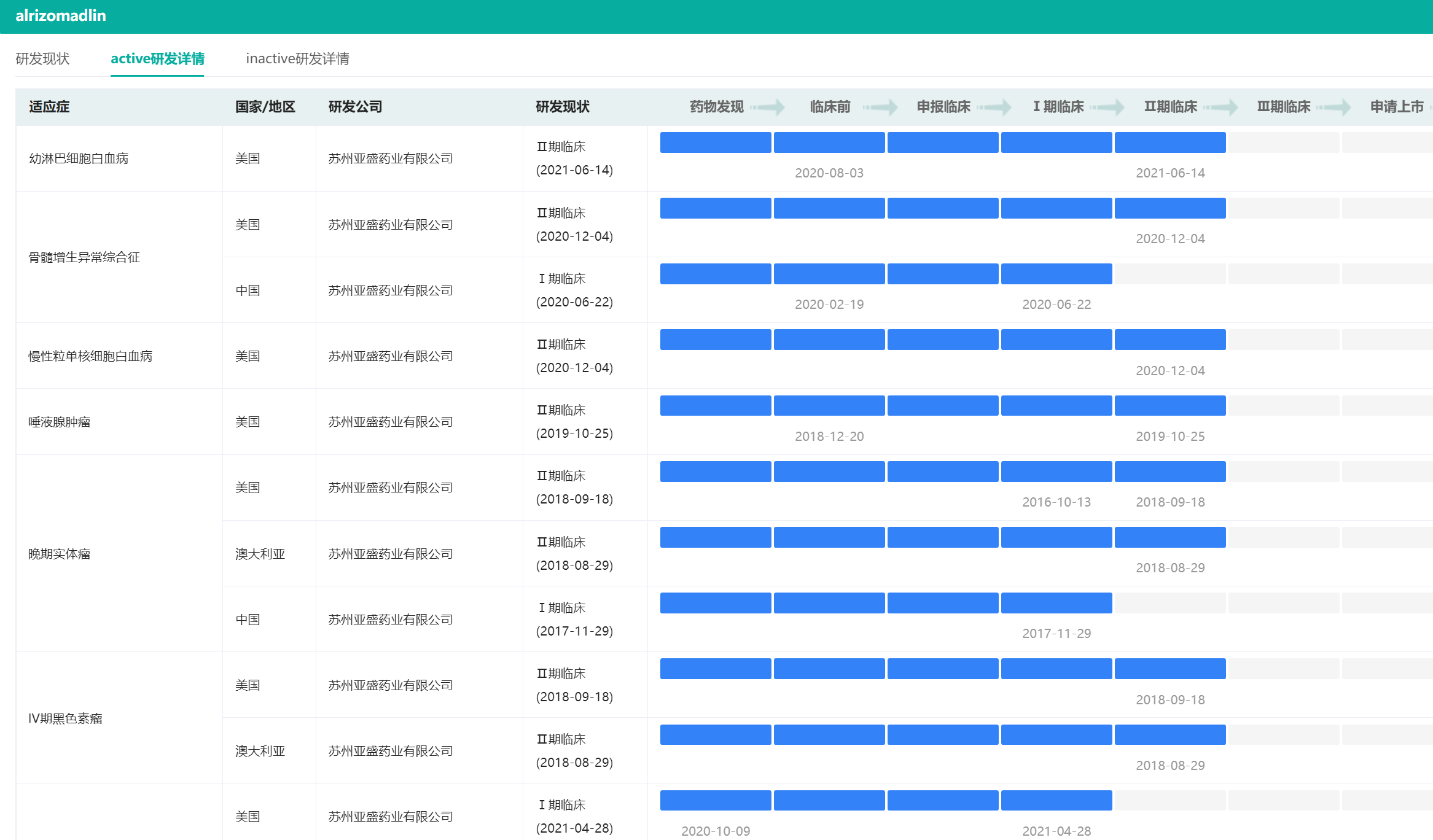
图片来源:药融云全球药物研发数据库
神经母细胞瘤是一种起源于外周交感神经系统的胚胎肿瘤,是儿童最常见的颅外实体恶性肿瘤,占儿童癌症死亡总数的15%。神经母细胞瘤是一种发育紊乱的疾病,大多在婴儿期诊断,41%的患者在出生前3个月确诊,大多数患者在5岁时确诊,中位年龄约为18个月。
亚盛医药致力于在肿瘤、乙肝及与衰老相关的疾病等治疗领域开发创新药物,拥有8个已进入临床开发阶段的1类小分子新药产品管线,包括抑制Bcl-2、IAP 或 MDM2-p53 等细胞凋亡路径关键蛋白的抑制剂;新一代针对癌症治疗中出现的激酶突变体的抑制剂等。目前,有4个在研新药获得15项FDA和1项欧盟孤儿药资格认定,2项FDA快速通道资格以及2项FDA儿童罕见病资格认证。
2.SC0062胶囊
智康弘义的SC0062胶囊是一款选择性内皮素受体ETA拮抗剂,拟用于治疗肺动脉高压;也是国内首个申报获批临床的该靶点药物,于2020年成功开展“评估SC0062胶囊在健康成人受试者中单次和连续给药的安全性、耐受性、药代动力学特征及食物影响的I期临床研究”(CTR20201868)。
SC0062胶囊I期临床研究数据(部分)
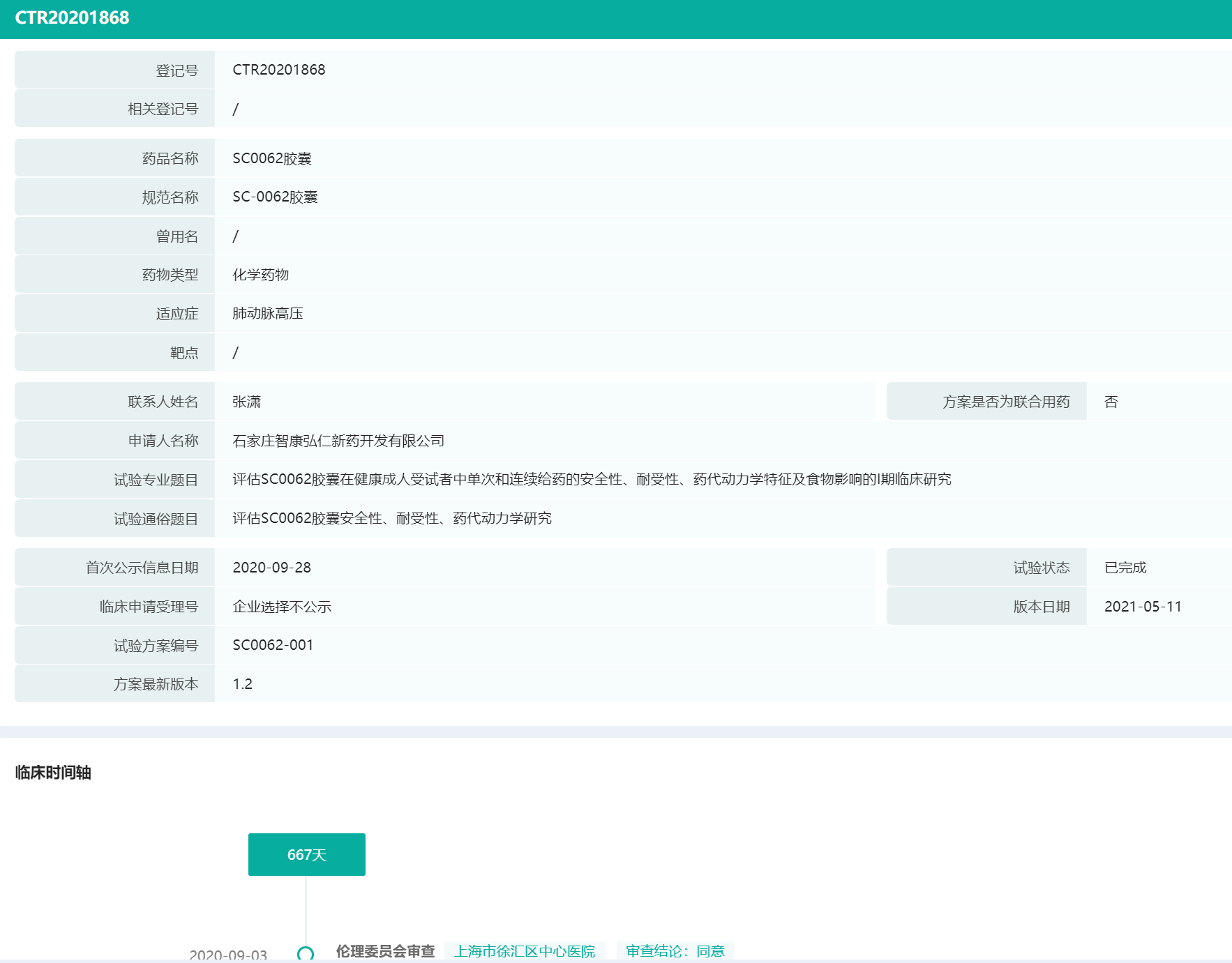
图片来源:药融云中国临床试验数据库
2022年7月,智康弘义研发的1类新药SC0245片也通过国家药品监督管理局临床默示许可,即将开展临床研究。SC0245片是一款ATR抑制剂,利用“合成致死”机制抗肿瘤,获批适应为联合拓扑异构酶Ⅰ抑制剂(伊立替康或拓扑替康)治疗小细胞肺癌。
ATR是ATM突变的合成致死靶点,被认为是继PARP后最有希望的合成致死靶点之一,目前全球已有多款ATR抑制剂处于临床阶段。SC0245片也是国内首个获批临床的ATR抑制剂,目前正在开展一项开放、单臂的Ia/Ib期研究,评价其在晚期恶性实体瘤患者的剂量探索Ia期研究,及在ATM 缺陷的胃癌患者和TP53突变的食管癌患者的Ib期临床研究。
SC0245片临床试验(ChiCTR2100045406)基本信息

图片来源:药融云中国临床试验数据库
3.瑞加诺生注射液
瑞加诺生注射液原为海融医药的立项开发品种,后续转让给参股公司瑞克卫生物。国产瑞加诺生注射液(国药准字H20213800)为国内独家首仿品种,参考适应症为冠状动脉疾病。于2021年10月获中国国家药品监督管理局(NMPA)批准上市,填补了国内心肌灌注显像诊断用药的空白,有助于提高患者用药的可及性。
瑞加诺生注射液(商品名LEXISCAN)其原研为ASTELLAS PHARMA US INC,作为放射性核素心肌灌注显像(MPI)中使用的一种负荷药物,适用于不能接受运动负荷试验而需进行药物负荷试验的患者。于2008年在美国上市,2020年美国市场销售额约为6亿美元。
国产瑞加诺生注射液药品批文基本信息(部分)
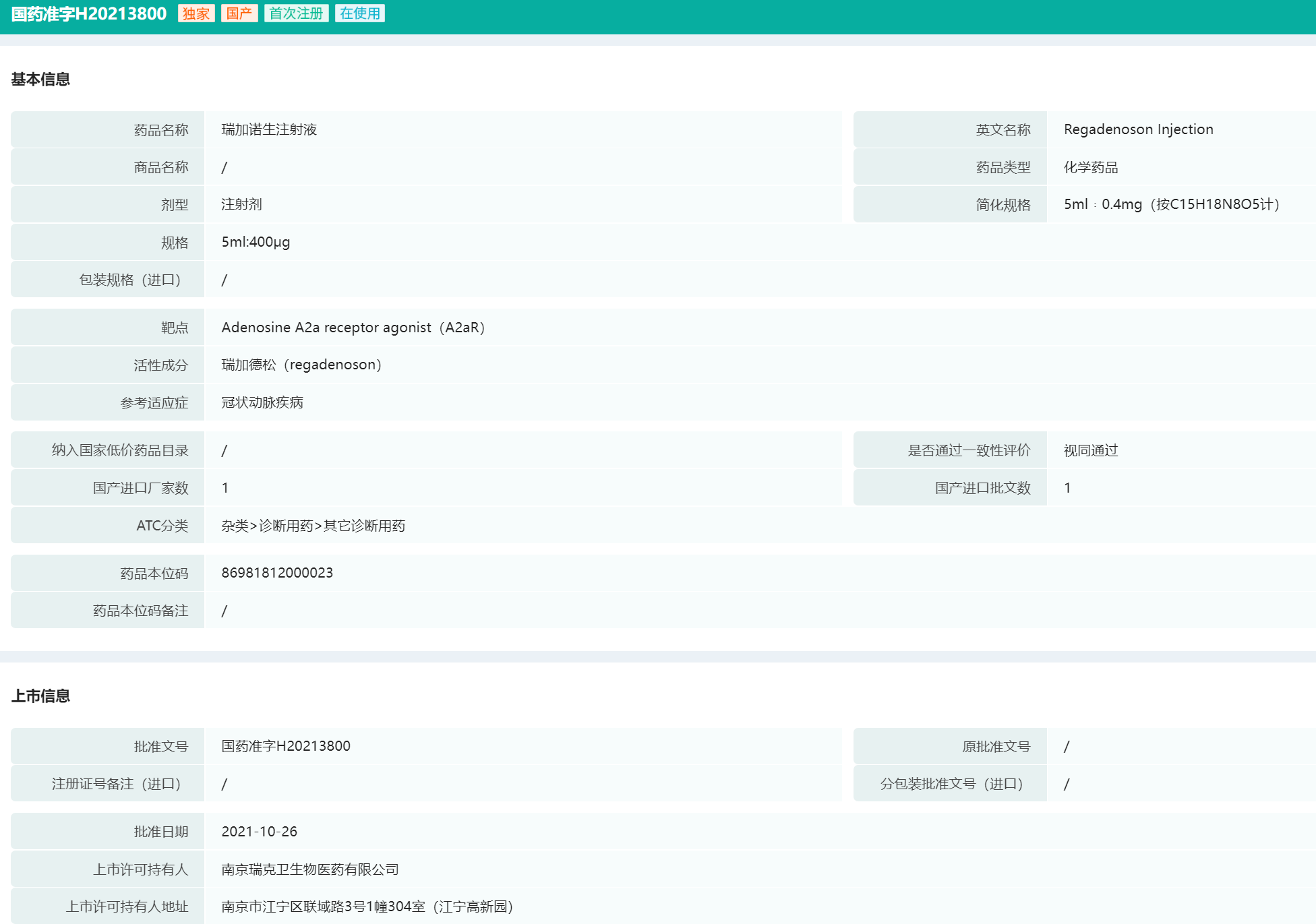
图片来源:药融云中国药品批文数据库
据药融云中国药品审评数据库显示,目前国内仅瑞克卫生物1家公司的国产瑞加诺生注射液获批上市。此外,南京健友生化制药、西安力邦制药两家企业的上市申请处于在审评审批中;四川国瑞药业、国药集团国瑞药业的临床申请已发件;通用电气药业的临床申请处于在审评审批中。
想要解锁更多药企创新药信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药企创新药产品布局、基本信息、研发阶段、最新进展、申报获批情况、临床试验信息、销售情况与市场前景,可否投入研发!注册立享15天免费试用和虎年首份医药数据大礼包!

<END>







































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论