8月上旬药品审评审批
进展要点
2021.08.01-2021.08.12期间药审中心受理总量为443个,涉及品种297个,涉及康方、正大天晴、恒瑞等企业
40个1类新药申请临床获CDE受理
新增27个按仿制药质量和疗效一致性评价品种申报的受理号
20个品种通过(含视同通过)一致性评价,3款首家过评
4款国产新药获批上市:中山康方生物新型PD-1单抗「派安普利单抗」获批
2021年8月1日至8月12日期间,共有4款国产新药、4款进口药获批上市;另有20个品种通过(含视同通过)一致性评价。
有北京双鹭药业「奥硝唑注射液」、浙江京新药业「匹伐他汀钙分散片」和远大医药「重酒石酸去甲肾上腺素注射液」这3款首仿获批上市,正大天晴/康方生物新型PD-1单抗派安普利单抗国内获批上市,具体信息如下:
一、4款国产新药获批上市

派安普利单抗
派安普利单抗是康方生物自主开发的具有创新性、潜在同类最佳的人源化抗PD-1单克隆抗体,目前由合资公司——正大天晴康方(由康方生物与正大天晴共同成立)进行共同开发和商业化。
此次派安普利单抗(AK105)获批上市,用于治疗至少经过二线系统化疗复发或难治性经典型霍奇金淋巴瘤(r/r cHL)患者,是第5款国产PD-1单抗。此外,派安普利单抗的三线鼻咽癌、一线鳞状非小细胞肺癌适应症均已报产,并有一线肝癌、一线非鳞非小细胞肺癌多项适应症处于Ⅲ期临床阶段。
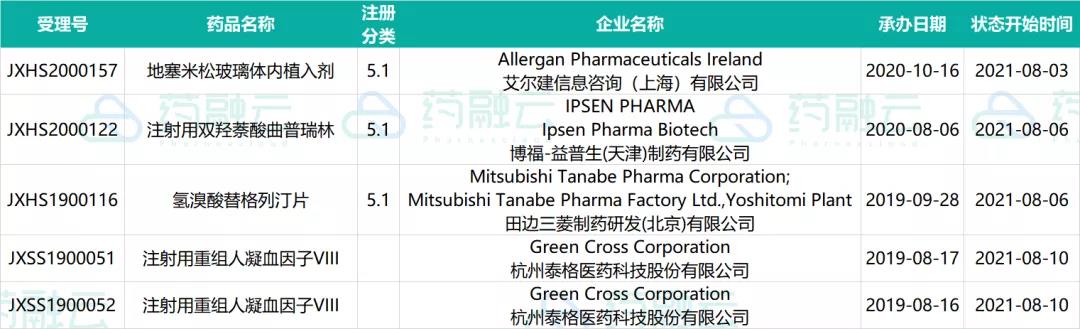
二、4个品种批准进口
三、过评品种信息
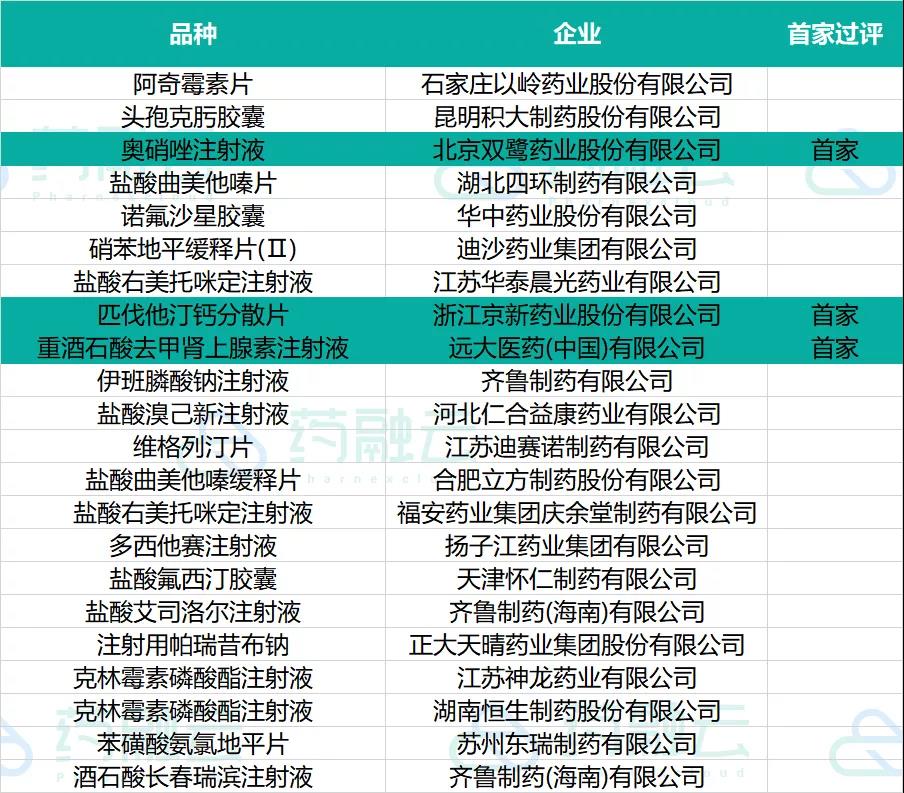
在审评审批阶段
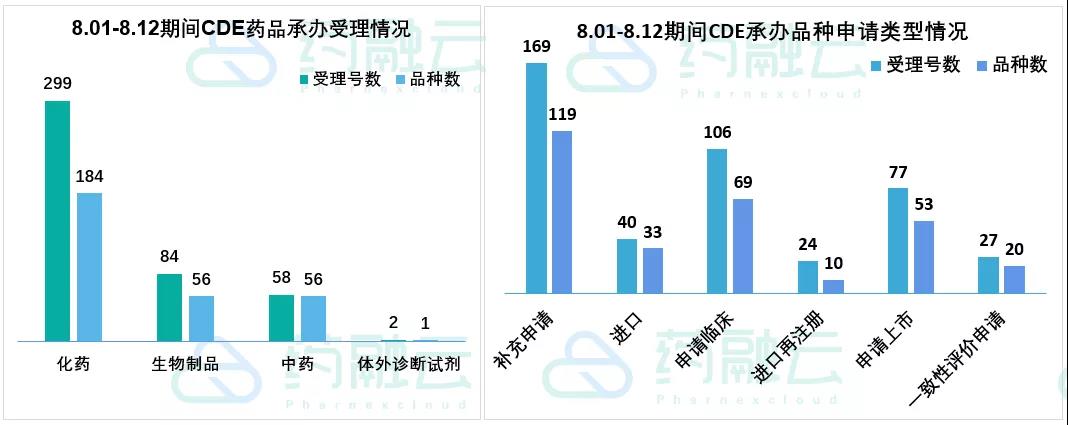
根据药融云中国药品审评数据,8月1号-8月12号期间共297个(按品种计,下同)药品获CDE承办,包括化药184个,生物制品56个,中药56个,,体外诊断试剂1个。
近期CDE承办的共有69个品种申报临床,其中包括55款国产新药,另有20个品种提交一致性评价。
近期受理国产新药共计95个受理号,有60个品种,其中6款药品提交上市申请,其余为申请临床。
申请上市的新药情况
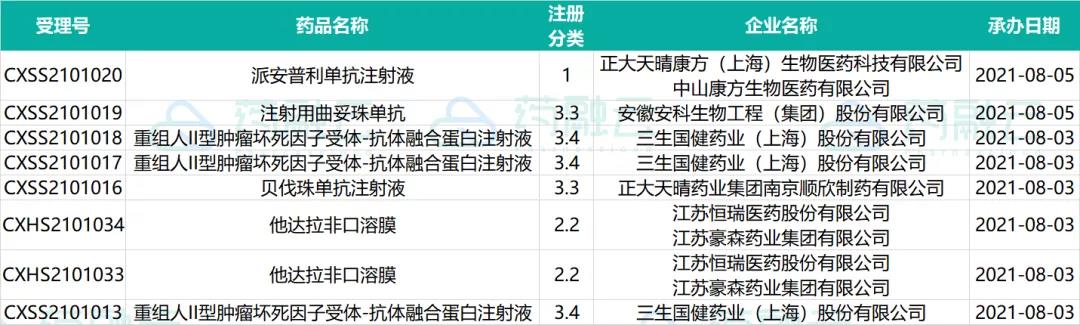
申请临床的1类新药情况
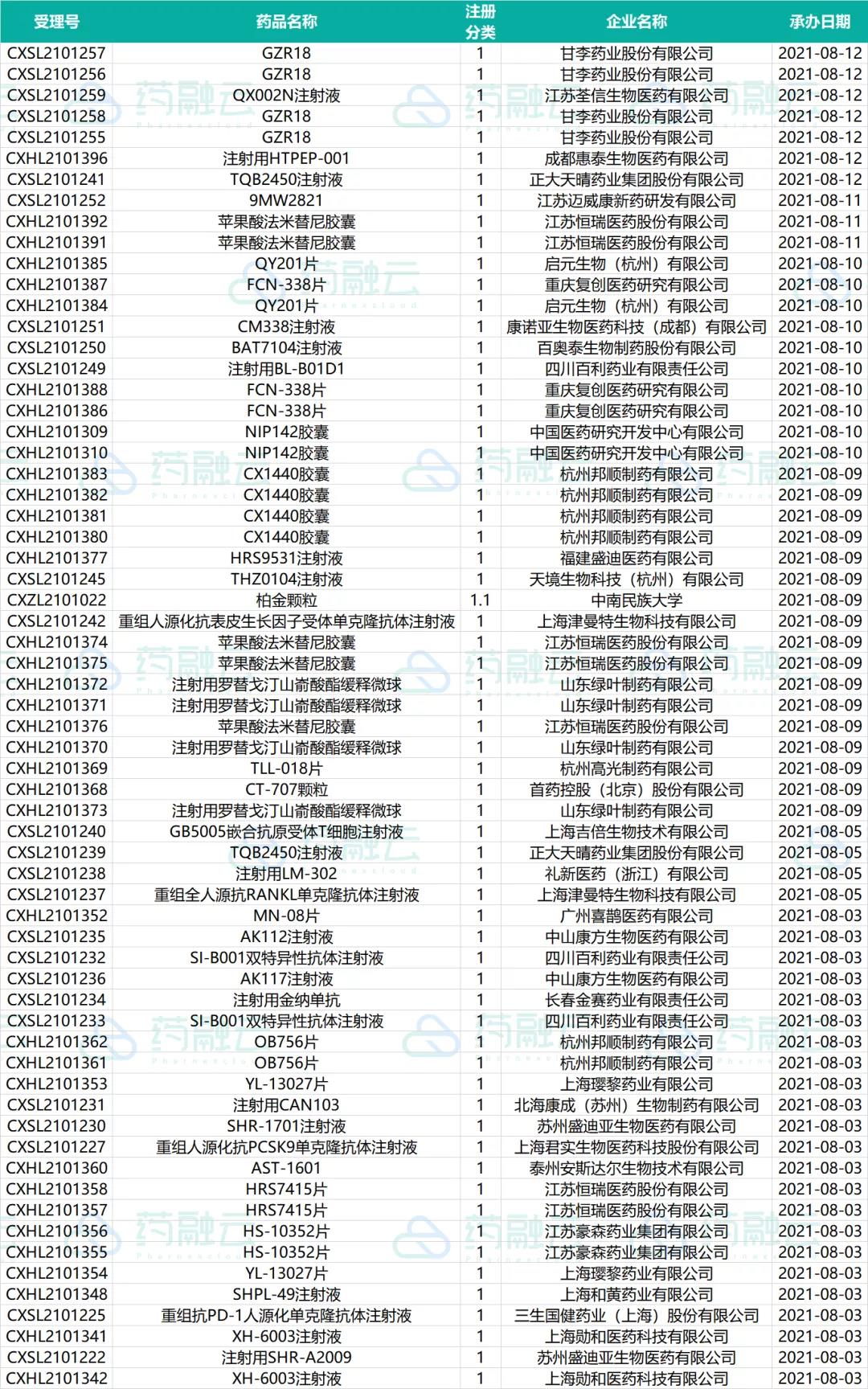
在审批阶段
近期共有53个品种(63个受理号)进入审批阶段,详见下表。

一致性评价申请
近期有20个品种提交一致性评价申请。








































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论