- 2021.03.12-2021.03.18期间药审中心受理总量为151个,涉及品种109个。
- 14个1类新药申请临床获CDE受理。
- 新增9个按仿制药质量和疗效一致性评价品种申报的受理号。
- 37个品种通过(含视同通过)一致性评价。
- 1款1类新药获批上市:国内首款埃博霉素类新药获批
近日,成都华昊中天药业的优替德隆注射液获批,这标志着中国首个埃坡霉素1类抗肿瘤新药正式获批。此次优替德隆的获批打破了我国长期以来晚期乳腺癌治疗的瓶颈,结束了国内近三十年来除紫杉醇外无突破性化疗药物的局面。详细信息如下:

2021日3月15日,成都华昊中天药业申报的1类创新药优替德隆注射液(商品名:优替帝)获批上市。优替德隆为埃坡霉素类衍生物,可促进微管蛋白聚合并稳定微管结构,诱导细胞凋亡。该药为我国自主研发并拥有自主知识产权的创新药,也是国内获批的第一款埃博霉素类新药。
优替德隆注射液联合卡培他滨,用于既往接受过至少一种化疗方案的复发或转移性乳腺癌患者。该品种上市为晚期乳腺癌患者提供了新的治疗选择。
资料显示,优替德隆是唯一两度(2016和2018年)入选国际最具影响力的临床肿瘤学年会ASCO做口头报告的中国乳腺癌创新药。该药品于2003年开始研发,2006年取得临床批件,2018年3月,CDE受理优替德隆1类新药的上市申请,2018年6月,将其纳入优先审评品种名单。
据药融云中国临床试验数据显示,优替德隆用于晚期非小细胞肺癌(NSCLC)以及结直肠癌(CRC)的II期临床试验目前正在进行中。

 在审评审批阶段
在审评审批阶段 根据药融云中国药品审评数据,3月12号-3月18号期间共109个(按品种计,下同)药品获CDE承办,包括化药78个,生物制品20个,以及中药11个。
近期CDE承办的共有22个品种申报临床,其中包括18款新药,另有8个品种提交一致性评价。

近期受理国产新药共计24个受理号,涉及18个品种17家企业,均为申请临床。包括14款1类新药申请。
下表为2021.03.12-2021.03.18申请临床的新药药物情况。

下表为2021.03.12-2021.03.18申请临床的进口药物情况。

下表为2021.03.12-2021.03.18申请进口的进口药药物情况。

在审批阶段
近期共有9个品种(13个受理号)进入审批阶段。
2021.03.12-03.18在审批阶段药物情况

数据来源:药融云中国药品审评数据库
制证完毕-待发批件
近期共计30个品种(涉及受理号41个)制证完毕-待发批件,有7个品种通过一致性评价,10个品种视同通过一致性评价。下表是制证完毕-待发批件的药物情况。
2021.03.12-03.18制证完毕-待发批件药物情况

已发件药物情况
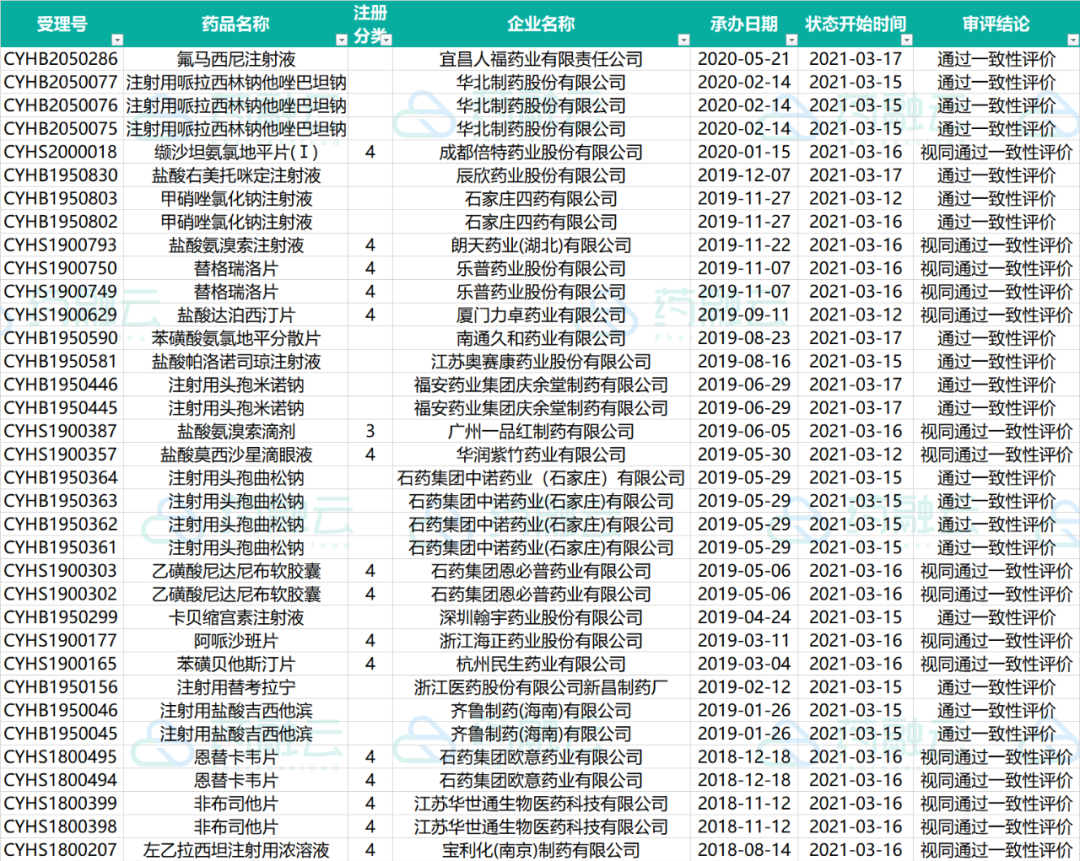
近期共计66个品种(涉及受理号113个)已发件,其中有11个品种通过一致性评价,12个品种视同通过一致性评价。下表是已发件过评药物情况。
2021.03.12-03.18已发件过评药物情况
一致性评价申请
近期有8个品种提交一致性评价申请。
2021.03.12-03.18药审中心一致性评价承办情况









































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论