
9月25日,君实生物(1877.HK,688180.SH)宣布,由公司自主研发的抗PD-1单抗药物特瑞普利单抗对比达卡巴嗪一线治疗不可切除或转移性黑色素瘤的随机、对照、多中心III期临床研究(MELATORCH研究)的主要研究终点无进展生存期(PFS,基于独立影像评估)达到方案预设的优效边界。君实生物计划将于近期向监管部门递交该新适应症的上市申请。
黑色素瘤是恶性程度最高的皮肤癌类型,2020年全球新发病例约32.5万,死亡病例约5.7万1。黑色素瘤在我国相对少见,但病死率高(2017年新发病例约1.6万,而死亡病例达到0.5万),发病率也在逐年增加2,3。此外,欧美白种人黑色素瘤患者的疾病亚型以皮肤型为主(约占90%),而我国患者以肢端型和黏膜型为主(约占70~80%),因此两者在发病机制、肿瘤生物学行为、治疗方法和预后等方面差异较大3。
近年来,免疫检查点抑制剂在黑色素瘤治疗上已取得巨大成功,并在欧美获批用于黑色素瘤的晚期一线和晚期二线及以上治疗以及辅助治疗。然而,截至目前国内仅有抗PD-1单抗获批用于晚期黑色素瘤二线及以上治疗,而晚期一线治疗仍以传统化疗或靶向治疗(仅适用于携带BRAF V600突变患者)为主4。因此,国内晚期黑色素瘤患者对于一线免疫治疗的临床需求迫切。
作为国内首个达成阳性结果的PD-(L)1抑制剂一线治疗晚期黑色素瘤的关键注册临床研究,MELATORCH研究(NCT03430297)旨在比较特瑞普利单抗对比达卡巴嗪在既往未接受系统抗肿瘤治疗的不可切除或转移性黑色素瘤患者中的有效性和安全性。研究结果表明,相较于达卡巴嗪,特瑞普利单抗一线治疗不可切除或转移性黑色素瘤可显著延长患者的PFS。特瑞普利单抗安全性数据与既往研究相似,未发现新的安全性信号。本研究的详细数据将在后续的国际学术大会上公布。
关于特瑞普利单抗注射液(拓益®)
特瑞普利单抗注射液(拓益®)是我国批准上市的首个国产以PD-1为靶点的单抗药物,已在全球(包括中国、美国、东南亚及欧洲等地)开展了覆盖超过15个适应症的40多项由公司发起的临床研究。正在进行或已完成的关键注册临床研究在多个瘤种范围内评估特瑞普利单抗的安全性及疗效,包括肺癌、鼻咽癌、食管癌、胃癌、膀胱癌、乳腺癌、肝癌、肾癌及皮肤癌等。截至目前,特瑞普利单抗已在中国获批6项适应症。
特瑞普利单抗注射液过评药企查询
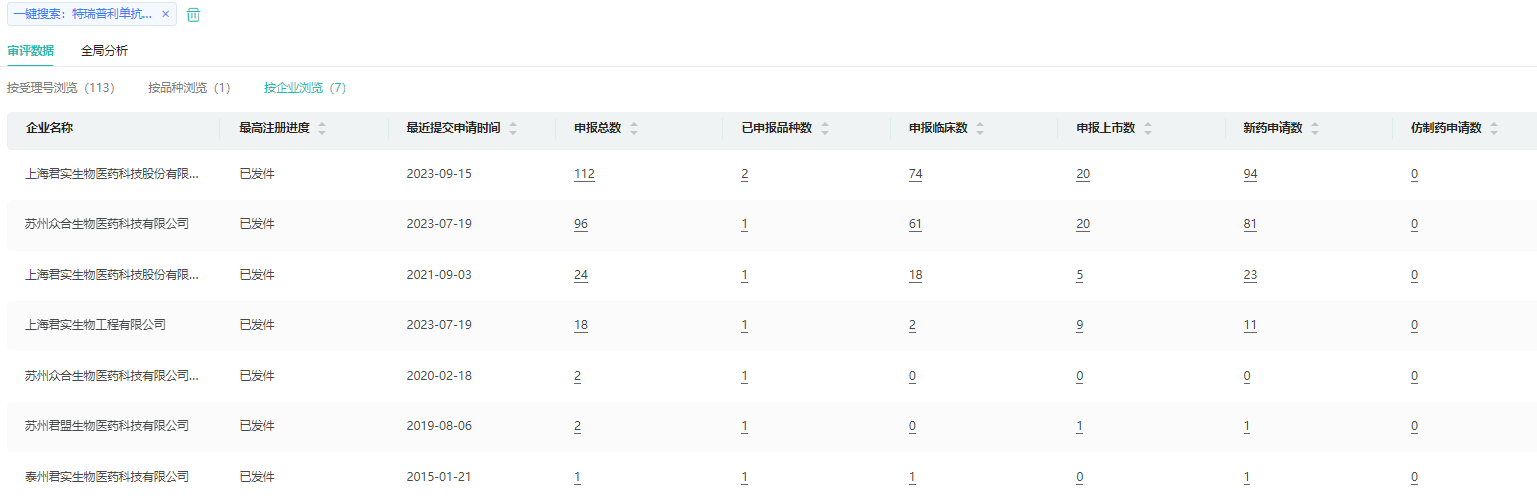
截图来源:药融云中国药品审评库
在国际化布局方面,特瑞普利单抗已在黏膜黑色素瘤、鼻咽癌、软组织肉瘤、食管癌、小细胞肺癌领域获得美国食品药品监督管理局(FDA)授予2项突破性疗法认定、1项快速通道认定、1项优先审评认定和5项孤儿药资格认定。
参考资料:
1.公司官网
2.药融云数据库
<END>
要解锁更多企业药品研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药品各国上市情况、药品批文信息、销售情况与各维度分析、市场竞争格局、一致性评价情况、集采中标情况、药企申报审批信息、最新动态与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!







































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论