一、创新驱动,生物领先
根据药融云数据库(www.pharnexcloud.com)显示,2020全年全球首次上市了140个药物,其中21个在首次我国上市的药物中有14个生物药,生物创新药逐渐成为我国研发主流趋势。随着政策的推进和技术的发展,医药行业由创新主轮驱动的生态环境逐步形成,我国药物研发结构正在进行调整。
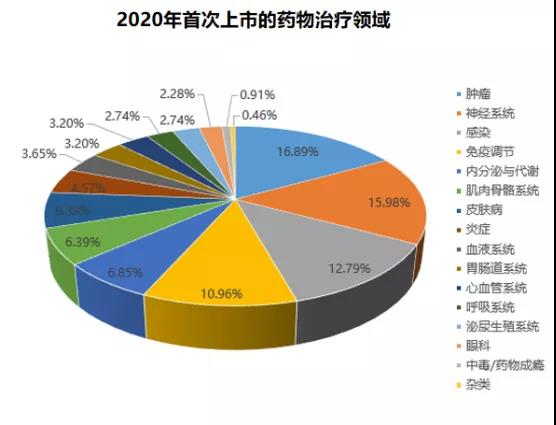
目前全球防治重大疾病的迫切需求和新药研发领域的热点依然是针对恶性肿瘤、神经退行性疾病、病毒性传染病以及自身免疫性疾病等。根据上图可以发现,其中占据最主要领域的是抗肿瘤药。除去生物类似药(biosimilar)外,抗肿瘤生物新药(bionovel)是未来创新药研发的主战场之一。
二、单克隆抗体药物
生物药包括单克隆抗体(含双抗)、ADC、重组治疗性蛋白、疫苗、血制品、细胞与基因治疗以及其他生物疗法等。单克隆抗体是由单一B细胞克隆产生的高度均一、仅针对某一特定抗原表位的抗体,可以与相应抗原发生特异性结合反应的免疫球蛋白。经过长期发展,单抗药物已经进入技术成熟阶段。
其中“药王”阿达木单抗(商品名“修美乐”)最为人所知。修美乐是由艾伯维(Abbvie)公司研发的第一个完全人源化抗肿瘤坏死因子-α(TNF-α)的单克隆抗体。根据公开资料,修美乐于2002年在美国经FDA批准上市,并在2010年进入中国市场。2012年之后,阿达木单抗就一直雄居全球处方药销售额的榜首。在2020年全球销售额为198.32亿元。上市以来,已治疗了超过百万名罹患免疫疾病的患者,大大改善了类风湿关节炎患者的残疾率。目前,阿达木单抗销量依然位居全球畅销药品前列,同时还保持着20%以上的增长率。

百奥泰,全称百奥泰生物制药股份有限公司,是一家成立于2003年7月28日的创新型生物制药企业,作为医药行业的老牌劲旅,它主要从事用于治疗癌症、自身免疫性疾病、心血管疾病的新一代抗体创新药和生物类似药的研发。公司于2020年2月正式在上交所科创板挂牌交易,股票代码为688177。
2020年11月7日,格乐立®获批上市。格乐立®是百奥泰公司自主开发的阿达木单抗注射液,也是首个获批上市的国产阿达木单抗生物类似药,可治疗类风湿关节炎、强直性脊柱炎、银屑病、克罗恩病、葡萄膜炎、儿童银屑病和幼年特发性关节炎等自身免疫性疾病。
三、持续投入研发,暂时扭亏为盈
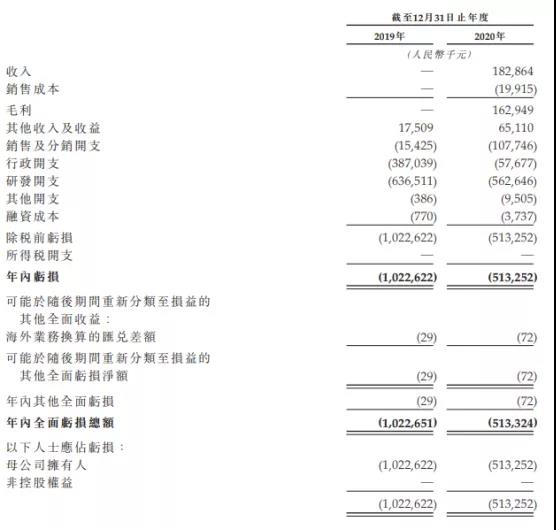
(2020年全年业绩,来源于公司港股招股书)
众所周知,生物医药领域研发活动具有技术风险高、研发周期长、资金投入大的特点。百奥泰由于其生物药产品管线丰富,投入了较大的研发资金。目前公司仅阿达木单抗于2020年上市销售,其他产品尚在市场拓展阶段,因此营业收入尚处于增长期,预计下一报告期末公司依然继续产生亏损。
百奥泰2020年年报显示,截至2020年12月31日,公司实现2020年全年营业收入1.85亿元;研发费用(R&D)5.62亿元;营业收入较上年同期增加了1.84亿元,主要原因为报告期公司的产品格乐立开始上市销售并产生了营业收入。根据公司2020年财报显示,百奥泰生产格乐立®24.3万支,销售约20.9万支,全年实现营业收入1.85亿元,实现主营业务收入的零突破,归母净利润为-5.13亿元。尽管如此,公司表示未来需持续较大规模的研发投入用于在研项目完成各类商业化推进,因此依旧会在下阶段处于亏损状态。
2021年7月29日,百奥泰披露2021年半年度业绩预告,公司预计2021年上半年度实现归属于母公司所有者的净利润为230万元到330万元,与上年同期相比增加2.46亿元到2.47亿元,公司预计归属于母公司所有者扣除非经常性损益后的净亏损为1,400 万元到1,700万元,相比上年同期减少亏损2.39亿元到2.42亿元。公司表示在2021年4月9日与 Biogen International GMBH 签署 BAT1806(托珠单抗)授权许可与商业化协议,并且完成了协议中约定的 3,000 万美元首付款(upfront)的条件,2021年7月21日百奥泰宣布收到由 Biogen 支付的 2,859 万美元首付款,公司预计该款项将对 2021 年上半年度业绩产生积极影响。不仅如此,预告期内公司积极拓展市场,业务规模逐步扩大,格乐立销量明显增加,预计药品销售收入较上年同期增加6,800万元到7,800万元,同比增长140%-160%。(公司将于8月28日披露半年报,药融圈将持续关注)

四、布局肿瘤免疫,管线多样化
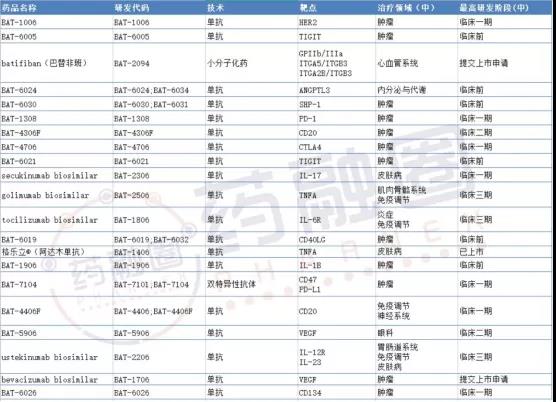
(百奥泰最新研发管线一览(截止2021年8月20日))
五、获批临床
根据药融云数据库(www.pharnexcloud.com)显示,BAT2306、BAT6026(OX40抗体新药)、BAT6021和BAT6005 这4 款单抗都已经获批临床。

2款 TIGIT新药
(1)BAT6021注射液:BAT6021是一款T细胞免疫球蛋白和ITIM结构域蛋白(TIGIT)单克隆抗体。位于免疫细胞表面的TIGIT与肿瘤细胞表面CD155结合,会抑制T细胞/NK细胞介导的肿瘤免疫激活,通过结合TIGIT蛋白,阻断导致肿瘤免疫耐受通路,重新激活淋巴细胞的抗肿瘤活性,从而达到治疗肿瘤的目的。2021年7月7日获批临床,适应症为晚期恶性实体瘤。
(2)BAT6005:是一款具有正常Fc效应功能的IgG1亚型抗TIGIT单克隆抗体,拟开发用于肿瘤治疗。TIGIT是一种免疫球蛋白超家族蛋白,高表达于激活的NK细胞、CD4+T细胞、CD8+T细胞以及免疫抑制Tregs细胞表面,2021年7月20日宣布获批临床。
BAT7104:BAT7104是靶向PD-L1/CD47的双特异性抗体药物,旨在抑制PD-1/PD-L1和CD47/SIRP-α途径。2021年8月10日,药审中心受理公示了百奥泰1类生物制品BAT7104注射液的临床申请。这个是百奥泰首款双抗新药申请。
六、临床一期阶段
HER2 单抗 BAT1006 、 CTLA4 单抗 BAT4706、PD-1单抗BAT1308和BAT4406F 以及IL-17单抗BAT2306推进了临床一期。百奥泰研发管线中有两款靶点为CD20的抗体新药,分别为BAT4406F、BAT4306F,其中BAT-4406F处于临床一期,是国内首家依据具体国情针对视神经脊髓炎谱系疾病适应症开发的靶向药物,BAT4306F用于治疗复发/难治CD20阳性B细胞性非霍奇金淋巴瘤,均属于1类新药。
七、临床二期阶段
BAT5906是百奥泰自主研发的1类抗VEGF新药,通过与人VEGF进行特异性结合而发挥药效,目前处于临床二期阶段。
八、临床三期
戈利木单抗生物类似药 BAT2506 和乌司奴单抗生物类似药 BAT2206 以及IL-6R单抗BAT1806启动了临床三期。
BAT1806(托珠单抗):由公司自主研发的重组人源化抗白介素6受体(IL-6)单克隆抗体BAT2506(戈利木单抗):全球首项的欣普尼候选生物类似药,戈利木单抗可靶向抑制 TNF-α 活性,适用于强直性脊柱炎及类风湿性关节炎等免疫疾病患者。
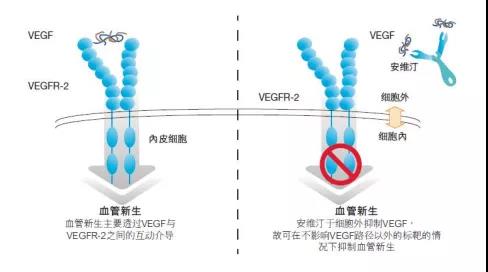
(BAT1706作用机制,图源自公司年报)
九、提交上市阶段(BLA/NDA)
BAT1706(贝伐珠单抗)目前处于中国、美国、欧盟上市申请阶段,为中国公司首项开发并开展全球多中心临床试验的安维汀候选生物类似药,公司就BAT1706已与百济神州、巴西的 Biomm 及海外的 Cipla Limited 公司进行商业合作license out,以拓展更多的全球市场份额。

BAT2094(巴替非班)目前处于国内上市申请阶段,为一项小分子 GPIIb/IIIa 拮抗剂候选药物, 标示为用于预防进行 PCI 疗程的 ACS 患者出现血小板聚集诱发的血栓形成。
十、新药研发:失败常伴左右
2021年3 月 4 日,百奥泰宣布已终止 Trop-2 靶向 ADC BAT8003 以及 PD-1 单抗 BAT1306 的临床试验。这是百奥泰今年终止的第 3 个项目,此前于 2 月 9 日,百奥泰已经终止了其 HER2 靶向 ADC BAT8001 项目,3 个项目累计已投入近 3.4 亿元。
终止BAT8001、BAT8003及BAT1306的临床试验,致使百奥泰的ADC 管线遭受失败,公司重新将管线开发重点转向了肿瘤免疫领域,一时之间也引发了医药界的讨论热潮,再一次让人明白新药研发的高失败率。
创新药的诞生不仅要耗费巨大人力、物力还有时间成本;药物开发本就不是一件容易的事情,百奥泰主动公开去披露自己研究项目在临床三期试验结果不达标,实际上也是一次新的突破,在大家留下深刻印象的同时也给予了一定鼓舞,即使是失败了,但是这意味着我国医药产业未来依然可以实现更大的进步,失败只会给我们总结经验教训,以求未来达到更高的标准。
百奥泰创始人、总经理李胜峰博士表示尽管公司的ADC药物被叫停,但是接下来公司将会开发新的ADC平台,包括新的连接子(linker)和毒素,也会进一步研发出更多候选产品,失败对于这个创新企业来说将会成为日后前进的动力。
新药研发及上市是项长期工作,存在诸多不确定因素,易受到技术、 审批、政策等多方面因素的影响,临床试验进度及结果、未来产品市场竞争形势均存在诸多不确定性,然而,百奥泰已经从早期的布局多种生物类似药逐渐向创新生物药进军,进一步加大新药研发,敢于及时遏制投入巨大的新药项目转而继续研发其他热门靶点,管线丰富却依然处于早期阶段,这对公司来说面临重重挑战的同时又充满希望,随着往后研发进程的不断推进,成功与否依然需要时间的证明。公司布局的临床前靶点还有:CD40抗体、IL-1β抗体、ANGPTL3新药、长效VEGF、EGFR/VEGF、等等。

十一、发展历程
2003年7月,百奥泰生物科技(广州)有限公司正式成立
2013年3月,向前国家CFDA递交“重组人抗TNF-α单克隆抗体注射液”(BAT1406)临床试验申请
2014年1月,向国家CFDA递交“重组人源化抗VEGF单克隆抗体注射液”(BAT1706)临床试验申请
2015年12月,“重组人抗TNF-α单克隆抗体注射液”BAT1406获临床试验批件
2016年,“重组人源化抗VEGF单克隆抗体注射液”BAT1706、“注射用重组人源化抗HER2单克隆抗体-美登素偶联物”(BAT8001)获国内临床试验批件;递交“重组人源化抗IL-6受体单克隆抗体注射液”临床试验申请
2017年11月,“重组人源化抗IL-6受体单克隆抗体注射液”获国内临床试验批件
2018年3月,重组Fc糖基化修饰抗CD20人源化单克隆抗体注射液获得国内临床试验批件
2019年11月,公司名称变更为百奥泰生物制药股份有限公司,格乐立®(阿达木单抗注射液)获得国家药监局批准上市
2020年,百奥泰登陆上交所科创板,与Pharmapark就BAT2506在俄罗斯及其他独联体国家达成合作;与Biomm公司就BAT1706在巴西达成合作;与百济神州就BAT1706签订在中国的授权、分销、供货协议
2021年4月,百奥泰与Biogen公司就BAT1806达成合作







































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论