
2024年12月11日,广东东阳光药业股份有限公司已中国香港联交所提交上市申请。这标志着东阳光集团医药资产资本运作的重要一步,东阳光药研发、生产和销售一体化进程全面提速。

BD&L :
2024年11月,东阳光药的 HEC88473( FGF21/ GLP-1 双受体激动剂)大中华区以外地区权益与Apollo Therapeutics Group Limited(APL-18881)达成授权许可,其中包括 1200 万美元的首付款和最高 9.26 亿美元的开发、监管及商业里程碑付款。
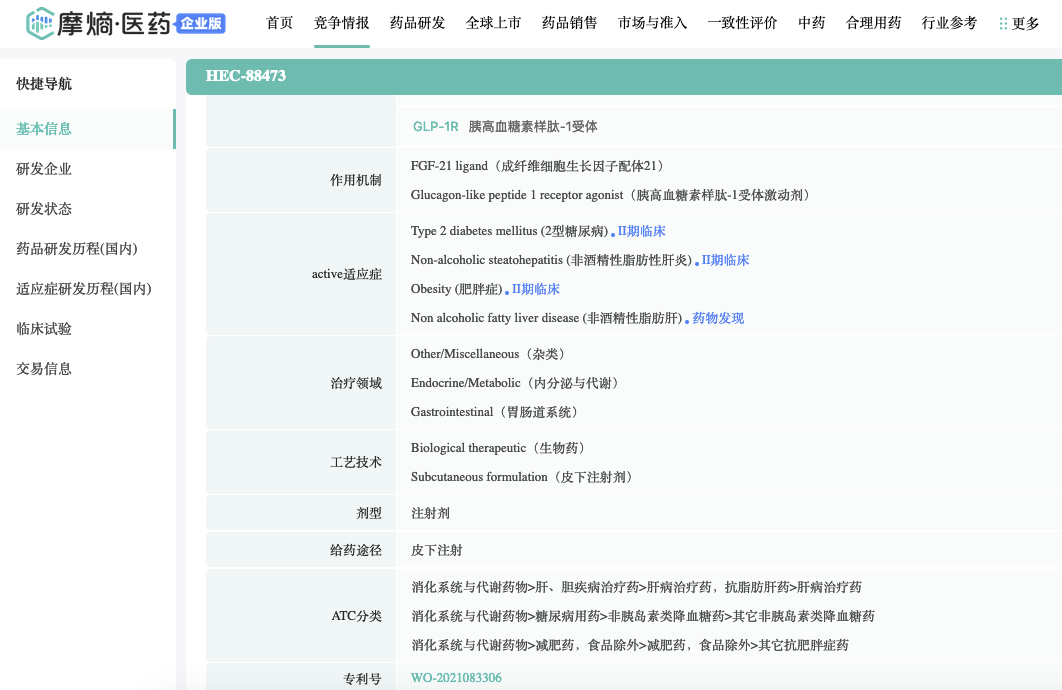
截图来源:摩熵医药数据库
也在上月,克立福替尼(第二代高选择性FLT3口服小分子抑制剂)在中国大陆的商业化权利独家许可给上市公司三生制药。东阳光药在协议有效期内将获得6000万元首付款,以及有望获得研发注册及商业里程碑付款。研发注册里程碑付款取决于是否能达到协议的研究阶段及特定监管机构的批准。商业里程碑付款则取决于能否在各主要市场达到协议的年销售额。在克立福替尼在中国首次商业销售并回款后以及在协议有效期内,东阳光药将每月向沈阳三生支付其该月相关净回款到账金额的约定百分比作为服务费。合作协议的有效期为签署日起到首次商业销售之日起至少15年。同时,东阳光药将继续负责克立福替尼的研发、注册(包括作为上市许可持有人(MAH))和生产;沈阳三生将独家负责克立福替尼在中国大陆的商业化。
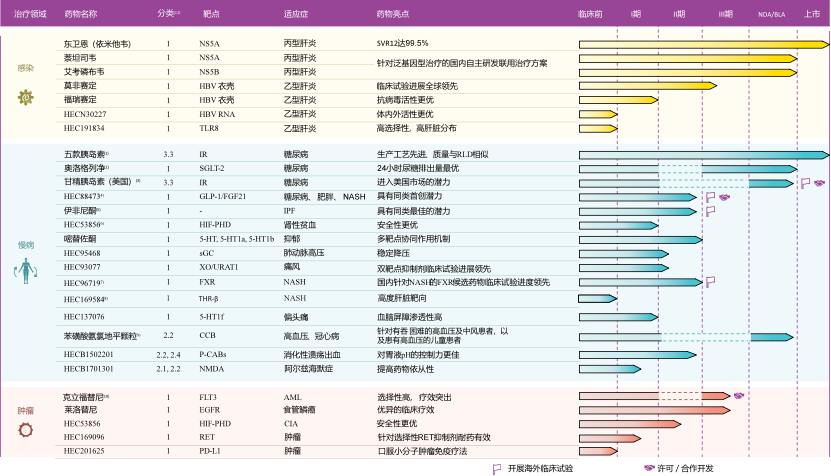
从最新招股书获悉:截至2024年6月30日,广东东阳光药业股份有限公司在全球(包括中国、美国及欧洲)拥有147款获批药物,还有超过100款在研药物,包括45款1类在研创新药物,其中3款创新药已处于NMPA中国上市评审阶段,10款在研创新药物处于2期或3期临床试验。该公司在战略重点治疗领域(包括感染、慢病及肿瘤)拥有多元化的产品组合。
























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论