
12月16日,据CDE网站最新公示,东阳光药业申报的1类新药HEC169584胶囊获得临床试验默示许可,标志着该药物正式进入临床试验阶段,拟开发治疗非酒精性脂肪性肝炎(NASH)。HEC169584是一款用于治疗NASH的在研THR-β激动剂药物。

截图来源:CDE官网
据摩熵医药数据库显示,HEC169584是东阳光药业AI驱动药物设计(AIDD)实验室精心研发的首款小分子新药候选物,专门针对NASH这一严重且治疗难度大的疾病。临床前研究结果显示,HEC169584在体外对THR-β细胞表现出高度的活性,并且具有改善肝纤维化的潜力,为NASH患者提供了新的治疗选择。
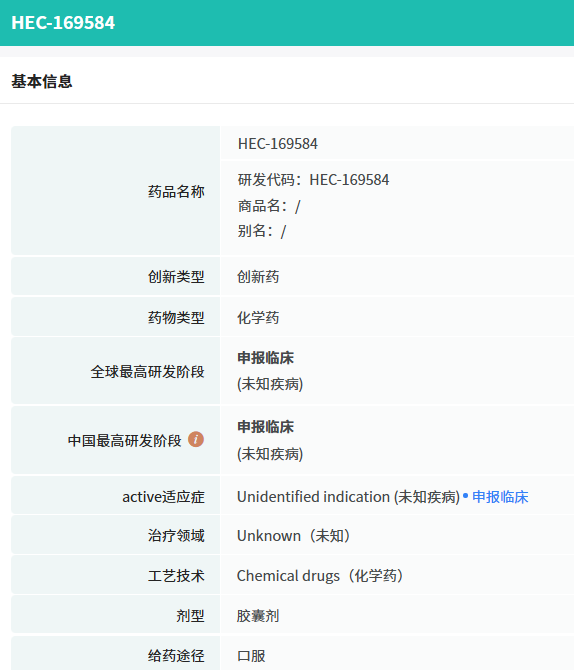
截图来源:摩熵医药全球药物研发数据库
从2024年10月15日在国内首次申报临床,到12月16日获得CDE的临床试验默示许可,HEC169584的研发进程体现了东阳光药业在创新药物研发领域的实力和效率。这一重要里程碑的达成,为药物的后续开发和上市奠定了坚实的基础。


















































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论