
近日,亚虹医药(股票代码:688176.SH)公开宣布,其自主研发的APL-2302(一种泛素特异性蛋白酶1,USP1抑制剂)用于治疗晚期实体瘤的新药临床研究(IND)获美国食品药品监督管理局(FDA)批准。
方达医药携手母公司泰格医药为该项目提供了IND大包服务。方达医药主要提供了从API,制剂,到DMPK,毒理等实验室服务;泰格医药主要提供了注册,临床资料支持等服务。在项目执行过程中,方达医药,泰格医药与亚虹医药保持紧密沟通,及时解决项目中遇到的问题,为APL-2302的IND获批提供了重要支持。



APL-2302是亚虹医药自主研发的USP1抑制剂,通过“合成致死”机制发挥抗肿瘤作用。在临床前研究中,APL-2302单药治疗和联合治疗在肿瘤抑制方面表现出良好的体外和体内活性,有潜力成为治疗特定生物标志物阳性(如BRCA基因突变等)的晚期实体瘤(乳腺癌、卵巢癌、前列腺癌等)的新选择。
方达医药是全方位的医药研发CRO公司,自成立以来,始终坚守“中美两国,同一质量体系”准则,获得的试验数据支持多国申报。目前已顺利通过60多次美国FDA和 150多次 NMPA的现场核查。长期致力于助力客户提升研发效率,为患者带来更多突破性的治疗方案。

本文资料来源参考:亚虹医药

方达医药
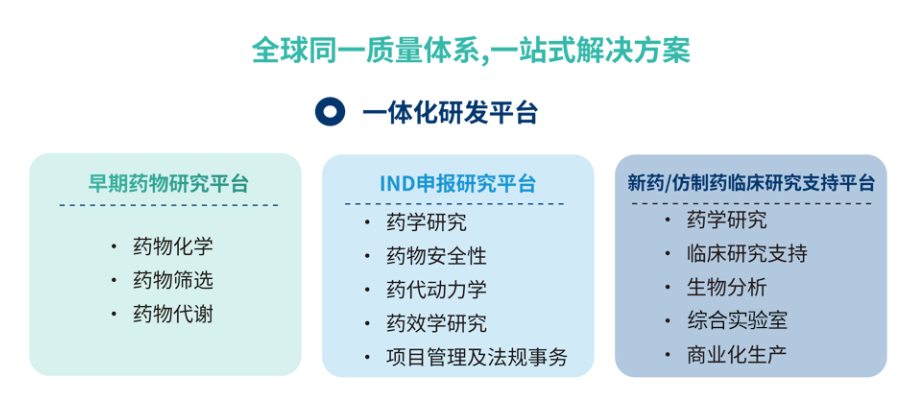
方达医药是全方位的医药研发CRO公司,在中国和北美分别建有生物分析中心,制剂产品开发中心,临床运营中心,药化中心,药物筛选中心和临床前安评中心。为全球药企提供药物化学、药物活性筛选、药学研究、DMPK、临床前安评、生物分析、综合实验室和临床研究等一站式研发外包服务。
方达医药始终坚守“中美两国,同一质量体系”准则,获得的试验数据支持多国申报。运营20多年来,方达医药建立了经验丰富的科研团队和坚实的质量管理体系,目前已顺利通过60多次美国FDA和150多次NMPA的现场核查。
方达医药
★
NEWS
★

• 官网|www.frontagelab.com •
• 邮箱|Marketing@frontagelab.com.cn •
• 招聘|Weiyang@frontagelab.com.cn •




































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论