
2024年5月20日,Dyne Therapeutics公开募资3亿美元,同时也公开了两款抗体核酸偶联药物(AOC)DYNE-101和DYNE-251的最新临床结果。当日股价上涨27.82%,截至当前市值为27.31亿美元。

其中DYNE-101靶向DMPK的AOC药物,正处于1/2期临床试验。同类型的竞争对手是Avidity Biosciences的AOC-1001,即将进入3期临床试验。本文将从多方面进行2款药物对比。

一、分子设计
DYNE-101和AOC-1001均由三部分构成,但整体差异较大。
DYNE-101采用Dyne 的FORCE平台技术制造,抗体部分为TfR1 Fab,连接子根据专利推测为可裂解型MC-Val-Cit,核酸部分为DMPK ASO。
AOC-1001采用Avidity 的HARBOR平台技术制造,抗体部分为Fc端沉默的TfR1 人源化IgG1抗体,连接子为不可裂解型MCC,核酸部分为DMPK ASO。
二、作用机理
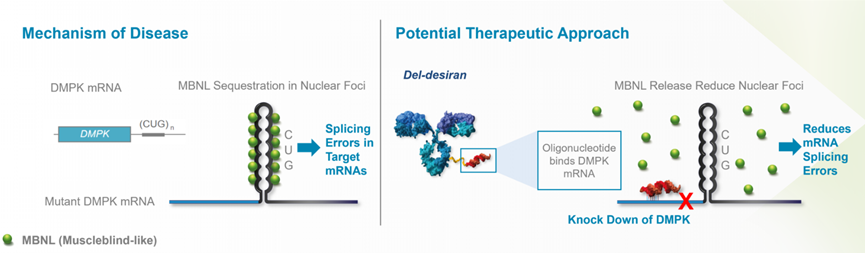
DM1 是由DMPK基因中 CUG 三联体重复数增加引起的。正常人中的CUG重复数约为 35,但 DM1 患者的重复数可达上千个。当CUG重复数过多时,会形成大发夹环,将DMPK mRNA 困在细胞核中,与MBNL 蛋白结合,形成核灶,并阻止 MBNL 发挥其处理许多其他基因的 mRNA 的正常功能,产生非典型蛋白质,最终导致 DM1。
DYNE-101和AOC-1001通过TfR1受体,定向递送至肌肉组织,携带的小核酸完成内体逃逸后,进入细胞核,降解DMPK mRNA,释放MBNL。
三、研发进展
目前,AOC-1001研发进度至少领先DYNE-101两年,而且最近获得了突破性疗法认定,最快预计2028年上市。而Dyne正在为DYNE-101寻求加速批准机会,预计在2024年底完成。
DYNE-101研发历程如下:
· 2022年5月2日,临床前研究数据公布(ASGCT)
· 2022年6月12日,新西兰 IND申请通过
· 2022年9月5日,开展DM1临床1/2期研究(NCT05481879)
· 2023年5月25日,获得美国孤儿药资格认定
· 2023年9月19日,获得欧盟孤儿药资格认定
· 2024年5月20日,临床结果公布
AOC-1001研发历程如下:
· 2021年4月18日,临床前研究数据公布(AAN)
· 2021年7月21日,获得美国孤儿药资格认定
· 2021年8月24日,获得欧盟孤儿药资格认定
· 2021年10月18日,获得美国快速通道资格认定
· 2021年10月28日,开展DM1临床1/2期试验(NCT05479981)
· 2022年8月4日,开展DM1临床2期试验(NCT05479981)
· 2022年12月14日,临床1/2期试验结果公布(MDA)
· 2024年3月3日,临床2期试验结果公布(MDA)
· 2024年5月1日,开展DM1临床3期试验(NCT06411288)
· 2024年5月8日,获得美国突破性疗法资格认定
三、临床疗效
根据AOC-1001和DYNE-101最新结果分析如下:
1. 基线数据
DYNE-101试验患者相比AOC-1001更加年轻,AOC-1001试验中招募了更多的女性患者,此外在10-meter walk run test 中,AOC-1001试验中的患者表现更差。其余相同指标表现一致。

2. 有效性
vHOT全称为Video Hand Opening Time,要求受试者进行最大程度的握力 5 秒,然后快速伸展手指,手不抖动,分别测量拇指和中指的最大张开时间,用于评估肌强直,数值越小越好。
试验显示,两者都能显著改善vHOT指标。其中,DYNE-101在低剂量(1.8mg/kg)下,可达到与AOC-1001高剂量(4mg/kg)相似疗效,DYNE-101高剂量(5.4mg/kg),已初步显示出更好的疗效。

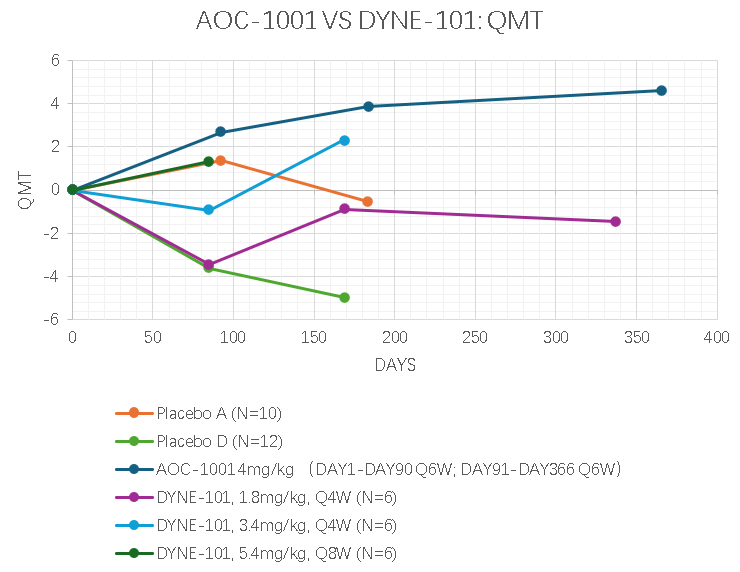
QMT,全称为quantitative muscle testing,使用测力计等设备,测试包括手、肘、膝盖和脚踝多个肌群的肌肉力量,数值越大越好。

在QMT指标上,AOC-1001表现更好,DYNE-101 高剂量(5.4mg/kg)预计能够达到类似效果。
DM1-Activ是一种患者报告结果量表,包含25个问题,数值越大越好。
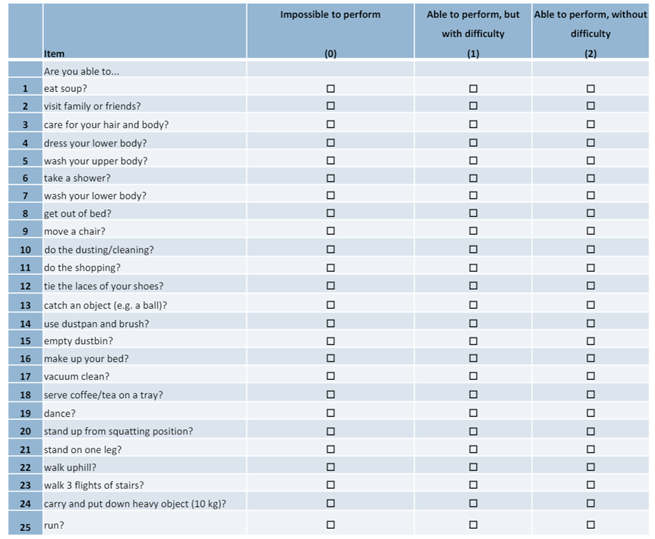
从DM1-Activ来看,DYNE-101在中剂量组(3.4mg/kg)表现于与AOC-1001相似。根据前面指标表现,预计DYNE-101 5.4mg/kg 效果会更好。
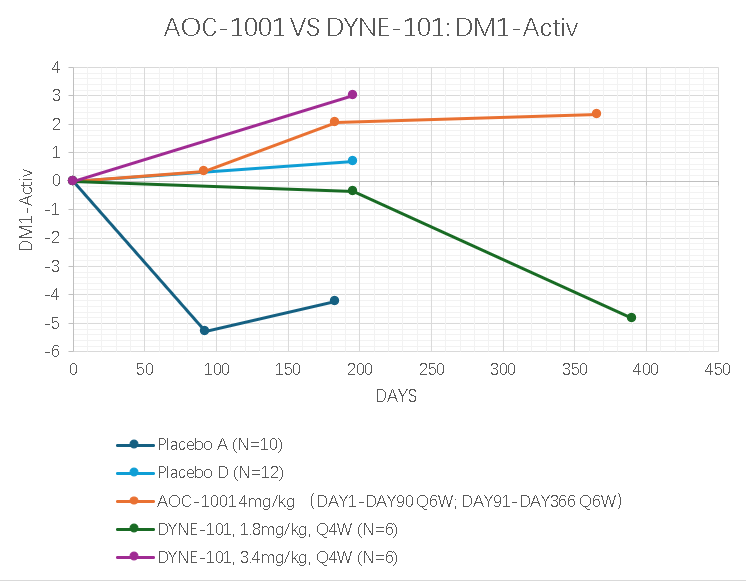
DYNE-101剂量已经爬坡到6.8mg/kg,计划最高爬升至10.2mg/kg,以获得注册性数据,疗效可能会有更大的提升。
3. 安全性
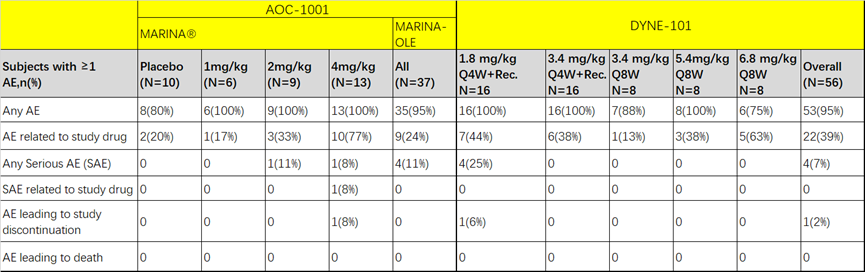
两者都表现出剂量依赖的不良反应。DYNE-101相比AOC-1001安全性更好,治疗相关AE发生率和SAE都低于AOC-1001,显示出更高的治疗指数。
AOC-1001最常见的不良反应为恶心和头痛。DYNE-101最常见的不良反应为鼻咽炎、程序性疼痛、流感、发热、腹泻、头痛和背部疼痛。
四、市场规模
根据Dyne估算,美国DM1患者超过4万人,欧洲DM1患者超过7.4万人。
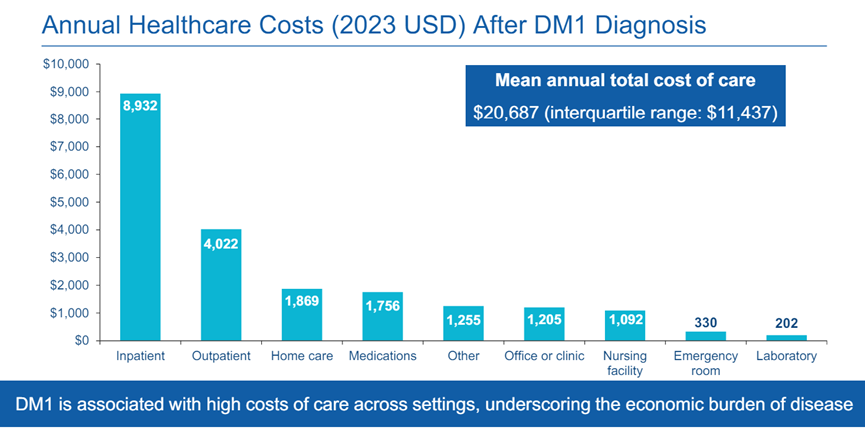
根据URMC和Dyne合作的真实世界研究数据显示,美国DM1患者平均每年医疗支出为2万美元,大部分为住院费用,其中医药费为1700美元。综合以上数据来看,DM1欧美国家医药市场规模在24亿美元。
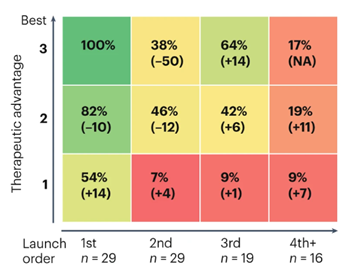
根据BCG 2023年上市顺序对药物销量影响研究,假设AOC-1001治疗优势为2,DNYE-101治疗优势为3,并且AOC-1001早于DNYE-101上市,市场份额将会接近2比1。目前暂无有效治疗手段,因此AOC-1001的峰值销售额可能为12亿美元,而DNYE-101的峰值销售额可能为6亿美元。
五、总结
DYNE101分子设计与AOC-1001差异较大,作用机理相似。在临床试验中,DYNE101表现出了更好的疗效和更高的安全性,但是在研发进度上稍显落后,对后续上市销售额可能会有较大影响。目前DM1没有较好的治疗手段,期待AOC-1001和DYNE101能够早日上市,造福患者。
参考来源:
1.Dyne Therapeutics 官网
2.Avidity Biosciences官网
3.Nature Reviews Drug Discovery 22, 531-532 (2023)
4.WO2020028861A1
<END>
想要解锁更多药物研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!






































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论