
摘要
喷雾冷冻干燥是一种相对较新的干燥技术,涉及的步骤包括:液滴形成、冷冻和升华。与其他干燥方法相比,它的优势在于生产出的产品具有更高的结构完整性、优良的质量和更好的货架稳定性。凭借这些优点,喷雾冷冻干燥已在药物递送领域获得了大量应用。喷雾冷冻干燥产生的颗粒在肺、鼻粘膜、肠道和皮肤中表现出更高的稳定性。与传统干燥技术相比,这些颗粒还具有通过各种递送途径持续释放和特异性的重要特性。推动了喷雾冷冻干燥药物的商业化市场。本文重点介绍了喷雾冻干粉的制造方法和其在药物传递系统中的应用。还概述了喷雾冷冻干燥的其他应用。
1.介绍
人体是复杂器官的组合体,容易发生疾病。使用药物来治疗不同的疾病,涉及不同的递送系统。药物递送系统(DDS)是指将药物或生物分子引入生命系统以达到积极治疗效果的方法。DDS的主要是开发靶向治疗,在目标区域使药物制剂达到最佳释放。DDS旨在通过减少与药物消耗相关的副作用来延长人类寿命。药物递送方法分为传统系统和新型系统。
1.1传统的药物传递系统
传统的DDS包括口服给药、颊/舌下给药、直肠给药、静脉给药、皮下给药和肌肉内给药。而且传统的DDS具有一定的局限性,会产生依从性差、生物利用度低、药物浓度波动大,还会使蛋白质和肽相关的药物发生酶降解、分子大小变化和电荷效应,导致治疗效率降低。此外,该DDS还具有非特异性的特点。目前需要新型DDS来完善传统DDS的不足。
1.2新型给药系统
新型DDS具有更安全的药物输送和更长的药物半衰期,以及可开发用于药物缓释和靶向递送的新概念和技术。在靶向DDS中,药物被靶向并递送到特定部位(结肠、肺等),药物在此处释放,避免了首过效应,副作用最小,治疗效果更好。这种新型的DDS通过在指定的时间段内以预定的速率输送药物,解决了与常规药物输送相关的问题。该DDS采用不同的技术制备,使用载体或标记物,如脂质体、纳米颗粒、微球、微乳液、单克隆抗体、纳米混悬剂、重新密封的红细胞和胶束。制剂在经过喷雾干燥(SD)、冷冻干燥(FD)、沉淀和喷雾冷冻干燥(SFD)过程制备后,应用到人体。
对生产温度、pH和盐浓度敏感的药物来说,SFD制备方法是绝佳的选择。SFD方法可以很好地控制制剂的粒度,且制备过程中使用快速冷冻的方法,避免了药物和赋形剂之间的相分离范围,提供了更好的分子分布并。同时,避免了SD使用高干燥温度和FD工艺耗时等问题,且设备成本远远低于FD。
与FD中生产的高孔隙率的饼状结构不同,SFD制备的粉末是球形的,具有光滑的形态。本综述重点介绍SFD用于DDS的新型应用。
2.喷雾冷冻干燥
SFD是一种干燥工艺,应用于制药技术领域和食品技术领域。SFD已被用于生产高活性的微囊益生菌细胞和具有高质量的脱脂奶粉。由于涉及低温制备,所以可以保护高挥发性的化合物。
SFD按照应用可以分为三类:(1)高价值食品;(2)药品;(3)活性成分。前两类侧重于干燥作为单元操作,后者侧重于封装感兴趣的成分。
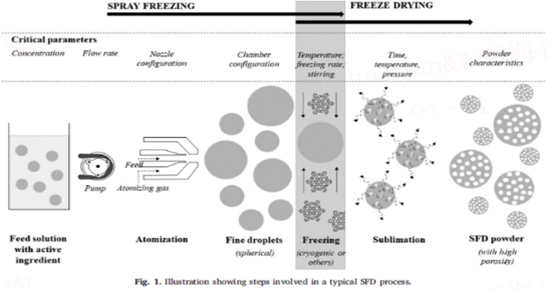
众所周知,SFD(Fig.1)是两种干燥技术(即SD和FD)的组合。典型的SFD过程中涉及三个主要步骤:将液体分散成液滴,通过冷冻使液滴凝固,在低温下进行真空干燥。在SFD技术中,雾化是将液体分解成较小液滴的主要步骤。影响雾化的因素包括喷嘴类型、料液粘度、雾化能量、进料流速和表面张力。
2.1 SFD在输送系统中的应用
世界纳米技术的发展引起了制药领域对改进靶向给药系统的需求。SFD具有改进药物粉末的物理性能和治疗特性。前者侧重于粒径分布、空气动力学行为和体积密度,后者指的是其在生物系统中的活性,目前已证明SFD在疫苗、胰岛素、干质粒、阿霉素和重组人血管内皮生长因子(rHEGF)中的潜力。
2.1.1口服给药
与其他药物递送途径相比,口服途径被认为是最优选的药物递送途径,其优点是不会引起任何组织损伤或受试者的感觉不适。口腔是口服给药途径的第一步,由角质化区、舌下区、颊部和非角质化区域等黏膜层组成。疫苗最好能用口服给药,因为能以较低的成本向受试者提供保护。同时指出,口服胰岛素能较好地维持血糖稳态,并被认为是胰岛素输送的最佳方法,因为它可以适当地释放激素以补偿糖尿病的代谢异常。研究人员认为口服给药是最优选的非侵入性给药途径。还强调了低无菌限制、药物剂量的灵活性、生产的便利性、更好的患者依从性和相对较低的成本,作为口服 DDS 的附加优势。
胃肠道(GIT)中的药物稳定性和吸收高度依赖于个体的生理和药物的性质等因素相关。通常,药物的口服生物利用度都以溶出度、渗透性和溶解度表示。由于 GIT 中涉及复杂的代谢,口服药物在目标部位的作用仍面临一些挑战。口服给药的主要挑战来自胃肠道,如吸收减少就会导致其在肠上皮细胞的生物利用度差。另外,胃中的pH值也会导致给药药物的更高降解率。为了克服这些问题,应该对药物进行修改,以通过靶向给药来保正其在特定部位的作用。减小药物制剂尺寸可以增加表面积,以获得更好的药物溶解和扩散速率。
为提高维生素E的口服生物利用度而进行的一项研究中,使用SD、FD和SFD等不同技术进行了微胶囊化。研究结果表明,SFD生产的多孔颗粒具有更高的溶解速率。同时,发现SFD技术制备的维生素E具有最高的口服生物利用度。阿奇霉素是一种高度不溶于水的抗生素,但使用SFD技术可以提高阿奇霉素的口服生物利用度。研究表明,使用SFD技术生产的脂溶性药物,溶出度会提高8.9倍。如图2阿奇霉素的光滑球形(图2C和2D),其天然不规则形状(图2A和2B)。聚集效应明显并且观察到皱褶形态,阿奇霉素表面积的减少归因于SFD过程,从而导致药物分子在载体内明显分散,颗粒表面光滑与进料浓度有关。可通过化学修饰、共溶性、pH调节、微粉化固体分散等方法改善难溶性药物的溶解度,从而使药物通过口服途径获得生物利用度。除了药物外,SFD还用于包封植物乳杆菌,包括植物乳杆菌、干酪乳杆菌和副干酪乳杆菌等多种益生菌菌株。结果表明,与其他技术相比,该技术提高了口服生物利用度。因此,SFD可用于改善脂溶性药物的口服生物利用度。
2.1.2肺部给药
由于肺部给药方法是非侵入性的,药物的肺部输送受到了极大的关注。该方法在各种呼吸系统疾病的治疗中起着至关重要的作用。人肺的更大表面积和更高的溶质渗透性改善了通过肺部途径的药物递送。肺部给药的优点,避免首过代谢和上皮细胞的薄壁,有助于各种疾病的治疗。肺部药物输送的机制包括惯性撞击、重力沉降和布朗扩散。用于向肺部给药的递送装置包括雾化器、加压计量吸入器和干粉吸入器。动物和人体研究都证明了使用肺DDS的潜力。制备用于鼻腔递送的颗粒必须满足不会在鼻腔中产生任何刺激或不适。此外,颗粒尺寸的过度减小可能会导致其转运到肺部深处。
对于在肺中靶向递送药物,空气动力学粒径起着重要作用。较轻的颗粒比较重的颗粒在空气动力学上更好,因为较轻的颗粒可以递送到深入肺内,从而获得药物的有效吸收。如前所述,空气动力学直径范围在1-5μm的颗粒非常适合吸入,它可以更好的递送至肺部。
从表1中可以明显看出,大多数喷雾冷冻干燥药物可用于肺部靶向。空气动力学颗粒尺寸是控制这种系统中颗粒输送的主要因素。在肺DDS中,颗粒的性质及其大小起着重要作用。由于碰撞效应,最大尺寸颗粒会滞留在呼吸道的上部。尺寸范围为1-5μm的超细粉末悬浮在呼吸道的肺泡区域,因此该尺寸可以达到有效的药物输送。对于经鼻给药,颗粒的空气动力学直径应为4.8-23μm;而对于表皮给药,空气动力学直径应在40-70μm的范围内。除了粒径分布外,药物的溶解度对于在体内实现所需活性和全身循环也起着重要作用。
干粉吸入剂的应用已在生物制药中广泛应用,制备干粉的方法有:SD、机械研磨和沉淀技术等。SD技术可生产规定尺寸范围内的自由流动粉末,缺点是在入口处温度较高,容易发生使材料变性和热降解。使用SD和SFD制备了一种蛋白质吸入粉,且均使用双流体喷嘴系统。喷雾冷冻干燥颗粒显示出多孔性质,具有改善的表面积和球形形态,空气动力学直径为2.7μm。然而,喷雾干燥的颗粒是球形和凹坑结构,空气动力学直径为3.5μm。使用级联冲击器确定SD和SFD颗粒的细颗粒分数,以确认所生产粉末的空气动力学粒径。在撞击器的不同阶段收集粉末,并在扫描电子显微镜下进一步检查。结果表明,SFD产生了更大的多孔颗粒,与SD相比,SFD中的雾化效果至少可提高50%,其产量大于95%。还得出结论,与液体对照制剂相比,喷雾冷冻干燥制剂的稳定性更好,特别是蛋白质/肽。使用SFD作为鼻内给药的替代方法制备流感疫苗,颗粒形态显示高度多孔的颗粒,空气动力学直径为5.3μm,有利于颗粒沉积在肺。此外,还观察到抗原的保留很高,从而提高了药物的免疫原性反应。


使用SFD技术配制的疫苗粉末可以更好地替代传统DDS。使用双流体喷嘴SFD技术制备了鲑鱼降钙素,用以治疗骨质疏松症和佩吉特病。颗粒的形态被发现是高度多孔的球形,表明它可以用于药物的肺部输送。此外,确定了喷雾冷冻干燥颗粒的体外沉积行为,颗粒表现出令人满意的细颗粒分数大于40%,且颗粒聚集度低,表明肺泡区域的颗粒沉积更好。卡那霉素作为吸入药物的SFD工艺,在10%卡那霉素浓度下,退火温度、时间、压力和喷嘴尖端提升的优化条件分别为−15°C、5小时、100kPa和1mm。使用该工艺获得了约3.58μm的空气动力学粒径,与原始卡那霉素相比,该药物显示出95.7%-98.4%的抗生素活性。颗粒的高孔隙率很明显(Fig.3)。
此外,使用SFD技术制备了布地奈德颗粒,吸入给药用于哮喘治疗的。最初,使用反溶剂方法在微流控反应器中制备颗粒,然后使用超声雾化探针对其进行喷雾冷冻干燥,然后表征颗粒的体外气溶胶特性。结果表明,使用SFD制备的粉末表现出良好的气溶胶性能,因此可以有效地用于通过肺部途径递送药物。使用SD和SFD使用海藻糖固定化胰蛋白酶,并进行了表征。配方结果表明,与SD相比,1:1的胰蛋白酶包衣海藻糖对酶活性具有更好的保护作用。因此,与生产吸入用粉末的其他工程方法相比,SFD是制备具有球形形态、高比表面积和低密度颗粒的最合适方法,便于肺部沉积。还观察到喷雾冷冻干燥的颗粒更容易到达肺部深处,具有独特的空气动力学特性,可以促进药物的全身循环。
2.1.3透皮给药
透皮递送使用皮肤作为连续给药及其全身循环的部位。通常,将药物贴片放置在皮肤上,以便将受控剂量的活性制剂释放到血流中。透皮给药克服了肝脏首过效应,从而提高了药物的生物利用度。此外,它允许通过一个狭窄的治疗窗口有效地使用具有较短生物半衰期的药物。通过透皮层递送药物已被广泛接受,因为它能够作用于目标部位而不会破坏皮肤。药物在透皮层内的渗透机制涉及通过表皮,也称为经表皮吸收。经表皮途径面临的主要阻力最初是在角质层,其厚度约为10-20μm。下一步涉及药物渗透通过有活力的表皮,最后药物渗透到真皮层内。由于药物在透皮层内扩散途径简单,避免了GIT内部涉及的复杂新陈代谢,不会产生任何副作用。由于患者间的差异很小,经皮DDS以预定的速率将药物输送到血流中。
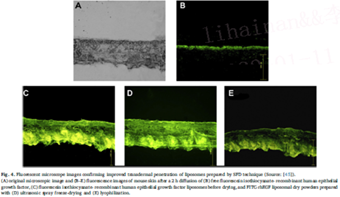
任何透皮给药系统的设计都取决于药物的渗透率,目的是药物可以很容易地到达目标部位。使用超声SFD技术和冻干法配制负载rhEGF的脂质体粉末。在制备rhEGF粉末时选择了脂质体,因为它们是药物的有利载体。结果表明,使用超声SFD技术生产的脂质体粉末产生多孔颗粒,其结构完整性没有明显变化。这是因为在SFD中避免了冰晶的形成,而在传统的冻干技术中,由于冷冻时间延长,观察到脂质体双层的破坏。体外释放研究也证实了这一结果,其中在通过冻干配制的脂质体的情况下观察到初始突释(即前1小时内50%);而使用SFD制备的脂质体在8小时内显示出持续的药物释放。因此,SFD的情况下与冻干相比,可以防止干燥过程中的药物泄漏。在透皮给药中,使用SFD技术制备的负载rhEGF的脂质体粉末显示出改善的结果,这已从荧光显微图像中得到证实(Fig.4)。由于SFD粒径范围比冻干制备的脂质体小,导致SFD配制的rhEGF脂质体的渗透性更高。与常规递送系统相比,SFD可用作改善药物治疗特性的有效技术。
由于机械稳定性差,鼻腔和肺部DDS对高孔低密度颗粒的要求并不适用于表皮应用。对于表皮应用,粒径、密度和速度至关重要。与FD相比,SFD可以生产具有不同粒度和密度的高流动性粉末(低密度颗粒用于鼻和肺输送,高密度颗粒用于经皮输送)。
3.未来研究的局限性和方向
尽管介绍了SFD的优点和独特功能,但该技术与任何其他技术一样,也有其自身的局限性。由于低压和低温要求,该技术在资本和运营成本方面都很昂贵。在扩大规模的背景下,大多数开发的SFD装置是批量型的,不适合完全商业用途。Meridion技术已将使用半连续SFD工艺制造单克隆抗体的工艺商业化。该粉末残留水分含量小于0.1%,并且易于流动。SFD粉末复溶性好,可以在2-4min内完全复溶,长期储存中无颗粒聚集现象。研究人员在中试规模中,使用SFD技术进行蛋白质的气溶胶递送。然而,设计能够满足不同产品范围的精确尺寸的喷雾冷冻和冷冻干燥室等仍然是一个挑战。使用液氮等冷冻剂还需要额外的防护措施,包括操作安全性和适当的设计,以尽量减少浪费。与传统的SD相比,SFD的处理成本高出30-50倍。
4.结论
综上所述,SFD在食品、医药方面具有多种应用。本综述侧重于SFD在药物输送中的应用,与其他干燥技术相比,稳定性和生物利用度均有所提高。SFD生产的多孔颗粒具有较大的表面积和良好的流动性,使其适合通过肺部途径输送药物。SFD生产的粉末具有优异的复溶性,使其适用于药物的药代动力学递送。然而,需要详细了解颗粒冷冻所涉及的动力学及其对颗粒结构的影响,因为它在药物输送中起着至关重要的作用。此外,了解喷雾冷冻干燥颗粒在人体内输送药物的机制也很重要。
<END>





















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论