瑞科生物董事会谨此宣布,为进一步提高公司综合竞争力,增加风险抵御能力,补充在研产品管线研发资金,促进业务平稳健康发展,于2024年11月11日,董事会会议上通过了本公司定向发行内资股的议案,拟依据特别授权向认购方扬子江药业集团有限公司(以下简称为“认购方”)发行不超过143,112,702股内资股。本公司于2024年11月11日与认购方签署了股份认购合同,据此,认购方有条件同意认购,且本公司有条件同意发行共143,112,702股内资股,认购价为每股人民币5.59元,预计本次发行的募集资金约为人民币800,000,004元。
本次发行将根据特别授权发行,董事会将根据相关条文向临时股东大会提呈上述事宜,以供审议通过。一份载有(其中包括)本次发行进一步详情及其他事宜的通函,连同临时股东大会的通告将适时刊发。
由于本次发行须待若干条件获达成后,方告完成,故本次发行可能会或不会进行。股东及潜在投资者于买卖本公司证券时务请审慎行事。
根据《中华人民共和国公司法》、《中华人民共和国证券法》、《非上市公众公司监督管理办法》、上市规则等相关法律法规、部门规章及规范性文件的规定,本公司拟定本次发行方案如下:
1.发行股票的种类和面值
本次定向发行内资股(以下简称“本次发行”)拟发行由境内投资者以人民币认购的内资股普通股,每股面值为人民币1.00元。
2.发行数量
本次发行的股份数量为不超过143,112,702股,分别约占本次发行前现有已发行内资股总数及已发行股份总数的92.44%及29.63%,分别约占本次发行后已发行内资股总数及已发行股份总数的48.03%及22.86%。实际发行数量以监管机构批复及发行对象最终认购数额为准。
3.发行对象
本次发行的发行对象为扬子江药业集团有限公司。该发行对象并非为本公司的关连人士,本公司现有股东无优先认购安排。
4.发行价格
本次发行的价格为人民币5.59元/股。
5.发行方式
本次发行以非公开发行的方式向选定的发行对象发行内资股普通股。
6.限售安排
本次发行的股份需遵守中国法律法规、上市地监管规则及公司章程关于股份转让的规定。
7.滚存未分配利润处置
本次发行完成前的滚存未分配利润由本次发行完成后的本公司全体股东按照各自实缴出资比例享有。
8.募集资金用途
预计本次发行的募集资金约为人民币800,000,004元,在扣除相关发行费用后,将用于带状疱疹疫苗产品的研发和补充营运资金。
9.发行方案有效期
本次发行方案的有效期为自公司股东大会审议通过之日起12个月。董事会可视乎实际情况提请股东大会审议并酌情批准延长本次发行方案的有效期。
关于扬子江药业
扬子江药业集团有限公司(以下简称“扬子江药业”)创建于1971年,是一家在中国注册成立的有限责任公司,其主要从事化学药、中药、大健康产品的研发、生产和销售的大型民营医药企业。扬子江药业是全国首批创新型企业,总部位于江苏省泰州市,现有员工18000余人,旗下子公司分布泰州、北京、上海、南京、广州、成都、苏州、常州等地。扬子江药业秉承“求索进取 护佑众生”的使命,践行“高质、惠民、创新、至善”的核心价值观,弘扬“为父母制药、为亲人制药”的质量文化,致力向社会提供优质高效的药品和健康服务。
关于瑞科生物
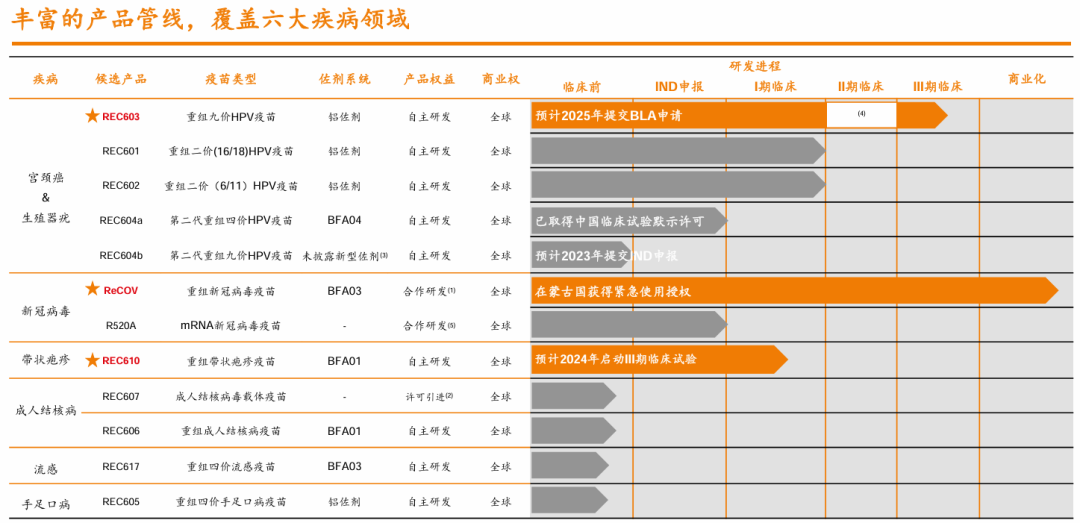
江苏瑞科生物技术股份有限公司(香港联交所股票代码:02179)始创于2012年,是一家以自主研发为核心驱动力的创新型疫苗公司。公司始终秉持“创制一流疫苗,守护人类健康”的使命,已构建新型佐剂、蛋白工程和免疫评价三大创新疫苗技术平台,是全球少数几家可自主研制及生产全系列疫苗新型佐剂的公司之一。目前,公司拥有10余款高价值创新疫苗管线组合,覆盖宫颈癌、带状疱疹、呼吸道合胞病毒等重大疾病领域。公司核心产品重组九价HPV疫苗REC603和新佐剂重组带状疱疹疫苗REC610处于中国III期临床研究阶段。
前瞻性说明
本新闻稿可能包含与本公司财务状况、经营业绩、资本状况、战略和业务有关的预测、估计、预测、目标、意见、前景、结果、回报和前瞻性陈述,这些可以由使用前瞻性术语,例如“可能”、“将”、“应该”、“预期”、“预期”、“项目”、“计划”、“估计”、“寻求”、“打算”、“目标” 、“相信”、“潜在”和“合理可能”或其否定词或其他变体或类似术语(统称为“前瞻性陈述”),包括战略重点、研发项目和任何财务、投资和资本目标以及本新闻稿内书面或口头描述的任何其他目标、承诺和抱负。任何此类前瞻性陈述都不是未来业绩的可靠指标,因为它们可能涉及重要的陈述或暗示假设和主观判断,这些假设和主观判断可能会或可能不会被证明是正确、准确或完整的。无法保证前瞻性陈述中列出的任何事项是可以实现的、将实际发生或将实现的或完整或准确的。这些假设和判断可能被证明是不正确、不准确或不完整的,并涉及已知及未知的风险、不确定性、或有事项和其他重要因素,其中许多不在本公司的控制范围内。亦无法保证本公司可以成功开发或销售其核心产品或其他候选产品。由于各种风险、不确定性和其他因素(包括但不限于一般市场状况、监管变化、地缘政治紧张局势或数据限制和变化)。任何此类前瞻性陈述均基于本公司在作出陈述之日的信念、期望和意见而作出,若情况或管理层的信念、期望或意见有所改变,本公司不承担并在此声明其不承担任何更新、修改或补充这些陈述的责任或义务。出于这些原因,阁下不应依赖任何前瞻性陈述并明确警惕阁下不应依赖任何前瞻性陈述。本公司或其代表不就本新闻稿所载任何预测、估计、预测、目标、承诺、前景或回报的实现或合理性作出任何明示或暗示的陈述或保证。
E.N.D

往期文章推荐:
总投资约30亿元,建筑面积10万平米,国内一细胞治疗药物研发与生产基地正式开工




































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论