1.1.1 总体概况
根据摩熵数据统计,2024.11.04-2024.11.10期间共有77个创新药/改良型新药临床申请/上市申请获国家药品监督管理局药品审评中心(CDE)承办(按受理号统计,不含补充申请)。其中,国产药品受理号60个,进口药品受理号17个。
本周共计17款创新药/改良型新药临床试验申请获得“默示许可”,包括化学药7款,生物药10款,无中药。其中值得注意的有:
(1)ZT-006片
11月5日,CDE官网公示:质肽生物的ZT-006片获得临床试验默示许可,用于成人2型糖尿病患者的血糖控制,以及成人超重或肥胖患者减重治疗。公开资料显示,ZT-006片是质肽生物自主研发的口服GLP-1类多肽药物,采用定点脂肪酸链修饰技术(QLLong)和大分子口服递送技术(QLOral)开发。
(2)LPM-682000012片
11月7日,CDE官网公示:绿叶制药的LPM-682000012片获得临床试验默示许可,用于治疗抑郁症。
(3)HYP-6589片
11月7日,CDE官网公示:汇宇制药的HYP-6589片获得临床试验默示许可,用于治疗晚期实体瘤。公开资料显示,HYP-6589片是一款高选择性SOS1小分子抑制剂,可特异性与SOS1的催化区域结合,阻止其与失活状态KRAS-GDP的相互作用并同时阻断SOS1驱动的反馈,减少KRAS-GTP 激活状态的形成,从而抑制下游的RAS-RAF-MAPK和RAS-PI3K-AKT-mTOR两条关键信号通路,发挥抗肿瘤作用。
本周共3款新药获批上市,即灌注用盐酸氨酮戊酸己酯、马来酸阿可替尼片和阿伐可泮胶囊。
11月5日,国家药监局发布药品批准证明文件送达信息:亚虹医药的灌注用盐酸氨酮戊酸己酯获批上市,用于膀胱癌(包括原位癌)患者的膀胱镜检查,包括既往的膀胱镜检查结果为疑似或已确诊的膀胱癌,或者随访期需要膀胱镜检查的患者。本品联合蓝光膀胱镜作为白光膀胱镜的辅助检查。
11月5日,国家药监局发布药品批准证明文件送达信息:阿斯利康(AstraZeneca)的马来酸阿可替尼片获批上市,用于既往至少接受过一种治疗的成人慢性淋巴细胞白血病(CLL)/小淋巴细胞淋巴瘤(SLL)患者。公开资料显示,马来酸阿可替尼片是新一代高选择性BTK抑制剂,通过与BTK共价结合抑制其活性。在B细胞中,BTK信号导致B细胞增殖、转运、趋化和粘附所需的途径激活。
11月5日,国家药监局发布药品批准证明文件送达信息:安进的阿伐可泮胶囊获批上市,用于治疗抗中性粒细胞胞浆抗体(ANCA)相关性血管炎。公开资料显示,阿伐可泮胶囊是一种口服小分子,补体C5a受体C5aR1的选择性抑制剂。通过阻断中性粒细胞表面补体过敏性毒素C5a受体(C5aR1)来选择性阻断其作用。
1.1.2 本周获批临床创新药/改良型新药信息速览(不含补充申请)
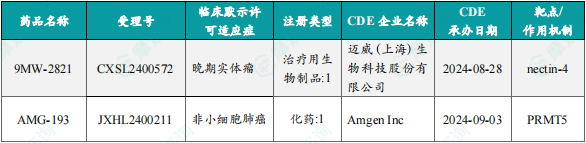
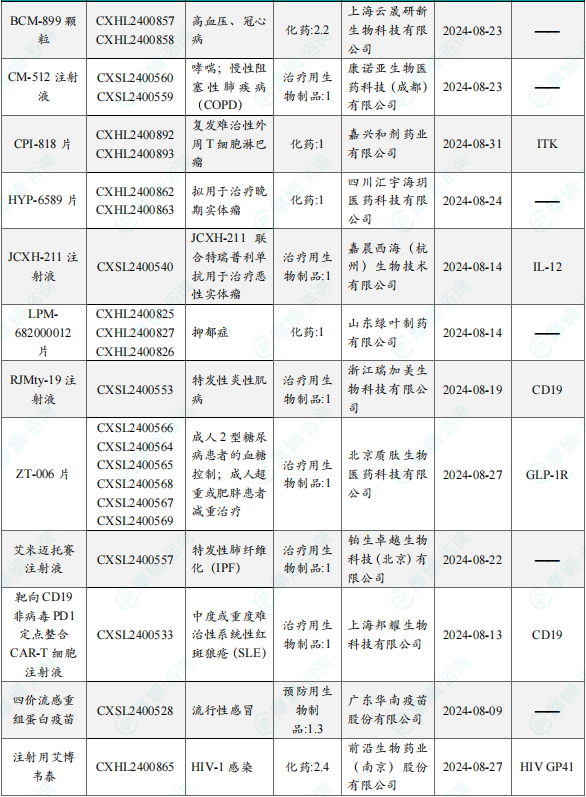
备注:(1)此处未包括补充申请之情形;(2)此处所列创新药/改良型新药,主要是指CDE受理批准的1类、2类、5.1类以及生物制品3.1类和3.2类。(3)更多获批临床信息及研发进展详情及相关靶点全局分析等,可通过摩熵中国药品审评数据库获取并下载EXCEL表格。
1.1.3 本周获批上市创新药信息速览
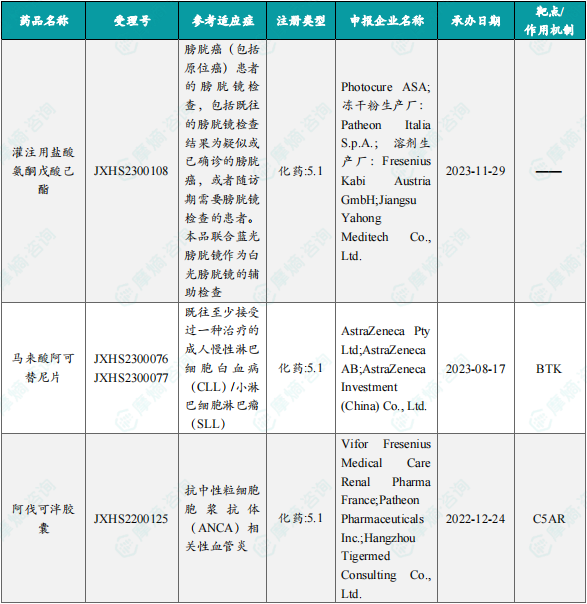
备注:(1)此处所列新药,主要是指国家药品监督管理局(NMPA)首次批准在中国上市的药品,包括新分子实体(以及包含有新分子实体的复方)、生物药、中药和疫苗。其中,新分子实体主要是化药注册分类下的1类(境内外均未上市的创新药)、5.1类(境外上市的原研药申请在国内上市);生物药主要为NMPA首次批准的国产及进口生物药;不包括生物类似物、新适应症、新剂型。(2)更多信息如获批临床品种相关靶点、研发企业、全球上市及研发进展及相关靶点全局分析等,可通过摩熵数据库获取并下载EXCEL表格。
同期事件:
1. 2024年第45周11.04-11.10国内仿制药/生物类似物申报/审批数据分析
2. 2024年第45周11.04-11.10国内医药大健康行业政策法规汇总
3. 2024年第45周11.04-11.10全球医药大健康行业投融资数据
4. 2024年第45周11.04-11.10全球创新药研发概览
以上内容均来自{摩熵咨询医药行业观察周报(2024.11.04-2024.11.10)},如需查看或下载完整版报告,可点击!
想要解锁更多药物研发信息吗?查询摩熵医药(原药融云)数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!













































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论