""相关的结果
-
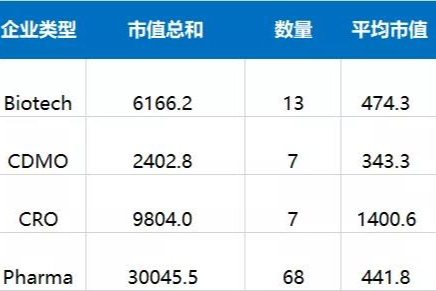
医药公司分四类,你奋斗在哪一类?
生物医药产业风起云涌,自进入21世纪以来,它已悄无声息地已经走过了三个阶段。自2001年“科创板医药第一股微芯生物扎根中国算起,虽然彼时仿制药风头正盛,却已表露“暮年之相”,创新改革的力量正在暗暗聚集。进入2010年,技术的瓶颈突破加之资本的热情涌入,一大批以Me-too,Me-better, fast-follow为特征进行研发布局的公司纷纷宣布将不落下对标国际大厂的每个风口,创新在技术储备和人才聚集的数量方面初具规模,本土企业海外授权的项目逐渐变多。 -

粉体学性质的研究及对制剂工艺的影响
粉体即无数个固体粒子所组成的集合体,而粉体学顾名思义就是研究粉体基本性质的一门科学。我们日常科研工作中频繁提及的“粒”、“粉”等均属于粉体,两者的区别主要在于粒径差异,粒径<100μm称之为“粉”,由于粒径较小,粒子之间容易产生相互作用,故流动性较差;粒径>100μm称之为“粒”,跟“粉”相反,由于粒子自重大于其粒子间产生的相互作用,流动性较好。药物的粉体学性质主要包含有:粒子的形状及大小、粒径分布、密度、流动性、润湿性或吸湿性等,由于我们在日常的制剂研发工作中经常需要对API或辅料进行粉碎、混合、过筛等处理,有时候原料粉体学性质较差,还会选择一些粉体学性质优良的辅料来改善主药的粉体学性质等,这么处理操作的目的其实主要就是想通过改善粉体性质使之可以满足后续制剂加工的操作要求,所以粉体学性质的研究在固体制剂的开发应用中占据非常重要的地位,如果原料或颗粒的粉体学性质较差,例如其流动性较差,可能会影响片剂的压片或散剂的分装剂量;亦或者药物的孔隙率、或孔隙形状等会影响片剂的崩解、溶出乃至对吸收产生一定的影响,所以接下来就想和大家一起分享一下在制剂研究工作中主要研究哪些粉体学性质以及其对制剂工艺 -
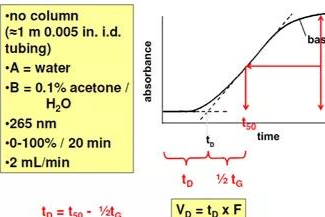
分析方法转移的仪器系统考量与探讨
分析方法转移是制药行业中常见的技术转移,常见的情形有在分析研发实验室间的转移;研发实验室与QC实验室间的转移;样品生产地点变更时,QC实验室间的转移。药物研发早期,对分析方法转移的法规要求不高;在研发后期或者商业化阶段,方法在QC实验室之间的转移,对定性与定量结果的一致性有较高要求。任何结果的偏离要非常小心,否则易产生超限或超趋(OOX)的结果。方法转移前,如果方法验证与耐用性的研究比较充分,对方法的认知比较了解,方法转移时出现检验结果偏移时会能有足够的信息与手段来应对与解决。 -
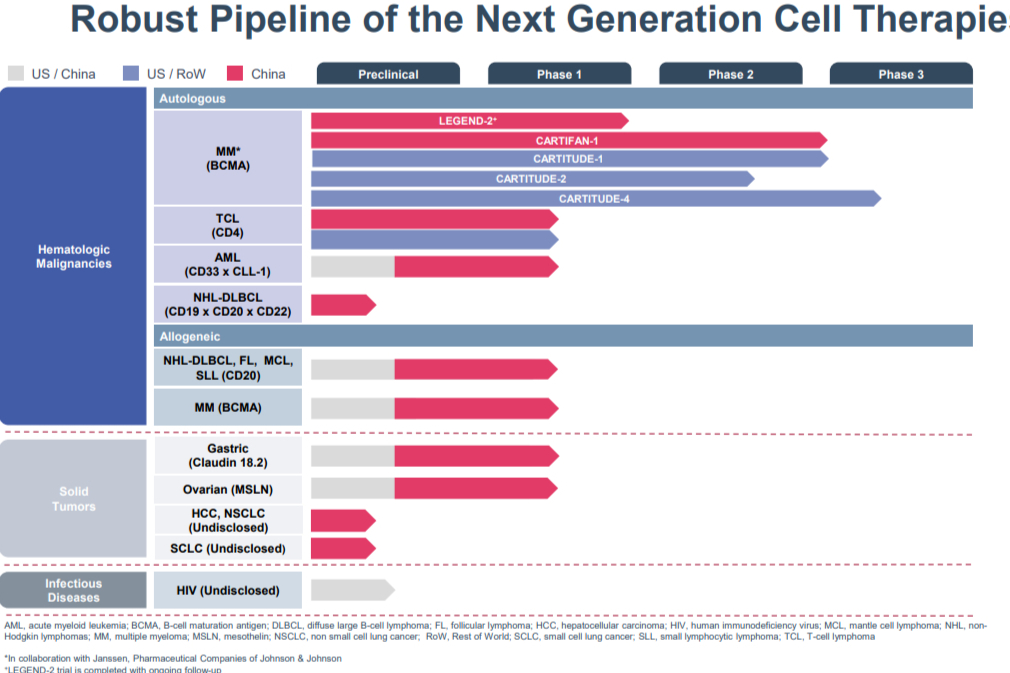
最新全球CAR-T细胞疗法研发格局
国内CAR-T公司走过了主题投资和技术验证2个阶段,已经进入产品兑现阶段。近日,复星凯特的CAR-T产品阿基伦塞注射液在国内获批上市,是国内首个上市的CAR-T细胞疗法。药明巨诺的CAR-T产品去年已申报上市,等待获批;北恒生物通用型CAR-T产品CTD401获得美国FDA孤儿药资格认定,国产CAR-T产品的实力得到进一步验证。 -
新锐|开发12-脂肪氧化酶抑制剂|完成1660万美元A轮融资
近日,Veralox Therapeutics 是一家生物技术公司,开发一流的小分子疗法,治疗具有显着未满足医疗需求的疾病的潜在病理,宣布完成 1660 万美元的 A 轮融资。该轮融资由 Hatteras Venture Partners 领投,Genesys Capital、Point Field Partners 和 Alexandria Venture Investments 参与,并得到了之前投资者的支持,包括Sanofi Ventures、JDRF T1D Fund, Maryland Momentum Fund, VTC Innovation Fund 和TEDCO。2019年,该公司完成了540万美元种子轮融资。 -

药品连续制造工艺的的确认与验证活动
确认和验证是一组相近的概念,确认(Qualifications)是证明厂房、设施和设备能够正确运行并且达到预期效果的一系列活动及其书面记录;验证(Validation)是证明任何操作规程或方法、生产工艺或系统能够达到预期效果的一系列活动及其书面记录。因此二者的内涵是基本一致的,只是确认侧重于硬件,验证侧重于软件。但需要注意的是,在验证活动中,也包含一种针对于软件的“确认(Verification)”,它强调的是某个规程或方法的符合性证明,与验证(Validation)在含义上有些微妙的区别。药品生产活动涉及到的主要确认与验证活动包括:厂房确认(Qualification of Facilities)、设施确认(Qualification of Utilities)、设备确认(Qualification of Equipment)、工艺验证(Process Validation)、包装验证(Validation of Packaging)、运输确认(Verification of Transportation)、分析方法验证(Validation of Test Methods)、分析方药品制造702413年前 -
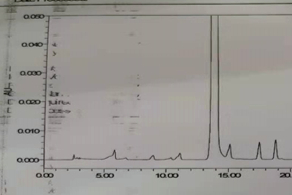
液相方法优化经典案例
液相分析方法是质量标准的重要组成部分,常用来检测活性成分、有机杂质、无机杂质、残留溶剂等,以检测药物是否符合其质量标准,确保其安全有效。在物料的日常检测(有关物质)中,通常会采用供应商提供的方法,但这些方法一般情况下仅满足样品检测需要,但是否满足系统适用性要求,需要进一步研究,具体例子如下 -
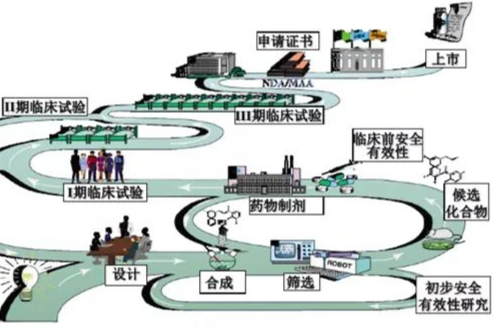
2021创新药药学研究知识点大全
2021创新药药学研究知识点大全,一个创新药的研究开发需要经历:疾病市场调研、分子机理研究、靶标的选择确认、分子设计、先导化合物合成及优化、药效药代和毒性初筛、临床前研究、临床研究、新药审评及上市等环节,从新药立项到最终上市,需要经历大约8-10年时间周期,所谓:“十年磨一剑”。新药药学研究经历了一个从发现到认知再到确认的过程,在这个过程中,安全性和有效性始终是筛选或淘汰候选药物的”金标准”,药学研究任务的顺利开展是支持后期临床前研究和临床研究的重要前提,是保证拟上市药物质量可控性的关键所在。 -

仿制药BE结果是否确为临床等效的金标准?
我国是仿制药大国,目前为止,绝大多数药企仍为仿制药企业。仿制药是用于对原研药进行功能替代,并体现价格优势的替代品,其使命之一,是与原研药的疗效一致。倘若仿制药出现了异于原研药的疗效特征,有两种表现:无效(低效),或者不良反应。这两种问题的根源在哪里,BE试验的结果对于判断仿制药与原研药的等效,是否有绝对价值?笔者在此进行浅要论述。 -
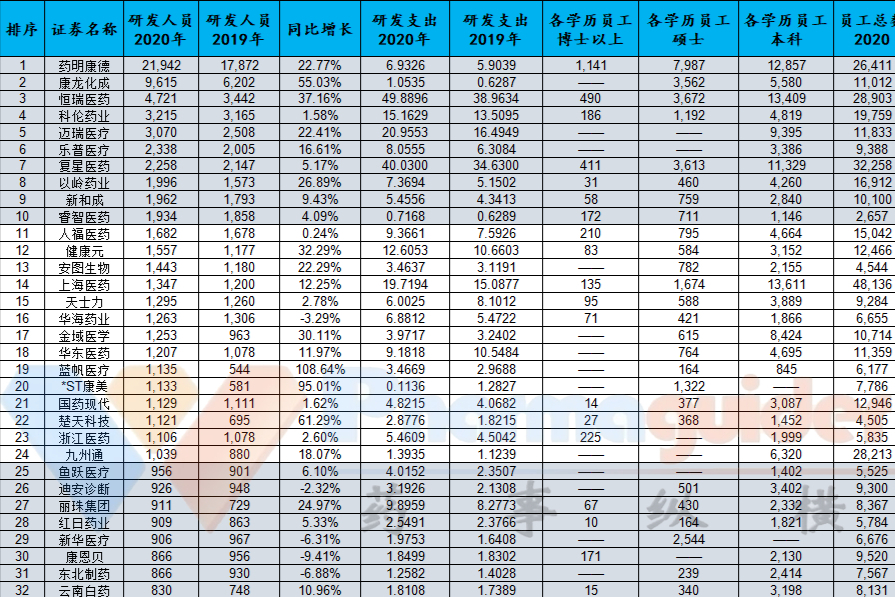
2021上市药企研发人员数量排行Top50:第一名2万多人
研发人才对药企至关重要,尤其是在创新的大浪潮下。 据申万行业分类,我们选取A股上市的所有医药生物公司(港股未披露相关数据),按照2020年报披露,研发人员数量Top50排序如下:













