
2023年10月9日,美国罗克维尔和中国苏州——信达生物制药集团(香港联交所股票代码:01801),一家致力于研发、生产和销售肿瘤、自免、代谢、眼科等重大疾病领域创新药物的生物制药公司,宣布其研发的重组人血管内皮生长因子受体(VEGFR)-抗体-人补体受体1 (CR1) 融合蛋白efdamrofusp alfa注射液(研发代号:IBI302)的III期临床研究STAR完成首例受试者给药。
IBI302基本信息
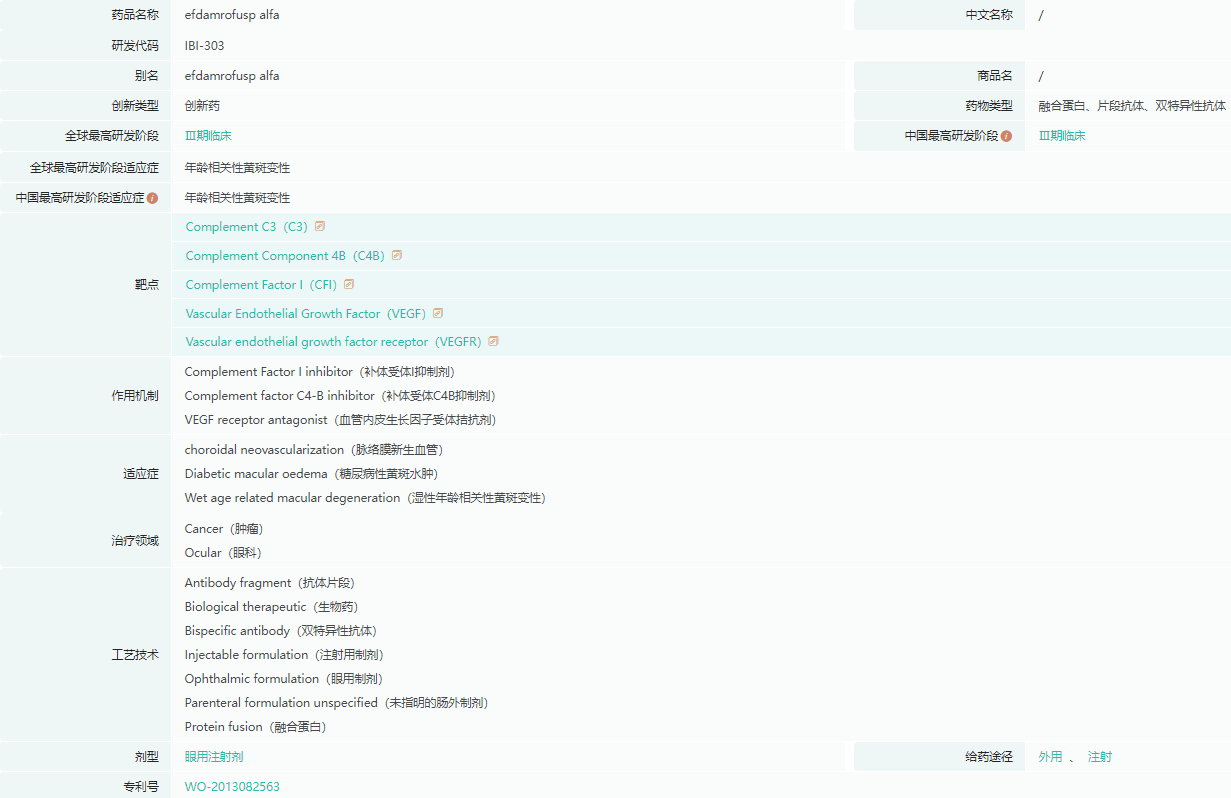
截图来源:药融云全球药物研发数据库
STAR是一项在新生血管性年龄相关性黄斑变性(nAMD)受试者中进行的随机、双盲、活性对照的III期临床研究(CTR20232229, NCT05972473),旨在评估玻璃体腔注射8mg IBI302的疗效和安全性,以支持IBI302的上市注册申报。本试验计划入组600例受试者,并按1:1比例随机分配至8mg IBI302组和2mg 阿柏西普组:所有受试者的访视均为每4周一次(Q4W),分配至IBI302组的受试者将接受8mg IBI302玻璃体腔注射(Q4W)至第8周,继之以个性化间隔给药(PTI)8mg IBI302 玻璃体腔注射;随机分配至阿柏西普活性对照组的受试者将接受2mg阿柏西普玻璃体腔注射(Q4W)至第8周,继之以2mg 阿柏西普玻璃体腔注射(Q8W)。该试验的主要研究终点为第44、48和52周时研究眼最佳矫正视力(BCVA)均值较基线的改变。所有受试者将持续接受玻璃体腔注射至第96周,并在第100周进行最终研究访视。

IBI302作为全球首个靶向VEGF和补体的双特异性融合蛋白,可以同时抑制VEGF介导的信号通路和减轻补体活化介导的炎症反应。已开展的两项II期临床研究的结果显示了IBI302在nAMD患者中良好的安全性和有效性以及长间隔给药优势:疗效方面,可以提高最佳矫正视力、改善视网膜厚度和新生血管的渗漏与总面积,并观察到对黄斑萎缩及纤维化的潜在改善作用;安全性总体特征良好,与现有抗VEGF单靶点药物类似。
该临床研究的主要研究者,上海市第一人民医院副院长、眼科中心主任孙晓东教授表示:“目前nAMD一线治疗药物是抗VEGF药物。但其治疗过程存在频繁注射、长期疗效衰减、部分患者疗效欠佳等问题,给广大患者带来诸多不便和经济负担,故目前在nAMD治疗方面仍存在巨大的未满足的临床需求。IBI302作为全球创新的抗VEGF-抗补体双靶点药物,在已经完成的临床I、II期研究中已经展现了显著的疗效,包括视力提高及视网膜水肿改善,并具备良好的安全性,我们还看到了初步的改善纤维化和黄斑萎缩积极信号,这给研究者带来了很大的信心。期待8 mg IBI302在III期临床研究STAR中不但能突破当前治疗瓶颈,显著延长给药间隔,减轻患者注射负担,还能展现出其潜在的长期给药后抗纤维化以及黄斑萎缩改善方面更多优势,为患者带来更加友好的给药方案以及更长久持续的视力获益。”
信达生物制药集团临床开发副总裁钱镭博士表示:“IBI302是信达生物拥有全球自主知识产权的用于治疗眼底病的创新药物,属全球首创抗VEGF-抗补体双靶点分子,已作为1类新药获得国家科技部重大新药创制专项课题的支持。前期的临床研究结果初步验证了IBI302良好的安全性和耐受性,以及改善视力的疗效,为我们开展下一阶段的研发带来了较大信心。在接下来的III期研究中,我们除了关注视力和视网膜水肿改善外,还将探索8 mg IBI302在长间隔给药上的疗效与抗纤维化与改善黄斑变性的潜力。我们期待在IBI302在III期临床研究STAR中取得成功,争取早日为患者提供更有价值的创新临床治疗方案。”
参考资料:
1.公司官网
2.药融云数据库
<END>
要解锁更多企业药品研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药品各国上市情况、药品批文信息、销售情况与各维度分析、市场竞争格局、一致性评价情况、集采中标情况、药企申报审批信息、最新动态与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!








































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论