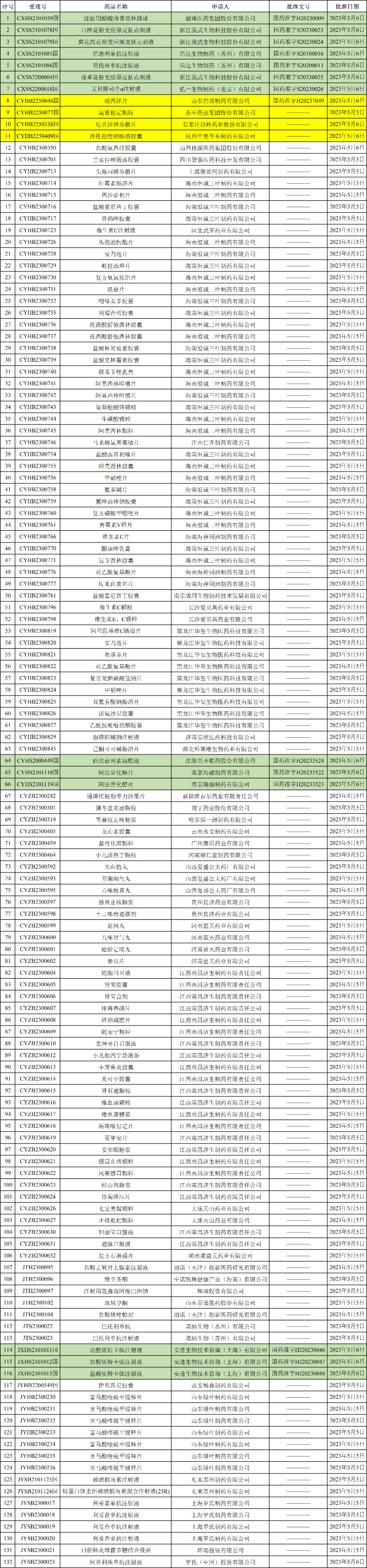
NMPA发布2023年05月09日药品批准证明文件送达信息,本批次共有132个受理号获批,其中有4个品种通过一致性评价,为:
- 山东信谊制药有限公司,地西泮片(首家过评)
- 苏中药业集团股份有限公司,氯雷他定颗粒
- 石家庄以岭药业股份有限公司,厄贝沙坦分散片(国内第二家过评)
- 杭州中美华东制药有限公司,泮托拉唑钠肠溶胶囊(国内第二家过评)
此外,信达生物的创新药物PD-1抑制剂信迪利单抗注射液(商品名:达伯舒®)新适应症获批,联合贝伐珠单抗、培美曲塞和顺铂,用于经表皮生长因子受体酪氨酸激酶抑制剂(EGFR-TKI)治疗失败的EGFR基因突变阳性的局部晚期或转移性非鳞状非小细胞肺癌(NSCLC)患者的治疗。截至目前,达伯舒®(信迪利单抗注射液)已获批七项适应症。
同时,信达生物的贝伐珠单抗注射液(商品名:达攸同®)也同时获批了第八项适应症。此次新适应症的获批主要基于一项随机、双盲、多中心、前瞻性Ⅲ期临床研究(ORIENT-31,NCT03802240)——信迪利单抗±贝伐珠单抗联合培美曲塞和顺铂,治疗经表皮生长因子受体酪氨酸激酶抑制剂(EGFR-TKI)治疗失败的EGFR突变的局部晚期或转移性非鳞非小细胞肺癌的分析结果。
<END>








































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论