
2022年12月20日,马萨诸塞州剑桥,Magenta Therapeutics(NASDAQ:MGTA)是一家临床阶段生物技术公司,该公司开发新型药物,旨在将干细胞移植的疗效带给更多患者。今天宣布,公司已向FDA通报了其ADC药物MGTA-117在I/II期研究中最高剂量组的两种剂量限制性毒性,在该队列中将不再有患者接受给药。
受到此消息影响,Magenta Therapeutics股价周二晚上大跌超过50%,目前市值仅为0.5亿美元。在今年春季公司还宣布了将裁员14%,并停止了MGTA-145管线研发。
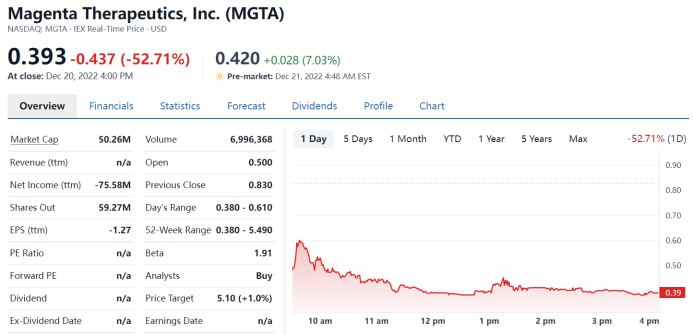
具体情况如下:
Magenta Therapeutics周二表示,根据针对复发/难治性急性髓性白血病(AML)和骨髓增生异常综合征(MDS)的ADC药物——MGTA-117,1/2期剂量递增临床试验的临床试验方案,它已停止对参与者进行给药队列4剂量水平(0.13 mg/kg),并计划以队列3剂量水平(0.08 mg/kg)对其他参与者进行给药。

Jason Gardner, Magenta Therapeutics CEO
队列4中有3例参与者接受了给药,在第二和第三次给药的参与者中观察到剂量限制性毒性(dlt)。第一名参与者完成了21天DLT观察期,无DLT发生。在该公司于2022年12月13日向投资者介绍情况之后,该公司收到报告称,队列4中的第二例参与者发生了被认为可能与MGTA-117相关的4级严重不良事件(SAE)(呼吸系统)。该SAE后来被确定为DLT和因肺部受累导致的疑似意外严重不良反应(SUSAR)。该参与者还出现了4级天冬氨酸转氨酶(AST)和3级丙氨酸转氨酶(ALT)升高,但胆红素、γ -谷氨酰转移酶或碱性磷酸酶无临床显著变化。2022年12月15日,本公司收到了第三例受药参与者的呼吸系统SAE报告。这一SAE随后被确定为队列4中的第二例DLT,从而触发了队列4中进一步给药的预设停药规则。截至本新闻稿发布之日,各临床试验中心报告,接受DLT的第一名参与者的呼吸状态和AST/ALT酶水平改善,接受DLT的第二名参与者的呼吸状态改善。

Magenta今天向FDA报告了临床数据和适用于第一个观察到的DLT的其他信息。Magenta还告知FDA,适用于第二个参与者的DLT事件的信息即将发布。
根据临床试验方案,并遵循本试验安全性队列审查委员会(Cohort Review Committee)在2022年12月19日提出的建议,Magenta计划继续以队列3剂量水平纳入患者。如2022年12月12日在2022年美国血液学会(American Society of Hematology)年会上发布的报告,在本临床试验前3个队列的15名参与者中,未观察到dlt。在基线和给药后采集配对骨髓样本的队列3中,4名参与者中有3名血液和骨髓中的癌症母细胞均被清除。公司仍然认为队列3剂量水平的获益/风险特征是可以接受的,以便继续招募参与者参与本试验。
关于MGTA-117
MGTA-117是Magenta最先进的靶向调节产品候选产品,旨在在患者接受干细胞移植或接受离体基因治疗产品之前,耗尽血液和/或骨髓中表达CD117的靶细胞。MGTA-117是CD117抗体与鹅膏素(amanitin)ADC药物(偶联药物)。CD117,也称为c-Kit受体,在造血干细胞、祖细胞和成癌细胞上高度表达。据药融云数据库显示,现其针对骨髓增生异常综合征、急性骨髓性白血病的临床试验均已在今年一月进入了2期阶段。
MGTA-117适应症研发状态
截图来源:药融云全球药物研发数据库
关于Magenta Therapeutics
Magenta Therapeutics是一家临床阶段的生物技术公司,开发的药物旨在将干细胞移植的治疗能力带给更多的血液癌症、遗传疾病和自身免疫性疾病患者。Magenta将干细胞生物学和生物治疗学发展的领导地位与临床和监管专业知识相结合,彻底改变血液和免疫重置,使更多的患者能够利用干细胞移植的治愈潜力,并可能提高未来基因治疗的资格。
参考资料:
[1] https://investor.magentatx.com/news-releases/news-release-details/magenta-therapeutics-provides-update-mgta-117-phase-12-dose
[2] 药融云数据库vip.pharnexcloud.com/?zmt-mhwz
<END>







































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论