
2025年1月20日,康诺亚和诺诚健华联合宣布,两家公司及其双方的合资公司共同与Prolium Bioscience(以下简称Prolium)达成许可合作,授权Prolium开发和商业化CD20×CD3双特异性抗体CM355(ICP-B02)。
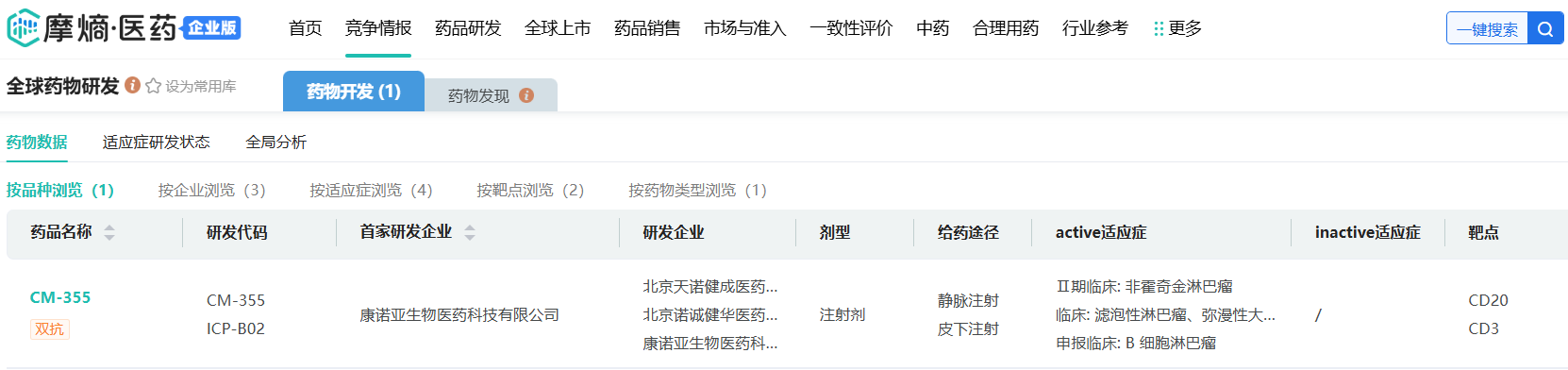

截图来源:摩熵医药数据库
CM355(ICP-B02)是康诺亚和诺诚健华联合开发的双特异性抗体。目前正在中国开展 I/II 期临床试验,旨在评估CM355(ICP-B02)在复发/难治性非霍奇金淋巴瘤(NHL)患者中的安全性、耐受性、药代动力学(PK)以及抗肿瘤活性。
研究显示,CM355(ICP-B02)的静脉输注(IV)制剂和皮下注射(SC)制剂在滤泡性淋巴瘤(FL)和弥漫性大B细胞淋巴瘤(DLBCL)患者中展示了初步的良好疗效。基于优异的研究数据,公司计划针对前线NHL 患者开展一项与其他免疫化疗联用的剂量扩展研究,该联合治疗的IND申请已获批准。
根据协议条款,Prolium将获得在全球非肿瘤领域以及亚洲以外肿瘤领域开发、注册、生产和商业化CM355(ICP-B02)的权利。康诺亚和诺诚健华将获得最高5.2亿美元(约37.8亿元)的总付款,包括首付款和近期付款,以及其他达成临床开发、注册和商业化里程碑的额外付款,并且双方将获得Prolium的少数股权。同时,康诺亚和诺诚健华还将获得未来产品净销售额的分层特许权使用费。
Prolium是一家总部位于美国特拉华州的公司,由RTW投资公司注资成立。RTW是一家总部位于纽约的全球性全生命周期投资公司,专注于在生物制药和医疗技术领域挖掘革命性和颠覆性创新。
总结
目前,全球范围内针对CD20xCD3双抗的研发竞争日益激烈,多家国际知名药企,如罗氏、艾伯维和再生元等,都在积极布局这一领域。
国内而言,中国生物制药下属企业正大天晴1类创新药CD3×CD20双特异性抗体TQB2825已获批临床;爱思迈生物研发的EX103用于治疗复发或难治CD20阳性非霍奇金淋巴瘤,I/II 期研究中显示具有良好的安全性,严重CRS发生率低且无ICANS;天广实生物也自主研发了一款CD3/CD20的T细胞重定向双特异性抗体MBS303;早在去年8月,嘉和生物CD3/CD20双抗以近5亿美元的价格通过NewCo模式出海。这一重大突破不仅彰显了中国生物医药企业在全球市场中的竞争力,也标志着CD3和CD20靶点治疗领域的又一次重大进展。
参考来源:
[1] 企业官方公告
[2] 摩熵医药(原药融云)数据库
想要解锁更多药品信息吗?查询摩熵医药(原药融云)数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药品各国上市情况、药品批文信息、销售情况与各维度分析、市场竞争格局、一致性评价情况、集采中标情况、药企申报审批信息、最新动态与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!


















































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论