TCE双抗出海在近期迎来“爆红”,被MNC买家们重点青睐和押注的方向,不是过去研发者们重点突破的肿瘤方向,而是在自免领域。
今年8月以来,国内Biotech分别完成了有关于四项与自免方向有关的TCE双抗BD交易,包括嘉和生物(CD3/CD20双抗)、岸迈生物(BCMA/CD3双抗)的Newco交易,还有就是同润生物和默沙东达成CD3/CD19双抗的巨额交易,以及GSK收购恩沐生物的CD3/CD19/CD20三抗CMG1A46的最新合作。其中诞生了在国内Biotech出海史上两项价值巨大的交易,同润生物和默沙东的合作首付款为7亿美金,仅次于BMS与百利天恒关于双抗ADC的合作;而GSK与恩沐生物的交易首付款为3亿美元,在过去国内众多BD交易中可算是第一梯队的水准。
在“美元攻势”指明MNC喜好之下,我想下一个国产创新药赔率最高的出海机会呼之欲出。
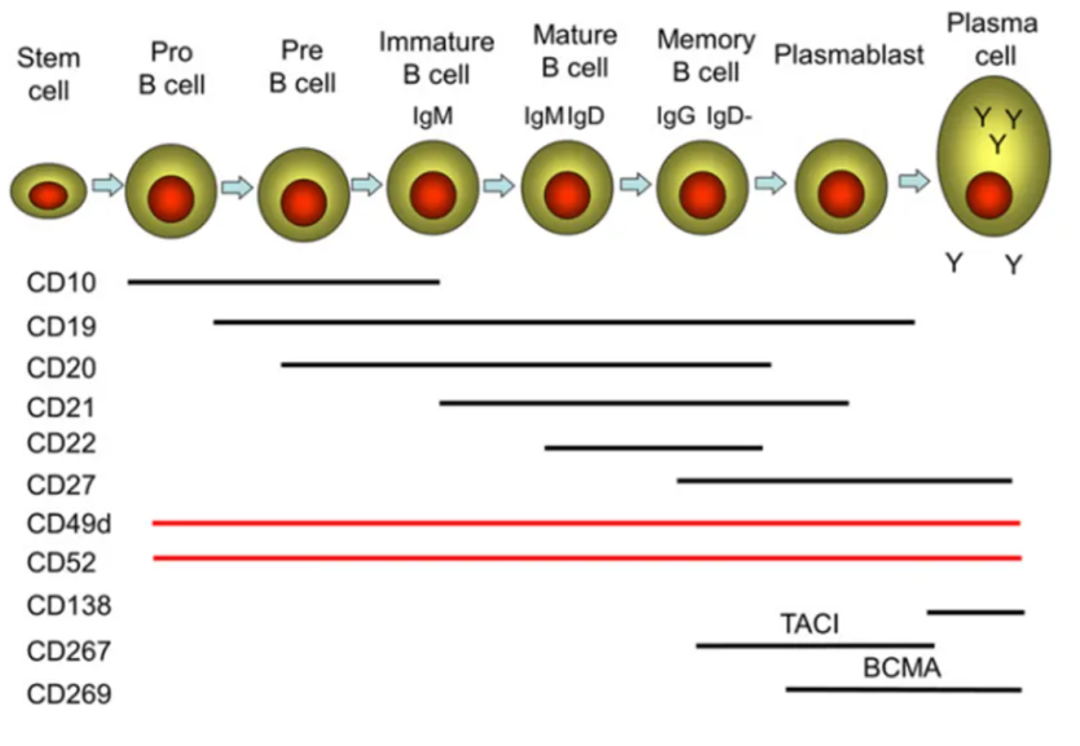
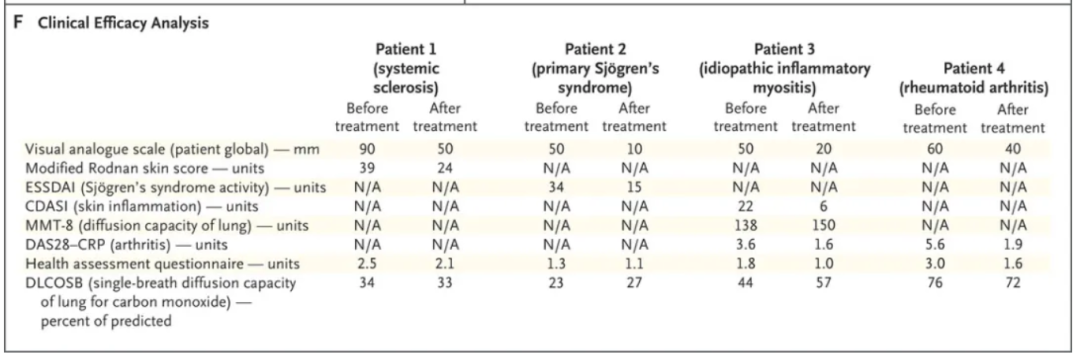
自免疾病可分为两种类型,一种是T细胞介导的免疫反应,其特征是免疫反应过度并攻击自身组织;另一种是B细胞介导的免疫反应,B细胞会产生自身抗体来介导免疫反应。而B细胞介导的自免疾病,最典型的是弥漫性结缔组织病(包括类风湿关节炎、干燥综合征等),其次也有分散在不同学科的适应症(重症肌无力、多发性硬化、天疱疮和溶血性贫血等)。基于这类自免疾病发病基础是产生自身抗体的自身反应性B细胞,B细胞耗竭疗法(BCDT)应运而生,其通过一定手段来清除B细胞从而减弱自身免疫来达到治疗目的,已经在单抗、CAR-T分子层面展现出了巨大潜力。在BCDT策略上,如何选择B细胞清除药物靶标就显得比较关键。B细胞在骨髓中发育,成熟后进入外周血,其依次明确的表面抗原和DNA重排情况可分为:祖B细胞、前B细胞、未成熟B细胞、过渡B细胞、初始B细胞、记忆细胞、原浆细胞和浆细胞等。其中,B细胞表面抗原包括CD19、CD20、CD38、CD138等,值得注意的是由于CD19在B细胞全生命周期表达、CD20在祖B细胞和浆细胞不表达,这两大靶点成为热门的研究目标。从理论上来看,对比针对B细胞清除药物靶标的单抗来说,TCE双抗一端定位各种B细胞,另外一端连接T细胞的CD3表位,有望更深度、更持久的清除B细胞,达到持续治疗B细胞介导的自免疾病。目前,已经有成熟药物在早期临床中初步验证了CD3双抗对于自免疾病的疗效。2024年4月Georg Schett在《Nature Medicine》期刊发表的论文显示,在6名严重多重耐药的类风湿性关节炎患者(RA)研究中,使用了非常低剂量的安进CD19/CD3双抗Blinatumomab对患者进行治疗,结果显示:Blinatumomab的治疗成功使得患者B细胞耗竭且伴随T细胞数量减少,患者临床疾病活动迅速下降且滑膜病变得到改善(B细胞和浆细胞大量存在于发炎的滑膜),并降低了自身抗体水平(自身抗体与RA患者严重疾病进展有关);研究中安全性良好,未出现CRS(细胞因子风暴)。除了Blinatumomab之外,2024年9月新英格兰医学杂志(NEJM)刊登了两篇强生Teclistamab(CD3/BCMA双抗)治疗自身免疫疾病的文章,其中一项研究展示了Blinatumomab治疗使得一名拥有6年病史、多款药物经治未出现显著缓解的系统性红斑狼疮(SLE)患者实现了完全缓解;另一项研究,Teclistamab对4位5种以上免疫抑制剂耐药的自免患者进行治疗,包括系统性硬化症、原发性干燥综合征、特发性炎性肌病以及RA患者,所有患者均取得积极疗效。TCE双抗在自免疾病展现出的潜力,对于近年因自免疾病再次热门起来的CAR-T和细胞治疗遭受较大竞争压力(目前美国已提交了35项SLE细胞疗法的IND,中国正在开发用于治疗自免疾病的CAR-T产品管线已有几十款)。
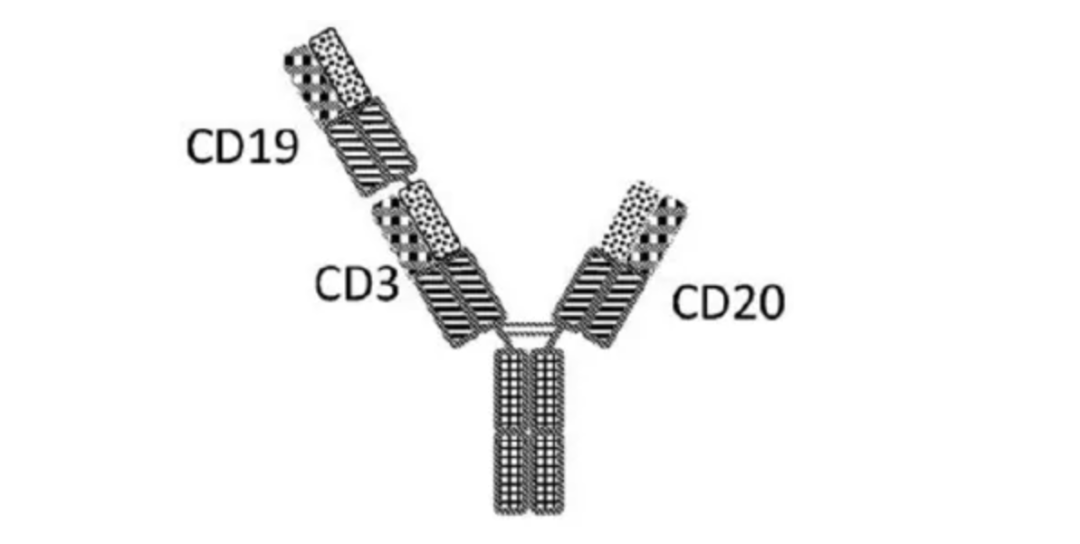
相比CAR-T疗法患者治疗前需清淋、等待制造过程并进行回输后观察,TCE双抗作为非个性化的通用药物,且可以制作成皮下注射剂型,患者依从性更佳。恩沐生物一个自免适应症都还没进入临床的三抗CMG1A46,为什么值得3亿美元的首付款?答案可能是基于CMG1A46定位于更新一代的TCE多抗,对于现有的TCE双抗有着潜在“降维打击”的能力,这从其在几年前在ASH大会上公布的临床前数据就可见一斑。
据医药观澜报道的数据显示,CMG1A46针对非霍奇金淋巴瘤(DLBCL)临床前数据具备几个显著的特征:1)高亲和力:CMG1A46与肿瘤细胞表面的CD19和CD20具有很高的亲和力(即便是CD20痕量表达的DLBCL),同理这意味着其对CD19、CD20表达的B细胞可能存在很强的耗竭能力;
2)疗效&安全性初探:相对传统的CD3/CD20,CMG1A46在临床前数据展出更强的肿瘤抑制活性;更值得注意的是,CMG1A46的剂量是传统CD3/CD20双抗的6倍,安全性风险却未有明显增加;3)半衰期:据报道,高亲和力的CD3双抗往往会导致较短的血清半衰期,而CMG1A46在食蟹猴的药代动力学研究表明,1mpk给药时CMG1A46在血清中的半衰期超过70小时。
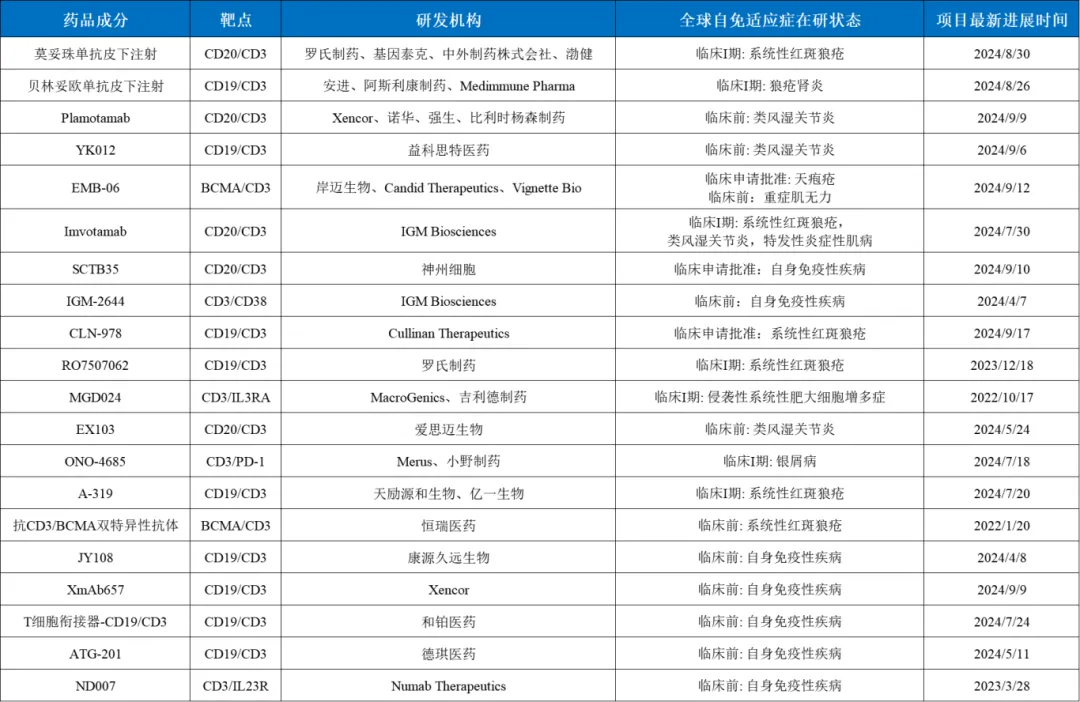
另外,获得默沙东青睐、以7亿美元首付款授出全球权益的同润生物CD3/CD19双抗CN201同样值得关注。CN201的发现基于药明生物的WuXibody双抗平台,据介绍,该平台特点在于几乎可利用所有抗体序列构建双抗,同时可灵活构建各种不同的价数的双抗,并可降低管线的免疫原性风险和延长在人体内半衰期。更值得注意的是,CN201在ASCO大会公布急性B淋巴细胞白血病一期临床数据显示:51位患者中有7位接受高剂量治疗,其中有6位完全应答(CR);安全性方面,所有患者中只有2位患者出现3级CRS,并未出现4级CRS事件。据上述早期中型样本量临床看,相信默沙东花大价钱收购CN201很大程度基于其疗效和安全性的平衡,在具备强大的B细胞耗竭能力的同时保证长期治疗的安全性,这在大部分自免疾病中非常重要。目前,全球范围内有超过20款TCE双抗开展了自免领域适应症探索,靶点选择集中在CD3/CD19、CD3/CD20、CD3/BCMA,大部分处于临床一期及临床前的阶段。海外研发进度靠前、以自免TCE多抗为核心管线的Biotech包括Cullinan Therapeutics、IGM Biosciences、Xencor等。IGM Biosciences以构建多个CD3双抗的IgM平台而崭露头角,2年前与赛诺菲达成3个肿瘤学靶点和3个免疫学靶点的管线合作,后调整方向专注在自免领域。目前,公司进度最快的管线是CD20/CD3双抗Imvotamab,在SLE、RA等适应症上开展一期临床。尽管Imvotamab自免适应症临床数据尚未读出,但早期基于近100名非霍奇金淋巴瘤(NHL)患者的数据,imvotamab展现出良好的安全性(所有剂量组CRS发生率为15%),并在结合和杀死低CD20表达细胞方面显示出优越的效力。Cullinan Therapeutics同样是海外市场备受关注的Biotech,其CD19/CD3双抗CLN-978早前刚刚进入临床阶段,成为首个FDA批准自免适应症IND的CD19 T细胞衔接器。CLN-978的设计具备一定的特点,其经工程改造可实现与CD19的极高亲和力结合(即便是CD19表达量极低的B细胞),另外其还含有一个与人血清白蛋白结合的单结构域抗体,以延长血清半衰期。在CLN-978过去已有的一期DLBCL临床中,3名患者每周接受30mg皮下注射,在首次给药后96小时内2名具有可检测基线B细胞的患者外周B细胞分别减少了93%和98%,而两名肿瘤体积较大的患者在首次给药后出现了一级CRS事件。不难看出,CLN-978具备强劲的B细胞耗竭潜力,同时安全性未来需要在SLE临床中进一步观察。神州细胞的SCTB35已经进入临床阶段,其为国内首款皮下注射CD20/CD3双抗,首个推进适应症为DLBCL,在今年9月国内获批了B细胞介导的自身免疫性疾病临床。其余国产TCE双抗均处于较早阶段,包括恒瑞医药、德琪医药、和铂医药、亿帆医药等均有布局。
结语:以长效自免单抗为核心管线的Biotech在海外的估值正在水涨船高,而TCE双抗作为能够更深度、更持续清除B细胞的新一代疗法,在未来的自免治疗格局上显然有机会占有一席之地,而最终决定性的因素,便是看哪家MNC或者Biotech能够做出一个类达必妥的安全性、有效性兼顾的出色产品。
本文系转载,仅做分享之用,不代表平台观点。图片、文章、字体等版权均属于原作者所有,如有侵权请告知,我们会及时处理。
------------------------------「长按」二维码添加小达「进群」
与更多行业伙伴共探市场前沿资讯

艾美达(北京)医药信息咨询有限公司,成立于2014年4月,是一家专业的医药行业咨询服务提供商。公司致力于将产业政策研究与真实世界的数据挖掘深度结合,洞悉行业政策对市场的影响,通过专业的研究提供前瞻性的市场分析,为企业产品上市后的市场准入提供整体解决方案。
<END>
*版权声明:本网站所转载的文章,均来自互联网,旨在传递更多信息。鉴于互联网的开放性和文章创作的复杂性,我们无法保证所转载的所有文章均已获得原作者的明确授权。如果您是原作者或拥有相关权益,请与我们联系,我们将立即删除未经授权的文章。本网站转载文章仅为方便读者查阅和了解相关信息,并不代表我们认同其观点和内容。读者应自行判断和鉴别转载文章的真实性、合法性和有效性。







































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论