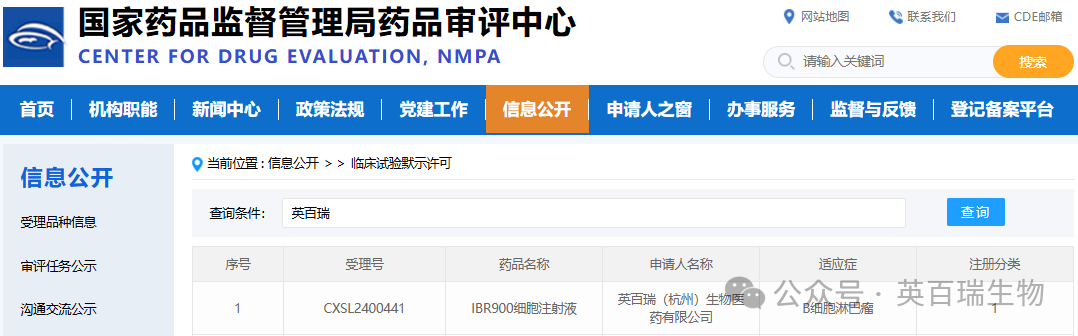
2024年9月25日,英百瑞提交的IBR900细胞注射液获得国家药品监督管理局(NMPA)的临床试验默示许可(通知书编号:2024LP02169)。IBR900注射液是英百瑞自主研发的1类生物制品,是同种异体健康供者PBMC来源的、非基因改造的、具有良好杀伤肿瘤细胞能力的通用现货型NK细胞产品。适应症为B细胞淋巴瘤。
关于IBR900细胞注射液:
IBR900是一种同种异体健康供者PBMC来源的、非基因改造的、具有杀伤肿瘤细胞能力的通用现货型NK细胞。年轻健康供者PBMC中的NK细胞可通过英百瑞自主知识产权的培养工艺,激活其免疫调节、无需预先致敏杀伤肿瘤的特性,未见细胞因子释放综合征(CRS)、神经毒性(ICANS)和异体移植的排异反应(GVHD),具有高安全性优势。IBR900细胞可通过NK细胞直接杀伤作用及分泌细胞因子、诱导凋亡等途径对血液瘤或实体瘤进行杀伤,同时也可以通过ADCC效应联合单克隆抗体对相应靶点阳性的肿瘤细胞进行杀伤。
在早期的非注册临床研究中,IBR900细胞注射液表现出极高的安全性,共有11例患者接受IBR900细胞注射液治疗,共计完成82个周期的IBR900细胞注射液治疗,均未发生因不良反应而停止治疗的事件,也没有观察到一例患者出现细胞因子风暴或感染等。显示出IBR900具有极高的安全性和强大的杀伤肿瘤细胞能力。
其中一例73岁弥漫大B细胞淋巴瘤(Ⅳ期)患者,因不能耐受化疗,接受IBR900细胞注射液联合CD20单抗治疗及IBR900细胞注射液单药治疗(单药治疗超过6个月),最佳疗效为部分缓解,截止发稿日期仍处于缓解状态,无进展生存期已达12个月,且用药过程中未发生任何不良反应。
B细胞淋巴瘤是B细胞发生的实体肿瘤,包括霍奇金淋巴瘤(HL)和非霍奇金淋巴瘤(NHL)等分型。B细胞淋巴瘤病理机制复杂多样,高度异质性且病情发展迅速,恶性程度较高的特点,严重威胁到患者的生活质量和生命安全。如弥漫大B细胞淋巴瘤(DLBCL)是一组在临床表现和预后等多方面具有很大异质性的恶性肿瘤。公司计划首先在复发/难治B细胞淋巴瘤患者中开展注册临床研究,鉴于公司产品优异的安全性与有效性的结果,尤其为那些年龄超过65岁、或因体质原因对现有治疗手段不耐受或治疗失败的患者带来新的希望。公司也计划在多种实体瘤、自身免疫性疾病、神经系统疾病、皮肤相关疾病等领域开展研究。
公司拥有专业完善的NK细胞产品制备全链条以及GMP制备中心,具备强大的研发能力,能够有效的支撑公司产品的开发迭代。具有全球最大规模的NK细胞扩增工艺,从50L-100L单批次培养体系逐渐升级。由最初的50L每批1000亿细胞提高到每批2000亿细胞,目前我们100L的培养体积单批次可达到5000亿以上。全球领先的NK细胞培养工艺,保证了批次间的稳定性好,可重复性强。大规模高质量的NK培养工艺同时可以降低成本,惠及更多患者人群。
关于英百瑞

英百瑞是一家临床阶段和风险投资支持的创新型生物医药公司,主要聚焦于全球前沿的肿瘤免疫治疗、以及免疫类疾病、慢性病和CNS类疾病的免疫治疗创新药的开发。英百瑞创始人苗振伟博士在2016年回国创业,确立了基于NK的现货通用性细胞药物研发的方向。英百瑞有国际独创的4大核心技术平台加速公司源头创新,有国际领先自主知识产权、年轻健康供者PBMC来源的体外大规模封闭式培养NK细胞的先进工艺。基于自有抗体偶联NK细胞平台技术开发了IBR854、IBR733、IBR822等多个通用现货型细胞治疗产品。目前,针对晚期实体肿瘤的全球首创IBR854细胞注射液即将进入II期临床试验和全球首款针对急性髓系白血病的IBR733细胞注射液已进入I期临床试验第二剂量组阶段。针对晚期实体瘤的IBR822是英百瑞第三款抗体-NK细胞偶联药物已于今年9月启动注册临床试验。IBR900是英百瑞第四款获得CDE临床默示许可的现货通用型NK细胞产品,临床应用的主要目标人群为65岁以上B细胞淋巴瘤或者现有治疗不耐受和失败的肿瘤患者。英百瑞还有多款在不同开发阶段的NK细胞产品。
英百瑞公司以患者需求为核心,以临床价值为导向,秉承“免疫治疗之光,点亮生命新希望”的理念,致力成为全球NK细胞免疫治疗的开拓者和领军者。
撰稿人:苏娜、裘海涛




































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论