
临床最新动态
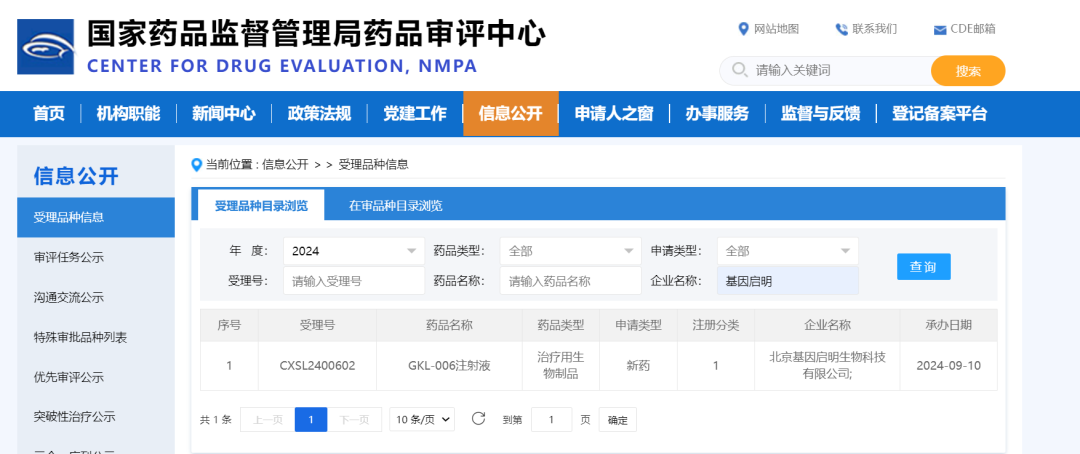
1)GKL-006注射液用于不可切除的原发性肝细胞癌的注册性临床试验已取得了重要进展。
2)GKL-006注射液用于原发性肝细胞癌患者根治性切除术后预防高危复发的注册性临床试验正在启动中。
北京基因启明生物科技有限公司成立于2015年,是全球首家开发iNKT细胞系列管线产品的头部企业;拥有生物医学、免疫学基础研究团队;iNKT细胞基础研究平台;临床研究平台;超规模扩增的细胞培养体系。国家高新技术企业、中关村高新技术企业、北京市“专精特新”企业、科技型中小企业、知识产权试点单位,中关村生物医药基地细胞产业领军企业,北京市大兴区科学技术协会副主席单位、北京专精特新企业商会副会长单位,获多项国家、国际发明专利,拥有完全自主知识产权的iNKT细胞超量扩增平台和独有的亚群分布等突破性技术。
重大突破:
(1)在全球首次完成iNKT细胞治疗原发性肝癌的安全性、有效性验证;
(2)GKL-006注射液用于治疗不可切除的原发性肝细胞癌获得国家药监局(NMPA)注册性临床试验批件(临床试验通知书编号:2023LP02333);
(3)GKL-006注射液用于原发性肝细胞癌患者根治性切除术后预防高危复发获得国家药监局(NMPA)注册性临床试验批件(临床试验通知书编号:2024LP01859)。
(4)GKL-006注射液用于不可切除局部晚期或转移性的胰腺导管腺癌获得国家药监局(NMPA)IND受理。
初步完成了我国在iNKT细胞治疗领域的核心技术突破和产业升级,实现了我国在iNKT细胞治疗领域的“领跑”地位,为加快发展新质生产力添砖加瓦。
E.N.D

往期文章推荐:
总投资5亿元,建筑面积8.8万平米!卡森细胞集团·黄河国际生命科学产业园开工
提高AAV产率新策略,增强ER蛋白加工基因表达可使AAV产量提高100%
40亿元,主要投向细胞基因治疗、医疗器械等领域,江苏无锡成立生物医药产业专项母基金
CXO迎来利好,工信部发文,药品方向重点围绕细胞和基因治疗、多肽药物、新型抗体药物等创新领域加快布局
国家三部门联合发文:四个自贸区允许外资企业从事人体干细胞、基因诊断与治疗技术开发和技术应用!
使用双AAV9载体,首款DMD碱基编辑药物完成首例患者给药,开启DMD基因编辑治疗新篇章
投资上亿元,建筑面积超2万平米,云飞医药研发及生产基地开工!
国内首个《基于mRNA-LNP技术的(细胞)免疫治疗产品开发指南》团体标准正式发布
总投资7.7亿、建筑面积超20万平米,国内一细胞与基因治疗产业项目正式开工
中国首个:锐正基因基于非病毒载体的体内基因编辑药物ART001获美国FDA临床试验许可
全球首款,数据亮眼!瑞博生物首次公布靶向FXI的药物RBD4059临床I期数据




































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论