
9月9日,据CDE 官网公司,海思科公司的1类新药HSK31858片被纳入拟突破性治疗品种,用于非囊性纤维化支气管扩张。

非囊性纤维化支气管扩张症是一种严重的慢性肺部疾病,由于感染、炎症和肺组织损伤的循环导致支气管永久性扩张。该疾病的症状包括慢性咳嗽、多痰、呼吸急促和反复呼吸道感染,这些症状可使基础病情恶化。
HSK31858是由海思科开发的一种口服、可逆性的DPP1抑制剂,主要用于治疗非囊性纤维化支气管扩张症(NCFBE),可通过抑制嗜中性粒细胞NSP酶的活化,来抑制嗜中性粒细胞的活化和向循环系统的释放。
DPP1(dipeptidyl peptidase I,二肽基肽酶1)是一种存在于中性粒细胞中的酶,它可以激活中性粒细胞蛋白酶(NSPs),包括中性粒细胞弹性蛋白酶(NE)、蛋白酶3(PR3)和卡他普西酶G(CG)。NSPs是一类具有强大的蛋白水解能力的蛋白酶,它们在正常情况下参与杀灭病原体和清除坏死组织,但在炎症性肺病中,它们的活性和数量过高,可以分解肺部的弹性纤维和胶原蛋白,导致肺部的结构和功能受损,进而导致肺部组织的损伤和纤维化。
DPP1抑制剂是一类可以特异性地结合并抑制DPP1活性的药物,它们可以通过减少NSPs的活化,降低肺部炎症和损伤,从而改善支气管扩张症等炎症性肺病的病理过程。
据公开信息,截止目前全球尚无同靶点药物获批上市,进入临床试验阶段的DPP1抑制剂仅有3款,进度最快的是Insmed的Brensocatib,Boehringer Ingelheim(BI)的BI1291583和海思科的HSK31858皆处于2期临床试验阶段,HSK31858是国内唯一进入临床试验阶段的DPP1抑制剂。
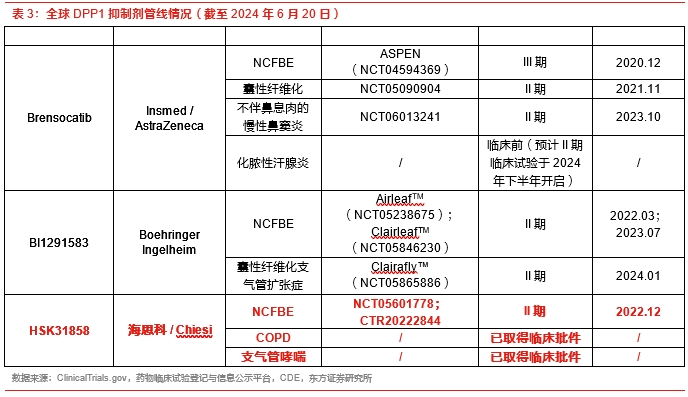
其中,Brensocatib最早由阿斯利康研发,2016年10月5日,阿斯利康以3000万美元首付款、1.2亿美元里程金的价格将其全球独家权益转让给了Insmed。今年5月,Insmed公司宣布Brensocatib治疗非囊性纤维化支气管扩张症(NCFBE)的3期临床试验ASPEN达到主要终点:与安慰剂相比,Brensocatib的两种剂量强度均在统计学上显著降低了肺部恶化(PEs)的年化率。具体数据为:与安慰剂相比,10mg Brensocatib治疗组在52周时实现肺恶化率降低21.1%;25mg Brensocatib组实现19.4%的降低。
Insmed预计在今年第4季度向FDA提交NDA, Brensocatib有望成为首个获批用于支气管扩张的DPP1抑制剂。
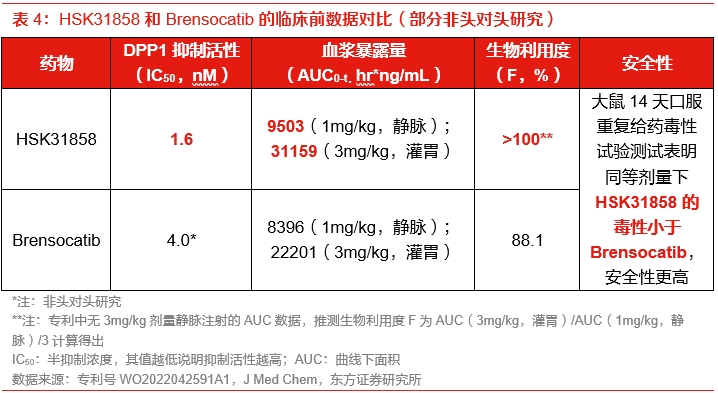
海思科的HSK31858显示出潜在同类最佳潜力。根据海思科的专利,HSK31858(推测为专利WO2022042591A1中的化合物1)在体外试验中表现出优于Brensocatib的DPP1抑制活性(非头对头研究),体内试验中也表现出更优的药代动力学特征、生物利用度和安全性。HSK31858在I期临床试验(NCT05663593)中表现出良好的安全性和耐受性,并能剂量依赖性地抑制全血NE活性。
2020年12月,HSK31858完成了一项随机、双盲、安慰剂对照的2期临床试验,显示,与安慰剂相比,HSK31858治疗12周可以显著延长NCFBE患者首次肺部加重所需的时间,同时降低肺部加重的频率。2023年11月,海思科以最高4.62亿美元与Chiesi Group签署授权协议,将HSK31858片大中华区以外权益许可给后者。
参考资料:
企业公告
【东方医药】行业专题:从Insmed DPP1抑制剂III期临床成功谈起







































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论