
内分泌系统疾病是指内分泌腺或弥漫性内分泌组织的功能异常,导致激素的过多或过少,从而引起各种疾病。据统计,内分泌领域有将近170余种疾病,可发生在全年龄阶段,内分泌治疗市场规模2023年估测为327.8亿美元,2024年达到350.5亿美元,预计2030年将达到538.5亿美元,复合年增长率为7.34%。
从药融云数据库获悉,致力于发现、开发和商业化用于治疗罕见内分泌疾病和内分泌相关肿瘤新药的Crinetics Pharmaceuticals(以下简称Crinetics)是一家总部位于美国加利福尼亚州San Diego的临床阶段的生物制药公司,由Scott Struthers博士在2008年创立。

药融云数据库:公司信息
2024年2月,Crinetics宣布同意以每股42美元的价格向机构和认可的医疗保健投资者私募出售830多万股股票,总收益预计为3.5亿美元。融资包括新投资者和现有投资者的参与,包括Adage Capital Partners L.P.、Driehaus Capital Management、EcoR1 Capital、First Light Asset Management、GordonMD Global Investments LP、Invus、Janus Henderson Investors、Paradigm BioCapital、Perceptive Advisors、Rock Springs Capital以及多家领先的共同基金。公司计划将这些资金用于临床阶段候选产品的研发、其他研究项目、营运资金和一般企业用途。截止2024年7月19日,Crinetics公司市值41.53亿美元,约合人民币300亿。截止发稿前(7月31日收盘),市值为41.89亿美元,每股53.12美元。

1. 涉足新领域,衍生新公司
研究发现,有130多种肽激素受体可以调节人体生理学的几乎所有方面,这些相同的肽受体也在各种癌症中过度表达,Crinetics打算利用其基本技术来制造结合这些受体的小分子,将放射性同位素携带到癌细胞中,用PET扫描对它们进行成像或用治疗性放射性同位素处理它们。

基于上述目的,2021年10月,Crinetics宣布与5AM Ventures和Frazier Healthcare Partners共同创立一家独立运营的新公司——Radionetics Oncology,旨在开发用于治疗各种肿瘤适应症的新型靶向非肽类放射性药物的深度管线。Radionetics的产品线基于一个广泛的平台和知识产权,利用Crinetics十多年的发现经验,公司平台使用非肽作为靶向剂,旨在向表达独特肽受体的肿瘤递送具有治疗活性的放射性药物。在公司成立的同时,Radionetics获得了Crinetics放射治疗技术平台的全球独家许可和相关知识产权,以换取股权、超过10亿美元的里程碑和净销售额的个位数特许权使用费,Radionetics以3000万美元的私募融资启动,5AM Ventures和Frazier Healthcare Partners是独家投资者,同时Radionetics还会和Crinetics进行研究合作,以确定多个其他靶点的候选药物。2024年6月底,Radionetics Oncology宣布与礼来达成战略合作,将共同推进靶向GPCR的小分子放射性药物,礼来向其注入1.4亿美元的前期资金。同时礼来保留了在未来以10亿美元收购Crinetics衍生产品的选择权,进一步巩固了双方的战略伙伴关系。
2. 明年或将推出商业化产品
Crinetics的研发管线专注于治疗内分泌疾病和相关肿瘤的小分子口服药物,具体管线的进展情况如下所示:

① Paltusotine
Paltusotine是一种口服非肽类、选择性靶向生长抑素受体2型(SST2)的激动剂,正在开发用于治疗肢端肥大症和类癌综合征。目前Crinetics已完成了肢端肥大症的临床试验3期研究和类癌综合征的临床试验2期研究。预计2024年下半年提交针对肢端肥大症的新药上市申请,与FDA确定PDUFA日期并有望在2025年下半年推出该产品。

药融云数据库:药品基本信息
肢端肥大症是以生长激素(GH)分泌过多为特征的垂体神经内分泌疾病,GH和胰岛素样生长因子1(IGF-1)长期持续分泌过多可导致全身软组织、骨和软骨的过度增生,引起面容改变,手足长大、皮肤改变、内脏长大,以及骨关节病变和阻塞性睡眠呼吸暂停综合征(OSAS)等一系列相关并发症。目前临床使用药物是SST多肽类药物(如奥曲肽Octreotide),该类药物对5种SSTR亚型受体特异性不强,易产生耐药等副反应,约30%的患者无法得到治疗。早期海外临床试验2期研究结果证明,Paltusotine有望取代目前的标准注射疗法,为肢端肥大症患者带来每日一次的口服治疗新选择。2021年第二季度,Crinetics启动了Paltusotine的临床试验3期计划,该计划包括PATHFNDR-1和PATHFNDR-2两项试验。PATHFNDR-1试验是一项为期36周的随机双盲、安慰剂对照治疗,主要评估肢端肥大症参与者从标准护理注射长效生长抑素类似物转为接受Paltusotine的治疗情况。2023年9月10日,Crinetics宣布PATHFNDR-1试验达到主要终点和所有次要终点,Paltusotine耐受性良好,在接受Paltusotine治疗的受试者中未报告严重的不良事件。

PATHFNDR-2试验是一项为期24周的随机双盲、安慰剂对照治疗,该试验在111名未接受药物治疗的肢端肥大症患者中进行,评估Paltusotine与安慰剂相比的疗效和安全性。2024年3月,公司报告了PATHFNDR-2试验的顶线结果,结果显示,该试验达成主要终点,接受paltusotine治疗患者(56%)24周后达到胰岛素样生长因子1(IGF-1)水平≤正常值上限(xULN)1.0倍的比例显著高于安慰剂组(5%,p<0.0001)。所有次要终点也均达到统计学意义,具体结果如下表所示:

类癌综合征见于约20%的神经内分泌肿瘤(NET)患者。神经内分泌瘤是一种罕见的、生长缓慢的癌症,最常发生在消化道中,当这些肿瘤转移到肝脏时,可能会发生类癌综合征,最常见的特征是腹泻和潮红。虽然注射长效生长抑素受体配体(SRL)疗法是类癌综合征的主要治疗方法,但这些注射会造成相当大的治疗负担,并且对许多患者的类癌综合征症状的缓解不足。2024年3月12日,Crinetics宣布了Paltusotine针对类癌综合征的开放标签临床试验2期研究的顶线结果,该研究是一项随机、开放标签、平行组、多中心试验,旨在评估Paltusotine在类癌综合征患者中的安全性、耐受性、药代动力学和疗效。结果表明,Paltusotine通常耐受性良好,安全性与先前的临床研究一致;可以快速和持续减少潮红发作和排便;在类癌综合征患者中的总体药代动力学特征与健康志愿者的预期一致。预计在2024年下半年开始针对类癌综合征的临床试验3期研究。

图源:国家药品监督管理局药品审评中心
2022年2月,Crinetics和日本的Sanwa Kagaku Kenkyusho(以下简称Sanwa)达成战略合作协议,Sanwa获得在日本独家开发和商业化paltustine的权利,并负责领导paltustine在日本用于肢端肥大症和神经内分泌瘤的开发和商业化。Crinetics保留在日本境外开发和商业化paltusotine的所有权利。根据协议条款,Crinetics将获得1300万美元的预付款,并有资格获得与实现某些开发、监管和商业目标相关的里程碑付款。此外,一旦帕妥索汀在日本获得市场批准,Crinetics将有资格根据产品净销售额获得分级特许权使用费。2022年8月,paltusotine获批在中国开展临床试验,用于治疗对手术或放疗反应不足,或不适用于这些治疗的肢端肥大症患者。
② CRN04894(又名Atumelnant)
CRN04894是一种口服给药的非肽类小分子ACTH拮抗剂,用于治疗ACTH(促肾上腺皮质激素)依赖性库欣综合征、先天性肾上腺皮质增生症(CAH)和其他ACTH过量疾病。ACTH依赖性库欣综合征是由垂体瘤引起的,垂体瘤分泌过多的促肾上腺皮质激素,进而导致肾上腺皮质醇的下游合成和过度分泌,皮质醇是人体的主要压力荷尔蒙,过量会导致死亡率和发病率显着增加。症状包括体重增加、脂肪沉积、皮肤变薄、容易瘀伤和疲劳等。先天性肾上腺皮质增生症是由于肾上腺类固醇激素生物合成过程某种酶先天性缺陷导致的常染色体隐性遗传性病,90%~95%的CAH病例为21-羟化酶缺乏症。临床表现谱系广泛复杂,主要为肾上腺皮质功能减退,部分患儿伴有电解质紊乱及性发育异常。
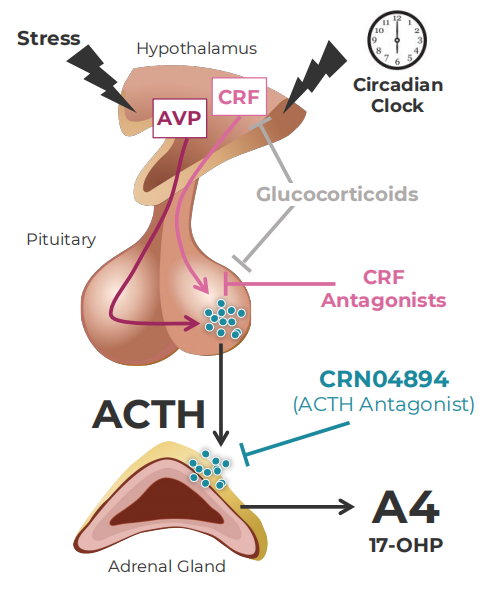
2024年6月,Crinetics公布了CRN04894研究的初步结果。针对ACTH依赖性库欣综合征的研究是一项临床试验1b/2q期、单中心、开放标签研究,旨在评估ACTH依赖性库欣综合征患者在10天治疗期间与CRN04894相关的安全性、耐受性、药代动力学和药效学生物标志物反应。该研究是与美国国立卫生研究院合作进行的,由Lynnette Nieman博士领导。结果显示,CRN04894使得ACTH依赖性库欣综合征患者的血清和尿液皮质醇快速持续降低。
针对CAH的研究(又名TOUCAHN试验)是一项为期12周的临床试验2期开放标签研究,旨在评估由21-羟化酶缺乏引起的CAH患者每天接受一次口服CRN04894治疗的疗效、安全性和药代动力学。截止2024年5月21日的数据表明,每日口服一次CRN04894可使经典先天性肾上腺皮质增生症患者的雄烯二酮和17-羟孕酮快速降低。预计该研究在2024年下半年获得研究的顶线数据;2025年上半年开始针对CAH的临床试验3期研究。

除了以上两个管线外,Crinetics的其他管线目前均处于开发阶段,包括针对甲状旁腺功能亢进的甲状旁腺激素拮抗剂、针对多囊性肾病的SST3激动剂、针对格雷夫斯病和TED(甲状腺眼病)的TSH拮抗剂、以及针对糖尿病/肥胖的口服GLP-1/GIP非肽。预计甲状旁腺激素拮抗剂和TSH拮抗剂这两个新项目会在2024年开始首次人体研究,并在2025年进入临床开发阶段。以上是两个项目的临床前疗效数据。
3. 财务状况
从药融云数据库获悉,Crinetics整体亏损在逐年增加,从公司报告的管线结果来看,公司逐年增加的投入似乎在近两年会有所回报。

药融云数据库:公司年报
Crinetics在2023年度的研发费用为1.685亿美元,上年同期及1.302亿美元。一般及行政费用为5810万美元,上年同期为4240万美元。研发费用和行政费用的增加主要归因于人事成本的增加。2023年公司净亏损2.145亿美元,上年同期为1.639亿美元。2023年全年收入为400万美元,而2022年同期为470万美元。

2024年第一季度的研发费用为5330万美元,上年同期为3850万美元。该项增加的主要原因是人事费用增加了940万美元,外部服务和设施费用增加380万美元,制造和发展活动支出增加140万美元。一般和行政费用为2080万美元,上年同期为1220万美元。增加的主要原因是人事费增加560万美元。2024年第一季度净亏损6690万美元,上年同期为4600万美元。2024年第一季度的收入为60万美元,收入来自2024年Paltusotine候选产品的许可安排以及2023年Paltusotine和CRN01941候选产品的许可安排。

截至2024年3月31日,Crinetics的非限制性现金、现金等价物和投资总额为9.010亿美元,2023年年底只有5.586亿美元,在2024年2月28日,Crinetics进行了私募股权融资,募集资金总额约为3.5亿美元。根据目前的预测,预计其现金、现金等价物和短期投资将足以为公司到2028年的运营计划提供资金。当然,如果公司最先进管线有望在明年推出,公司就有望在明年之后实现收入增长,并能够接连推进其他管线的进展,以下是Crinetics到2030年预期的战略情况:

此文仅用于向医疗卫生专业人士提供科学信息,不代表平台立场,不作任何用药推荐
参考来源:
[1] CDE/NMPA官网
[2] 药融云数据库
[3] FDA/EMA/PMDA
[4] 相关公司公开披露(除标注外,正文图片均来自企业官网)
https://crinetics.com/;
https://mp.weixin.qq.com/s/RCTpRF-exA8QZMjCq24cqg;
https://radionetics.com/news/radionetics-oncology-enters-into-strategic-agreement-with-lilly;
https://rs.yiigle.com/m/CN131222202127/1328050.htm#:~:text=%E5%B8%95%E7%91%9E%E8%82%BD%E4%BA%8E2014,%E6%B2%BB%E7%96%97%E8%82%A2%E7%AB%AF%E8%82%A5%E5%A4%A7%E7%97%87%E3%80%82;等等。
<END>
想要解锁更多药企信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药企公司基本信息、投融资情况、产品管线分布、药物销售情况与各维度分析、药物研发情况、年度报告、最新进展动态、临床试验信息、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!







































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论