
体内基因编辑是一种直接在生物体内进行基因编辑的技术,通过这种方法,可以修复、替换或删除有缺陷的基因,以治疗遗传性疾病或其他相关疾病。CRISPR-Cas9技术通过RNA指导Cas9蛋白精确剪切DNA,具有一次性治愈、高精准度、广泛应用和持久效果等特点。尽管在多种疾病治疗上显示出潜力,但仍需克服脱靶和递送效率等技术难题。
mRNA-LNP和AAV是目前体内基因编辑常用的两种递送工具,它们各自的优缺点如下:
| 递送系统 | 优点 | 缺点 |
|---|---|---|
| mRNA-LNP | 快速表达、大容量、非整合性 | 肝外组织靶向性较差、暂时性表达 |
| AAV | 表达时间长、组织特异性、高感染效率 | 容量小(~4.5kb)、低频定点整合 |
将mRNA-LNP和AAV组合用于体内基因编辑系统的递送将实现优缺点互补:
目前已有研究将mRNA-LNP和AAV组合用于体内基因编辑,提升了基因编辑的效率,降低了给药剂量。
一位中国学者发表在nature biotechnology的文章评估了单独使用LNP递送SpCas9 mRNA和sgRNA,以及用LNP递送SpCas9 mRNA,AAV5递送gRNA在小鼠肺部的基因编辑效果。给药方式为单独使用LNP递送SpCas9 mRNA和sgRNA组以不同的剂量给药三次,而LNP-mRNA+AAV组则给单剂AAV5-sgRNA,三剂LNP-SpCas9 mRNA,结果显示后者的基因编辑效率比前者高10%~14%。
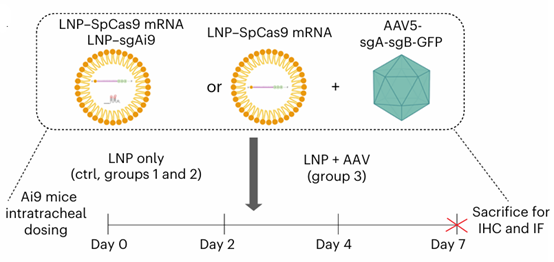

近日,基因疗法研发公司Tessera Therapeutics联合悉尼大学研究人员在Molecular Therapy上发表研究论文,在鸟氨酸转氨甲酰酶(OTC)缺乏症小鼠及诱导肝增殖的非人灵长类(NHP)中,评估了包封SB100X转座酶mRNA的脂质纳米颗粒(LNP)与AAV-DNA模板共递送的治疗效果。研究表明,mRNA-LNP + AAV组合方式避免了双AAV递送系统带来的转座酶非瞬时表达引起的持续异位和过度转座事件,并有效减少了AAV载体剂量,实现较传统AAV更好的基因编辑效果。

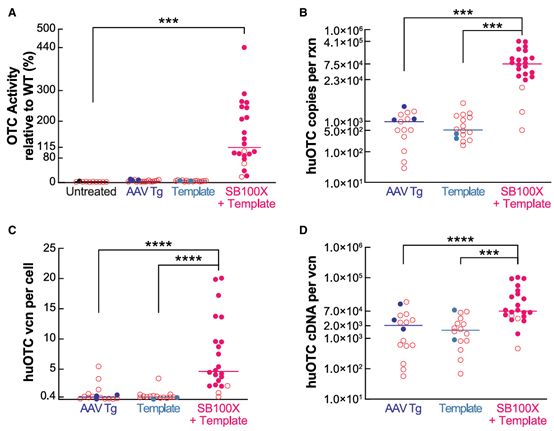
图2 SB100X mRNA和AAV构建体的序列示意图,小鼠全肝裂解物分析
基因编辑领域的头部企业Intellia Therapeutics正在开发一款体内基因治疗药物NTLA-3001,用于α-1抗胰蛋白酶缺乏症(AATD)相关肺病的治疗。该药物的作用原理是将功能性SERPINA1基因靶向插入白蛋白基因位点,使患者能够持续表达功能性AAT蛋白,从而阻止肺病的进展。NTLA-3001用LNP递送Cas9 mRNA和sgRNA,用AAV递送功能性SERPINA1基因,在NHP动物模型给药后,可以产生生理水平的hAAT,已持续一年以上。
 图3 NTLA-3001的作用原理及其在NHP动物模型中疗效评估
图3 NTLA-3001的作用原理及其在NHP动物模型中疗效评估
综上所述,mRNA-LNP和AAV组合用于体内基因编辑,可提高基因编辑效率,大幅减少药物使用剂量,从而提高药物安全性并降低未来基因疗法的成本。
派真生物可提供多种基因编辑mRNA现货以及AAV包装服务,助力您的体内基因编辑实验。
派真生物一站式CRO&CDMO服务平台,可为您提供全面的基因编辑工具和个性化定制服务。我们的产品线涵盖腺相关病毒(AAV)载体、mRNA、慢病毒载体,为您的体内基因编辑研究提供全方位的支持。
目前派真暑期大促火热进行中,mRNA现货低至500元,包AAV,满额送华为、苹果电子产品等豪礼,欢迎拨打13503000954或后台留言咨询!



参考资料:
1.https://doi.org/10.1038/s41587-023-01679-x
2. https://doi.org/10.1016/j.ymthe.2024.06.021
3. a57908a6-aaca-404d-9072-32471cd3d41e (intelliatx.com)






































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论