
ADC是肿瘤领域发展最快的治疗方式之一,目前已有15种ADC获批,超过210种正在进行临床试验。近年来,ADC的药物研发进入百花齐放阶段,特别是在HER2、EGFR、Trop2、CLDN18.2、Nectin-4等靶点上展示出显著的疗效和良好的安全性,联合用药,双抗ADC效果显著,为患者提供了更多的治疗选择。随着技术的不断进步和创新,ADC疗法在癌症治疗领域的应用前景十分广阔。
预计阅读时间:10分钟
抗体药物偶联物(Antibody drug conjugates, ADC)被称为癌症治疗的“魔法子弹”,它是一种将单克隆抗体与细胞毒性药物通过化学连接子连接而成的新型生物治疗药物。其概念核心在于将抗体的特异性靶向能力和细胞毒性药物的强大杀伤作用相结合。ADC进入血液循环后,其抗体部分能够特异性地识别并结合肿瘤细胞表面的靶抗原,形成ADC - 靶抗原复合物,然后通过细胞的内吞作用将ADC摄入细胞内部。进入细胞后,连接子在特定的细胞内环境下发生裂解,释放出细胞毒性药物,从而对肿瘤细胞产生杀伤作用。这种设计旨在实现对肿瘤细胞的精准打击,减少对正常细胞的损害,提高癌症治疗的有效性和安全性。

ADC药物开发需综合考虑多个关键因素。首先是靶点选择,要注重其在肿瘤细胞的特异性高表达及与肿瘤生物学过程的相关性;抗体设计方面,需确保低免疫原性、强特异性、高内化效率和长的半衰期,以实现ADCs在体内的有效传递;连接子设计要兼顾稳定性与可裂解性,还有化学性质的兼容性,同时应避免引起ADC聚集,防止在血液中过早释放有效载荷,并在目标位置精确释放活性药物;细胞毒性药物要确保在生理条件下表现出稳定性,并具有能够与抗体结合的官能团;除了选择抗体、连接子和细胞毒性药物之外,将小分子组分附着到抗体上的方法是成功构建ADCs的关键要素,选择合适的偶联方式,对ADC的稳定性和疗效有显著影响。ADC的概念由德国医学家、诺贝尔奖得主Paul Ehrlich在20世纪初首次提出。然而,直至20世纪70年代单克隆抗体问世以及蛋白重组工程技术成熟,ADC的研究才逐渐成为抗体药物研发的热门领域。2000年,惠氏制药研发的Mylotarg获得美国FDA加速批准,用于治疗CD33阳性的急性髓系白血病(AML)患者,此药物成为全球首款商业化的ADC药物。但因临床研究中出现致死性毒性,该药物于2010年撤市,后在2017年经规格调整和补充临床证据后再次获批上市。此后,ADC领域经历了漫长的沉寂期。
在这期间的八年内,仅有Adcetris、Kadcyla、Besponsa以及Lumoxiti四款新产品获批,整个ADC市场增长缓慢。2019年成为ADC发展历程中的重要分水岭。仅在这一年,就有Polivy、Padcev、Enhertu三款ADC获批。其中,由第一三共与阿斯利康合作的Enhertu被业内视为“ADC领域急剧回暖最大的催化剂”。Enhertu在Destiny - Breast系列研究中取得了颠覆性成功,显著改善了乳腺癌患者的生存和缓解水平。并且,由于Enhertu对HER2阳性和低表达的肿瘤均具有显著活性,这使得业界更加关注ADC对靶标以外恶性细胞的“旁观者效应”。2019年之后,ADC赛道迎来了Trodelvy、Blenrep、Zynlonta等产品的密集获批,市场规模也随之呈指数增长。然而,ADC 药物市场也面临一些挑战,如企业间合作的终止、潜在的耐药性问题等。但总体而言,其增长趋势明显,市场潜力巨大,在癌症治疗及相关领域的发展值得期待。
自首个HER2单抗药物获批后,HER2靶点在肿瘤治疗领域就备受关注,至今已经历了二十多年的发展历程。当前,已获批的HER2 ADC药物有恩美曲妥珠单抗、德曲妥珠单抗、维迪西妥单抗三种,此外还有大量HER2 ADC药物正处于临床研究阶段,像恒瑞医药的SHR - A1811和石药集团的DP303c等。在这些药物中,德曲妥珠单抗(DS - 8201,Enhertu)因具备独特的结构和高效的抗肿瘤活性,成为HER2 ADC领域中一项重大突破(图3)。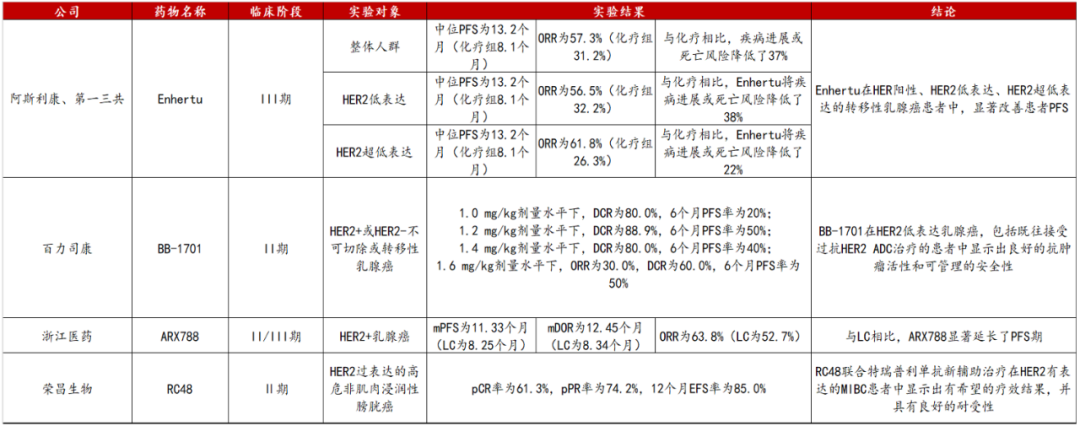
图3.2024 ASCO 最新HER2 靶点ADC药物数据DS-8201是由第一三公与阿斯利康联合开发的人源化靶向HER2的ADC药物。自2019年首次获批以来,该药已在美国、日本、欧盟、中国多个国家和地区获批上市,适应症领域涵盖 HER2 阳性乳腺癌、HER2 阳性胃癌、HER2 低表达乳腺癌、HER2 突变非小细胞肺癌、HER2 阳性实体瘤。在获批适应症和地区不断扩展的同时,德曲妥珠单抗的销售额也是逐年上涨。2023 年,德曲妥珠单抗全球销售额约3959亿日元(约30亿美元),同比增长约78%(图4)。
图4.DS-8201临床试验布局及全球销售收入
Trop2 ADC在肺癌领域的发展现状具有多面性。在疗效方面,不同公司的产品在不同亚组人群疗效各异。第一三共和科伦博泰的产品对EGFR阳性和非鳞癌人群疗效佳,但对EGFR野生型或鳞癌患者疗效受限;吉列德的产品在驱动基因突变人群疗效好,对非鳞癌和鳞癌有效性相当。戈沙妥珠单抗、SKB264、Dato - DXd在全球开发进展中领先。临床布局上各公司差异显著。科伦博泰/默沙东临床试验多,依据EGFR突变、PD - L1表达量和临床标准疗法对肺癌人群开展注册研究。第一三共/阿斯利康试验数量也较多,首个三期临床未区分基因和蛋白标志物,联合疗法布局更广,而吉列德试验数量少(图5)。 
2024年ASCO大会上,科伦博泰二期临床研究OptiTROP - Lung01初步数据亮眼,SKB264联合PD - L1单抗一线治疗驱动基因阴性NSCLC表现优异,低剂量组中位PFS达15个月,相比其他药物更具优势,凸显出SKB264(图6)与肿瘤免疫治疗药物联用在NSCLC领域潜力巨大。 Nectin - 4 ADC作为一种极具潜力的肿瘤治疗药物,在研发方面取得了显著进展(图7),在国际上,Seagen的Padcev是一款较早受到关注的Nectin - 4 ADC药物,在尿路上皮癌的治疗中取得了一定突破。然而,Padcev存在着如皮肤毒性等不良反应问题,这为后续研发提出了改进方向。国产企业在Nectin - 4 ADC研发中展现出强大的创新能力。迈威生物和石药集团等企业采用了先进的第三代ADC技术。这种技术通过对药物偶联工艺进行优化,大大提高了药物的均一性,减少了副作用。
以迈威生物的9MW2821和石药集团的SYS6002为代表,它们各自运用独特的技术实现了更优的疗效和安全性。9MW2821采用的IDDC技术以及SYS6002运用的转氨酶技术,都为药物的性能提升做出了贡献。这些技术使得药物能够更精准地作用于肿瘤细胞,在增强对肿瘤杀伤能力的同时,尽量避免对周围正常细胞的损害,进一步提高了治疗效果和患者的耐受性。从整体发展趋势来看,国产Nectin - 4 ADC前景广阔。随着研发的持续推进,有望在更多的适应症中展现其治疗价值。这不仅将为更多肿瘤患者提供新的治疗选择,也将进一步提升国产药物在国际肿瘤治疗领域的地位,推动全球肿瘤治疗水平的提高。
图7.Nectin-4 靶点ADC药物研发进展
CLDN18.2 ADC研发进展迅速(图8)。国内众多药企积极参与,其中信达生物的 IBI343、康诺亚与乐普生物合作的 CMG901、礼新医药的 LM - 302等产品已处于临床研究相对后期阶段。例如 IBI343被纳入突破性治疗药物名单,CMG901获得多项国际认定且临床数据表现出可观的客观缓解率和疾病控制率,LM - 302在不同癌症适应证的研究中也显示出较好的效果。此外,恒瑞、石药、德琪、健信等药企的相关产品也都在积极开展临床研究,大量临床数据不断涌现,为后续研发和药物优化提供依据,有望为癌症治疗带来新曙光。

随着肿瘤学导向的 ADC 药物的快速批准,未来可能会继续沿着现有路径发展,包括更多携带 TOPO1i、微管抑制剂和 DNA 损伤剂的 ADC 药物的研发,对已批准 ADC 药物在未探索适应症中的测试,以及对 ADC 与免疫检查点抑制剂和其他抗癌药物组合的评估。同时,为了实现 “魔法子弹” 的梦想,需要对 ADC 药物进行进一步的创新设计。这包括对 ADC 分子特征的精细调整,如通过选择具有不同效力和作用机制的细胞毒性分子、调整药物与抗体的比例以及链接技术等,以提高药物的活性并降低毒性。
此外,还可以通过联合使用其他药物或采用新的给药策略来优化 ADC 药物的性能。同时,更激进的创新思路包括替换 ADC 的一个或多个组件,如开发双特异性或多特异性 ADC、引入肽掩模、改造抗体的结合特性以及使用更小的分子替代抗体等。尽管 ADC 药物已经取得了显著进展,但我们对其作用机制的理解仍然有限。未来需要进一步深入研究 ADC 药物在体内的作用过程,包括药物的摄取、分布、代谢和排泄等环节,以及药物与靶点和其他生物分子之间的相互作用。这将有助于我们更好地设计和优化 ADC 药物,提高其治疗效果和安全性。













































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论