
由于缺乏有效的治疗靶点,三阴性乳腺癌(TNBC)是最致命的乳腺癌亚型。剪接因子SF3A2在TNBC组织中显著上调,并促进TNBC的进展。机理研究发现,E3泛素蛋白连接酶UBR5 促进泛素依赖性SF3A2的降解,而SF3A2又反过来调节 UBR5,从而形成一个反馈回路,平衡这两种促癌蛋白。此外,SF3A2至少部分地通过特异性调节MKRN1的可变剪接,即促进致癌异构体MKRN1-T1的表达,来促进TNBC的进展。此外,SF3A2还参与了外源性和内源性细胞凋亡的调控,从而导致TNBC细胞对顺铂产生耐药性。总之,这些发现揭示了SF3A2在TNBC进展和顺铂耐药中的未知作用,有望为治疗TNBC提供新的潜在治疗靶点。

01
SF3A2在三阴性乳腺癌组织中异常上调,且与TNBC患者的不良预后相关
为了鉴定促进TNBC进展的潜在靶点,作者分析了136个剪接因子的表达水平。84个剪接因子蛋白水平表达失调,64个剪接因子mRNA水平失调。其中有48个剪接因子在蛋白水平和mRNA水平均失调。根据筛选列表的排名,作者选择了SF3A2来进一步探究。


02
SF3A2促进TNBC细胞增殖,克隆形成,迁移和侵袭
为了探索SF3A2在三阴性乳腺癌细胞的生物学功能,作者检测了正常乳腺上皮细胞系MCF10A和其他10个代表性的乳腺癌细胞系中SF3A2的蛋白表达水平。基于SF3A2在这些细胞中的表达,作者分别在MDA-MB-231和SUM159PT细胞上敲低SF3A2。细胞功能学实验表明,SF3A2 敲低抑制TNBC细胞的增殖,侵袭和迁移能力。为进一步验证,设计了靶向SF3A2的UTR的shRNA序列,回补SF3A2能逆转SF3A2敲低所导致的细胞增殖、侵袭和转移能力下降。而在正常的乳腺癌细胞系中则没有明显表型。


03
SF3A2与UBR5相互作用,UBR5作为SF3A2的泛素连接酶,抑制SF3A2蛋白的表达
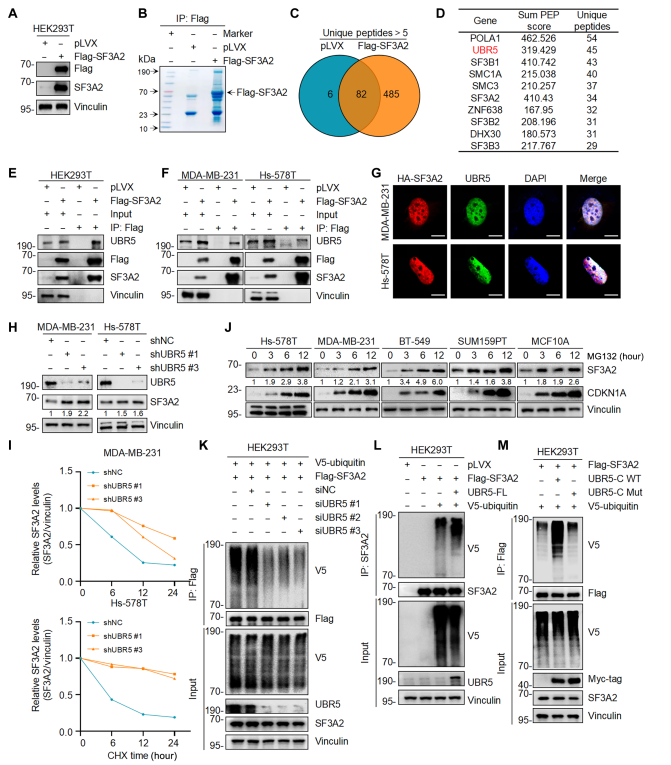
为探索SF3A2潜在的调节机制,在293T上过表达带Flag标签的载体,对IP产物进行质谱鉴定来寻找SF3A2相互作用蛋白。在这些相互作用蛋白中E3泛素化蛋白连接酶UBR5被选择来进行进一步验证。SF3A2和UBR5的互作进一步在MDA-MB-231和Hs578T细胞中验证。IF表明SF3A2部分与IBR5共定位。综上,SF3A2与UBR5存在相互作用关系。
由于UBR5是E3泛素连接酶,作者假设UBR5可能是SF3A2的上游调控子。已有报道表明UBR5的C端HECT结构域对其E3连接活性至关重要,HECT的C2768A突变导致催化失活。作者通过构建UBR5-C WT及UBR5-C Mut(C2768A)质粒,发现UBR5-C WT能降低SF3A2蛋白水平,而UBR5-C Mut(C2768A)则不能。体内泛素化实验表明UBR5-C WT而非UBR5-C Mut(C2768A)能够增强SF3A2的泛素化水平。综上实验证明,UBR5作为SF3A2的 泛素连接酶能够调控SF3A2的稳定性。

04
SF3A2缺失引起TNBC细胞的可变剪接事件的变化
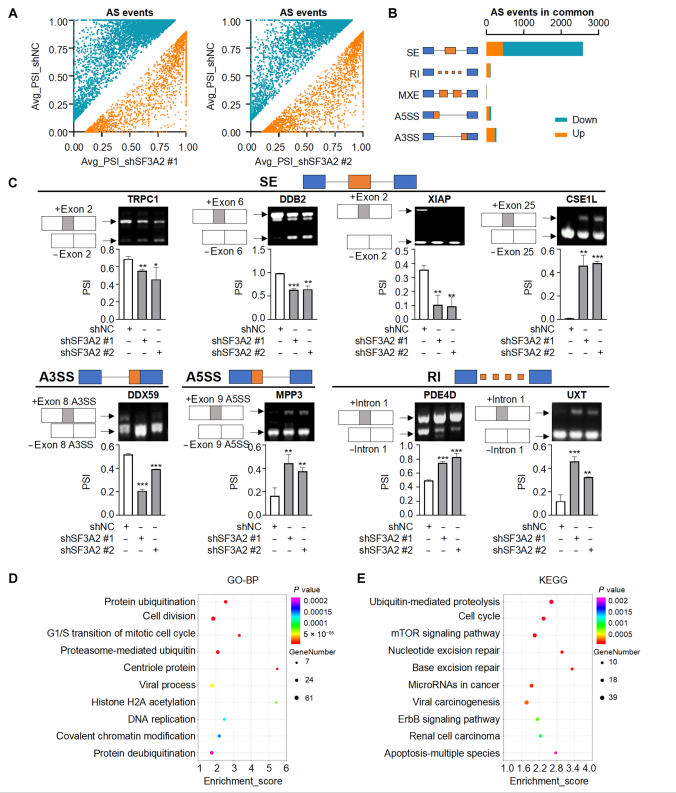
SF3A2是U2复合体的核心组分,IP实验证实了SF3A2与U2 snRNP复合体组分的相互作用。但是SF3A2缺失并不影响这些蛋白(SF3B1, SF3B2, SF3B3)的表达,说明SF3A2并不影响U2复合物的稳定性。作为一个剪接因子,SF3A2可能通过调节AS继而影响肿瘤进展。作者用SF3A2敲减及对照的MDA-MB-231细胞进行RNA-seq,并通过RT-PCR验证了部分结果。KEGG和GO分析表明SF3A2调节的可变剪接事件主要涉及蛋白泛素化、细胞周期、细胞分裂、细胞损伤。

05
SF3A2调节MKRN1的可变剪接转换
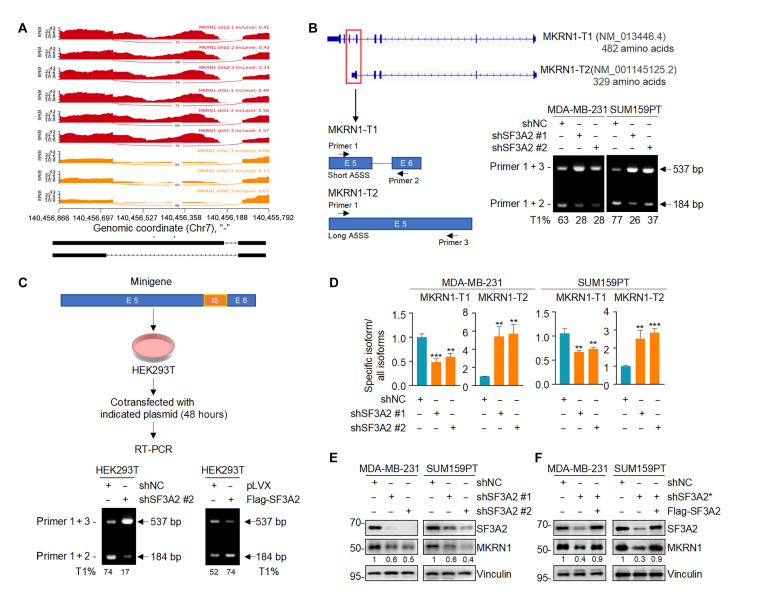
由于泛素化通路在GO和KEGG中排分第一,作者选择了一个经典的E3泛素连接酶MKRN1来进行进一步探究。SF3A2缺失时MKRN1的5号外显子通过A5SS差异保留。MKRN1通过A5SS 产生了两种主要的异构体:全长MKRN1(MKRN1-T1)和截短MKRN1(MKRN1-T2)。MKRN1-T1的第5号外显子较短,编码含有482个氨基酸的蛋白质,而MKRN1-T2的第5号外显子较长,编码含有329个氨基酸的蛋白质。minigene报告基因实验表明,SF3A2 缺失显著抑制短的exon 5的保留。此外,RT-qPCR显示,SF3A2缺失导致MKRNA1-T1的mRNA水平下降,相应的MKRN1-T2的mRNA水平则上升,在SF3A2缺失后,MKRN1-T1的蛋白水平下降,而通过重新表达SF3A2则可以恢复。综上表明,SF3A2可调控MKRN1的可变剪接转换。

06
SF3A2部分通过调节MKRN1的可变剪接转换来发挥其肿瘤促进作用
为了探索SF3A2在TNBC细胞中发挥其促肿瘤作用是否是通过调节MKRN1的可变剪接,作者在MDA-MB-231和SUM159PT细胞中敲低SF3A2,然后分别过表达MKRN1-T1和MKRN1-T2,使用这些稳定细胞系进行的功能测试表明,恢复MKRN1-T1(而非MKRN1-T2)可有效逆转SF3A2敲减对TNBC细胞生长和转移的影响。并进一步在体内进行验证。此外,用肺转移LM2-4175细胞系研究裸鼠的自发性肺转移。肺转移的发生率表明,SF3A2的耗竭会明显降低LM2-4175细胞的转移能力,而MKRN1-T1的恢复则可逆转这种能力。结果表明,SF3A2至少在一定程度上促进了TNBC的进展、通过改变MKRN1的剪接模式并促进MKRN1-T1的表达。


07
SF3A2缺失可通过MKRN1介导的FADD蛋白酶体降解途径从而促进细胞凋亡。SF3A2缺失会导致γH2AX水平升高并增加TNBC细胞对顺铂的敏感性
已有报道表明MKRN1通过泛素依赖的FADD降解从而调节DR介导的外源性凋亡。实验表明,SF3A2缺失导致FADD蛋白水平显著上升,促进TNBC细胞的凋亡。同时也探究了MKRN1不同异构体对FADD的调节作用。这些数据揭示了SF3A2-MKRN1-FADD通路在TNBC细胞外源性凋亡中的调节作用。
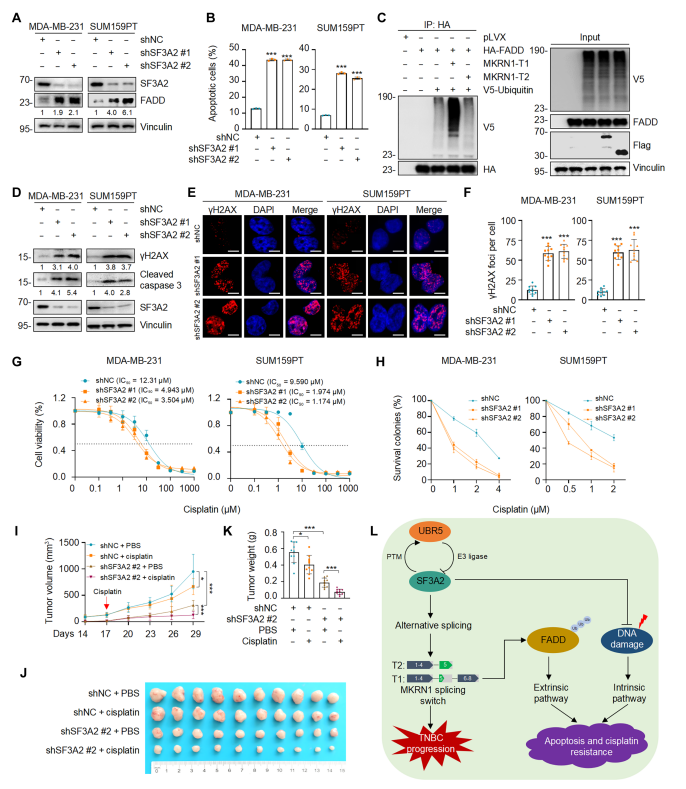
顺铂药物广泛用于TNBC患者,能促进细胞的凋亡。但耐药性的产生限制了顺铂的临床应用。作者进一步探索SF3A2对TNBC细胞顺铂耐药的影响。体内外实验表明,SF3A2是TNBC细胞产生顺铂耐药性的原因之一。
业务咨询



和元生物成立于2013年,作为深耕细胞和基因治疗核心领域的高新技术企业,专注于为细胞和基因治疗的基础研究提供基因治疗载体研制、基因功能研究、药物靶点及药效研究等CRO服务;为细胞与基因治疗药物的研发提供工艺开发及测试、IND-CMC药学研究、临床样品及商业化产品的GMP生产等CDMO服务;为再生医学及抗衰领域提供细胞制备、重组蛋白/外泌体等细胞衍生物生产、细胞存储等技术服务。致力于推动细胞和基因治疗及相关健康产业的技术开发及转化应用,造福生命健康。






































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论