
2024年11月13日,南方科技大学理学院化学系田瑞军教授团队联合海内外团队在 Nature 期刊发表题为“Clinical functional proteomics of intercellular signaling in pancreatic cancer”的研究论文,新研究开发了一类多维度临床功能蛋白质组学分析策略,并利用该策略系统解析了胰腺癌肿瘤微环境中的细胞间信号转导网络。
研究为发现全新胰腺癌标志物、药物靶点提供了系统功能蛋白质组大数据和新思路。

胰腺导管腺癌(PDAC)是胰腺癌的主要类型,也是最致命的癌症类型之一。目前,大部分胰腺癌被发现和诊断时已经是晚期阶段,患者会错过手术治疗的最佳时机,因此,开发可靠的早期诊断生物标志物和有效的靶向药物对癌症治疗、改善预后至关重要。
肿瘤微环境(TME)是癌症的关键特征,也影响了肿瘤的发生、发展以及免疫逃逸。在PDAC的肿瘤微环境中,存在大量非恶性间质细胞和细胞外基质,这些成分与肿瘤细胞存在密切的相互作用,可促进其增殖、转移和耐药。
当下,科学家可以通过基于质谱的蛋白质组学来系统地探索 PDAC 细胞间的信号转导过程,但目前的蛋白质组学研究大多处于细胞水平,或通过收集块状肿瘤样本来开展,这些方式仅能获得平均化分析结果,难以全面揭示临床样本中真实功能蛋白质组特征。
为此,田瑞军教授团队研究开发了一种临床功能蛋白质组学策略 TMEPro,该技术从底层原理出发,从湿实验和干实验两方面入手,采用多种蛋白质组学策略多维度解析肿瘤样本中功能蛋白质组特征,系统性解决了此前技术面临的难题。
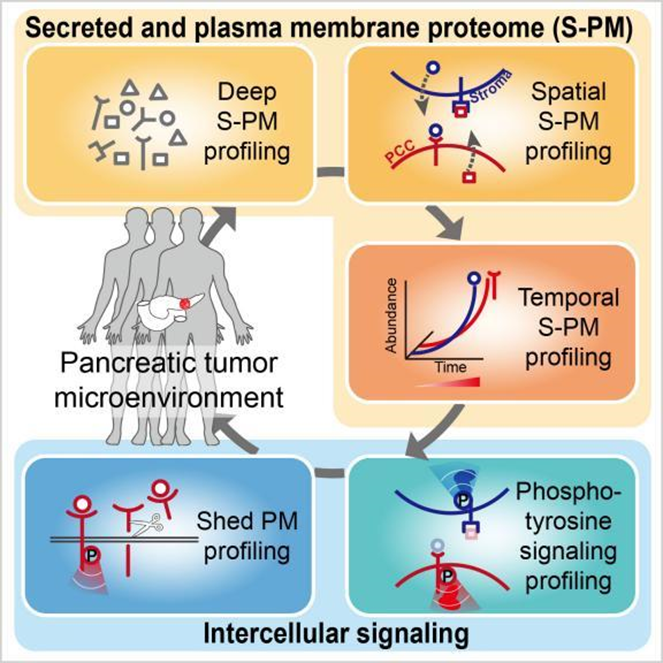
研究示意图
如上图所示,临床功能蛋白质组学策略TMTPro能从五个纬度对同一微量肿瘤样本进行分析。分泌蛋白和膜蛋白(简称S-PM蛋白)是细胞间信号转导的关键调控机器,也是最重要的生物标志物和药物靶点,因此,TMTPro策略针对S-PM蛋白进行了规模化分析。
由于大部分S-PM蛋白都具有高度糖基化的分子特征,新研究开发了基于双功能肼化学探针的糖蛋白标记策略,以此来同时富集这两类重要的功能蛋白。
该策略在100例PDAC等临床组织样本中共鉴定了近3000种 S-PM 蛋白,覆盖了近一半左右的人类蛋白组中已知的S-PM蛋白质组。此外,该策略还鉴定出了大量已知的癌症生物标志物和药物靶点。研究者也构建了目前最大规模、覆盖最全面的S-PM蛋白组大数据集,为研究胰腺癌细胞间信号转导网络和发现新的胰腺癌生物标志物和药物靶点提供了坚实的大数据基础。
为了进一步解析S-PM蛋白质组的细胞类型来源和细胞间信号转导流向,研究者开发了空间可视化蛋白质组学分析策略,系统地分析了13例PDAC肿瘤组织样本的癌细胞区域和基质细胞区域,得到了目前最大的PDAC空间蛋白组数据集。
上述数据集可实现对S-PM蛋白质组中近80%蛋白的细胞类型定位注释,研究发现细胞外基质通路相关蛋白主要富集于间质细胞,而绝大多数转运体相关蛋白则是来源于癌细胞。此外,研究者系统分析了两种细胞类型间的信号转导网络,共鉴定了260余对癌细胞与基质细胞间的旁分泌配体-受体膜蛋白信号轴。
随后,研究进一步解析了S-PM蛋白组随胰腺癌演进的动态变化趋势,研究者收集了PDAC模型KPC小鼠,早中晚期的肿瘤样本从时间维度上定量地对S-PM蛋白组进行分析。
通过系统比较人类来源数据与KPC小鼠数据中显著性变化的蛋白,研究者发现大部分蛋白具有一致的变化趋势,首次从组学层面证明了KPC小鼠在PDAC功能蛋白质组学研究中的合理性。
更为重要的是,上述组学数据的聚类分析揭示出S-PM蛋白质组具有三种显著的变化趋势。
其中,众多已报道的癌症标志物和药物靶点主要集中在中晚期才开始上调的数据集中,这里面揭示了晚期胰腺肿瘤中活跃的细胞间信号转导网络;而在肿瘤发展早期就显著上调的数据集,为发现新的早癌筛查标志物和药物靶点提供了重要的临床大数据资源。
酪氨酸磷酸化(pTyr)是细胞间信号转导网络激活的重要特征,异常的pTyr与肿瘤发生发展密切相关。为尽可能全面解析微量肿瘤组织样本中的pTyr蛋白质组,研究者通过两种蛋白质组学策略对其进行分析。
首先,团队通过前期开发的三功能化学交联探针,实现对pTyr修饰蛋白和相互作用蛋白的定量蛋白质组学分析;其次,通过高选择性直接富集pTyr多肽实现高灵敏度pTyr位点鉴定。
这两种策略的联合分析,实现了对pTyr蛋白质机器中酪氨酸激酶、酪氨酸磷酸酶以及酪氨酸磷酸化结合蛋白深度解析,并发现该蛋白质机器在胰腺癌中普遍高度激活,为细胞间信号转导网络的系统解析提供了关键功能维度数据。
研究者对上述四个维度的蛋白质组学数据进行了系统的多维度整合分析,构建了胰腺癌肿瘤微环境中癌细胞和间质细胞的双向分泌配体-受体膜蛋白-下游功能蛋白信号轴,共解析出1600多种关键的细胞间信号轴。
研究者挑选了血小板衍生生长因子和受体(PDGF-PDGFR)介导的,从肿瘤细胞到间质细胞的旁分泌信号轴进行验证,证明上述临床功能蛋白质组数据的可靠性。
令人意外的是,研究者通过进一步功能蛋白质组学分析发现了一个新的癌细胞-间质细胞互作的双向信号环路,即癌细胞分泌的PDGFs通过激活CAFs细胞的PDGFR-PTPN11-ERK-FOS信号通路,调控CAFs细胞分泌配体蛋白LIF的表达和分泌,进而激活癌细胞的LIFR-GP130-STAT3通路。
而研究者于2019年共同发表的Nature文章发现了LIF在胰腺癌中的重要生物学功能,并系统证明了它作为有效治疗靶点以及肿瘤诊断标志物的潜力。
值得一提的是,首个中和性LIF抗体靶向疗法,正在开展经美国FDA批准的二期临床试验。
最后一个维度的TMEPro分析,是基于创新预测算法的肿瘤微环境中膜蛋白胞外区脱落分析。
该分析源于TMEPro分析策略发现的数百种显著性变化蛋白酶,作者在此基础上成功地预测了22种高可信的发生膜外区酶切脱落的膜蛋白。作者对发生酶切脱落最为显著的受体酪氨酸激酶AXL进行了系统地验证,并发现MMP1和MMP11是胰腺癌肿瘤中特异性调控AXL等膜蛋白胞外域脱落的蛋白酶。
由于AXL与肿瘤进展密切相关,且其激酶抑制剂已经进入美国FDA批准的胰腺癌二期临床试验,研究者对这一额外维度的细胞间信号转导轴进行了系统的功能研究。
其开发了空间糖蛋白质组学分析流程,并对50例肿瘤组织中AXL胞外域、AXL完整蛋白及其分泌配体蛋白GAS6实现了极具挑战的绝对定量分析。
上述分析揭示约70%的AXL都发生了胞外域脱落,并发现当脱落的AXL量小于其配体GAS6时,病人更趋向于发生转移。更重要的是,研究者通过靶向酪氨酸磷酸化蛋白质组学分析等系统证明游离的AXL可以极高亲和力地结合GAS6,进而显著抑制AXL信号通路的激活。
此外,研究者在66例PDAC类器官的联合给药实验中发现联合抑制AXL的激酶活性和蛋白酶介导的胞外域脱落具有显著的协同效应,并在小鼠移植瘤和原位瘤模型中得到了验证。
总而言之,基于该项研究所开发的多维度临床功能蛋白质组学分析策略TMEPro,以及一个交互式数据检索网站TMExplorer, 不仅为系统解析肿瘤等组织微环境中的细胞间信号转导网络提供了新颖的系统水平功能蛋白质组学分析工具,还为探寻胰腺癌治疗和诊断的分子靶点提供了重要的大数据集。
此外,本研究所发现的细胞间信号转导回路和基于定量空间糖蛋白质组学分析的额外维度细胞间信号转导调控有望为胰腺癌靶向药物临床研究提供有益线索。
交互式数据检索网站 TMExplorer:
http://bioinfo.chem.sustech.edu.cn/TMExplorer_Beta/user-login.jsp
论文链接:
https://doi.org/10.1038/s41586-024-08225-y
免责声明





































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论