 关注小药说药,一起成长!
关注小药说药,一起成长!在过去十年中,携带放射性核素的单克隆抗体在癌症治疗(诊断和治疗)中的应用一直处于临床研究中,越来越多具有不同性质(半衰期、发射光谱、粒子或电子)的放射性核素得到评估。然而,到目前为止,临床试验中RIT放射性核素的选择仅限于I-131、Y-90、Lu-177和Re-188、Bi-213和At-211。此外,FDA只批准了两种放射免疫疗法(RIT)用于表达CD20抗原的血液肿瘤的靶向治疗。
RIT依然面临诸多挑战,准确的剂量测定对RIT至关重要;除了放射性核素的固有特性外,抗体的特性对RIT诱导不同的治疗效果也有重要的影响,经过内化的放射性标记抗体比靶向细胞膜的非内化抗体导致更多的DNA双链断裂。
此外,实体癌的RIT应用面临着重大问题,例如由于抗体的渗透性,需要很大的治疗剂量而引起的放射毒性,而抗体工程和放射性核素的新发现正试图克服这些问题,RIT逐渐展现出良好的应用前景。
总结过去10年中已发表的92篇RIT研究的出版物,可以发现67%与非实体肿瘤的RIT有关(62项研究),只有33%与实体肿瘤的RIT研究有关(30项研究),2013-2014年达到高峰。
非实体癌RIT的分类表明,对淋巴瘤(包括滤泡性淋巴瘤、套细胞淋巴瘤、Burkitt淋巴瘤、弥漫性大B细胞淋巴瘤、边缘区淋巴瘤和霍奇金淋巴瘤)的研究非常突出,占调查的92.5%。相比之下,实体瘤的RIT在更多种类的靶点和肿瘤上进行了评估,转移性癌占所有研究的61.9%。
在本世纪头十年中,积极的临床结果导致FDA先后批准了两种放射免疫复合物,即2002年批准的90Y-ibritumomab tiuxetan(Zevalin®,Bayer)和2003年批准的131I-tositumomab(Bexxar®,GSK),这两种药物均基于鼠抗CD20单克隆抗体。二者最初均适用于治疗复发性或难治性(R/R)、低度或滤泡性B细胞非霍奇金淋巴瘤(B-NHL)患者,包括利妥昔单抗难治性滤泡性NHL患者。
这两个药物获得批准后,随后人们进行了RIT大量的临床研究。
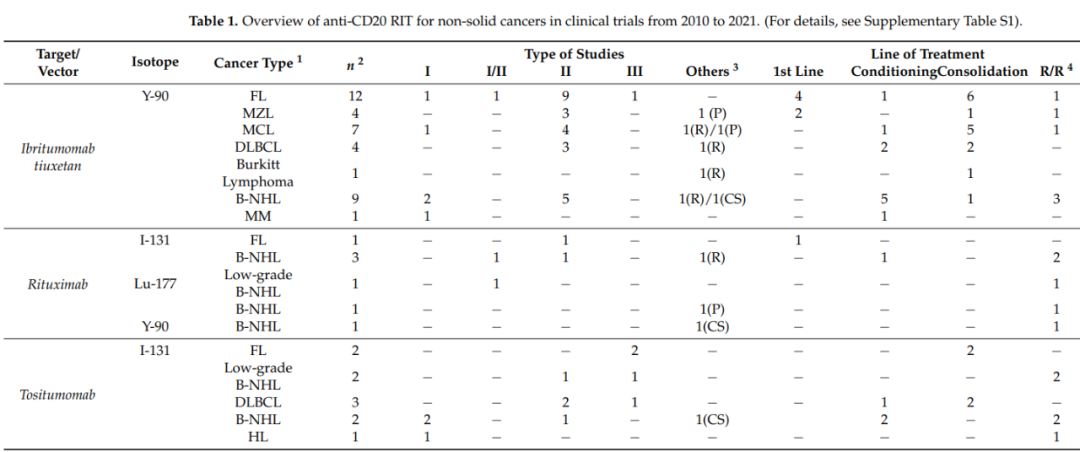
滤泡性淋巴瘤(FL)
在晚期FL的一线治疗中,已证明90Y-ibritumomab tiuxetan和131I-rituximab的疗效和良好耐受性。在FL中,使用90Y-ibritumomabtiuxetan对一线巩固方案进行的第二阶段评估显示了有希望的结果,与无巩固策略相比,无进展生存率(PFS)具有明显优势。然而,使用131I-tositumomab的III期一线巩固研究未能证明临床益处。
关于R/R FL,90Y-ibritumomab tiuxetan的安全性和有效性已在I期研究中得到证明。III期试验用131I-tositumomab评估RIT,然而,该试验提前终止,因为只纳入了14名患者,因此未能得出重要结论。
在边缘区淋巴瘤(MZL)患者中,三项II期研究表明,90Y-ibritumomab tiuxetan在一线治疗或巩固治疗中也有益处。
侵袭性B-NHL
在包括转化的低度B-NHL、DLBCL和MCL在内的侵袭性B-NHL中,评估抗CD20RIT的研究表明,耐受性良好。在大多数研究中,无论侵袭性B-NHL的类型如何,都强调了生存率的显著益处。然而,在MCL中的一项研究中,与涉及利妥昔单抗的方案相比,没有显示生存率的显著改善。
尽管有这些有希望的结果,但针对化疗敏感复发DLBCL患者的III期临床试验中,131I-tositumomab与BEAM或利妥昔单抗进行比较,在PFS和OS方面均未显示任何差异。
其他血液病
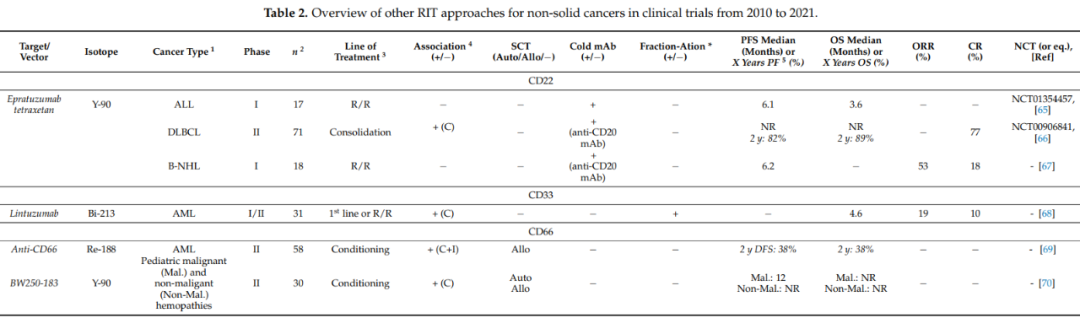
在非B-NHL的血液瘤中,I期抗CD20 RIT显示出良好的疗效和耐受性,包括MM(ORR:73%;CR:23%)和R/R霍奇金淋巴瘤(2例CR/12患者)。此外,还探索了除CD20以外的其他策略,例如,在B-NHL中使用Bi-213的抗CD33单抗,在AML中使用Re-188或Y-90的抗CD66单抗。
尽管放射核素和RIT步骤均有所改进,但实体肿瘤的RIT治疗仍然相当有限。在过去十年中,使用放射核素标记的单克隆抗体治疗实体瘤的临床试验减少了两倍。在所有已发表的RIT临床试验中,缺乏III期试验,约50%为I期试验,约40%为I/II期试验。它们中的大多数人都只评估了RIT的可行性和毒性,因此很难清楚地确定RIT的治疗效果。大多数关于实体瘤RIT的临床试验报告涉及数量有限的已处于转移期且对一线或二线治疗耐药的患者。
血液肿瘤的RIT主要集中于四种不同的抗原靶点(即CD20、CD22、CD33和CD66),到目前为止,实体肿瘤RIT测试了12种不同抗原,每种抗原在临床试验中仅评估一次或两次,因此使得比较不同的研究以确定RIT是否有效变得很困难。
RIT难以成功治疗实体瘤的一个原因是,它依赖于完整单克隆抗体的渗透和较低的剂量。然而,肿瘤血管系统血管渗漏和高度复杂的细胞外基质的存在阻碍了肿瘤细胞接触单克隆抗体。此外,大多数实体瘤中存在的缺氧状态会降低辐射效率。因此,人们开始尝试一些不同的替代方案。
IgG半衰期长是实体瘤RIT治疗的一个主要缺点,因为由于单克隆抗体的缓慢渗透,导致血液毒性和耐药。目前,已经探索了两种主要策略来规避这些问题,这两种策略都是基于改善携带放射性核素的载体的药代动力学。
基于片段的RIT

Fab′
Fab′在临床上最早于1994年就获得了FDA批准,以防止血管成形术中的血栓形成(ReoPro®)。迄今为止,FDA、EMA和中国也批准了几种Fab′片段药物,包括用于癌症治疗,例如Ranibizumab。但是,到目前为止,尚未批准任何RIT。
2002年,在一个非常小的试点研究队列中,对患有结直肠癌的患者进行了I-131标记的CEA靶向二价Fab′片段RIT评估。影像学显示,CEA表达的肿瘤患者存在特异性信号。然而,与其他器官相比,未能显示肿瘤的显著摄取。此外,在三名患者观察到聚集,这与患者血清中测量的CEA抗原量相关。
值得注意的是,Fab′片段也显示出一些诊断潜力。例如,以癌细胞表达的胰腺癌抗原为靶点的99mTc-nofetumimab-merpentan Fab′片段(Verluma®)已于1992年获得FDA批准用于诊断小细胞肺癌,但于2013年停止使用。
2011年, Anascorp®成为FDA批准的第一个F(ab′)2,用于治疗蝎子中毒的临床症状。随后,FDA于2015年批准了Anavip®,用于治疗北美斑蝰中毒的凝血效应。
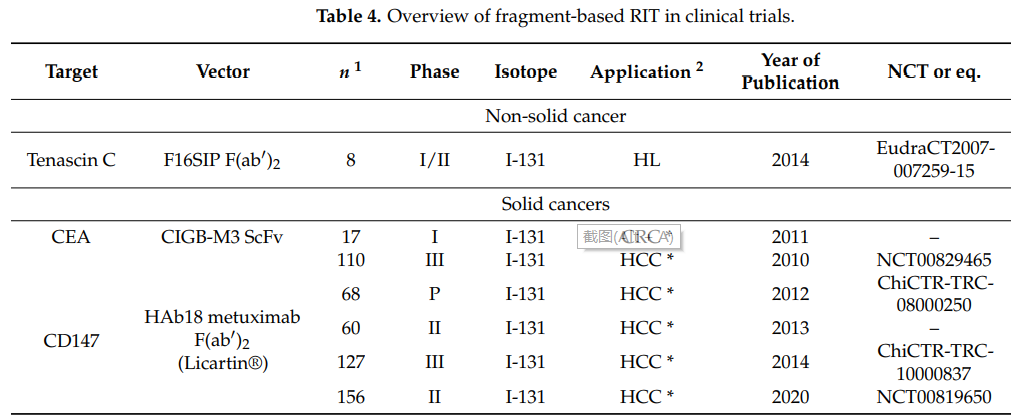
关于RIT,F(ab′)2是临床试验中评估的最常见的片段类型。但自2010年以来,只有两种仍在研究中,CD147用于转移性实体瘤,tenascin C用于霍奇金淋巴瘤。除CD147外,tenascin C和CEA的靶向治疗仍处于早期临床评估阶段(I/II期),仅涉及少量患者。在大多数情况下,使用常规I-131的放射性标记。
几项临床试验已使用131I-metuximab HAb18G/CD147 F(ab′)2(Licartin®)作为术后治疗,或与射频消融联合治疗复发性转移性肝细胞癌(HCC)患者。含metuximab的RIT与轻度至中度血液学/肝脏毒性相关,均≤3级;此外,甲状腺功能没有损害,在两个周期的治疗后也没有明显的人类抗鼠抗体(HAMA)阳性。在最近的研究中,中位OS在20到60个月之间,治疗组的5年PFS约为43.4%,而对照组为21.7%。
ScFv
在肿瘤学中,单链抗体片段已广泛应用于嵌合抗原受体(CAR)T细胞免疫治疗中。在RIT临床试验中,唯一一项描述使用放射性标记单链抗体的研究是在2011年的一项I期试验,该试验使用了131I-CIGB-M3三价单链抗体,靶向CEA。在17名患者的评估中,具有较低的非靶向毒性,且HAMA反应较低。尽管显示出不错的药代动力学结果和剂量测定,但迄今为止尚未进行临床开发。
预靶向放射免疫治疗(PRIT)
提高清除率和降低靶外毒性的另一个潜在策略是通过所谓的预靶向方法延迟其中单克隆抗体的放射性核素给药,延迟给药数小时至数天。

该方法首先给予完整的抗体或片段偶联物与靶点充分结合,通常在给予放射性成分之前数小时至数天,以有时间积聚到肿瘤中,放射性配基与和单克隆抗体偶联物具有高度特异性的有效载荷相联。为了获得快速反应,两种配基之间需要高亲和力。由于放射性配体体积小,在血液中生物分布快,半衰期短,因此,PRIT对于健康组织具有较低的非靶向毒性。
在过去的30年里,已经制定了不同的PRIT策略。最古老的策略涉及生物素和链霉亲和素之间的高亲和力。尽管在临床前试验中取得了不错的结果,但临床I/II期试验证明了链霉亲和素的免疫原性以及与内源性生物素的非靶向结合活性。
另一种基于双特异性或多特异性抗体或片段的PRIT策略很快被开发出来。2012年,对一种嵌合体双特异性人/小鼠(hMN-14×m734)F(ab′)2进行了II期研究,该嵌合体是一种用I-131标记的抗CEA×抗DTPA,用于治疗甲状腺髓样癌患者。bsAbs和131I-DTPA之间的给药延迟4至6天,结果表明,大多数患者对PRIT耐受性良好,此外,PRIT的疗效在76%的患者中被证明可以控制疾病,中位PFS为13.6个月,中位OS为43.9个月。最近,嵌合(hMN-14×m734)F(ab′)2在转移性结直肠癌的治疗中也显示出有趣希望的结果。
尽管FDA已经批准了两种RIT药物,但是过去十年未能扩大抗CD20 RIT的适应症,临床进行的RIT试验也逐年减少,人们对血液系统恶性肿瘤这种治疗策略的兴趣正在下降。此外,在实体肿瘤中,目前还没有经FDA或EMA验证的RIT。
然而,值得注意的是,实体瘤中RIT的数量显著增加,最近达到峰值,占正在进行的RIT临床试验的50%以上。大量新发现的靶点/抗体与有效的放射性核素的结合表明RIT在实体瘤,特别是转移性恶性肿瘤中有着新的应用前景。此外,最近在抗体片段生物偶联和预定向策略方面的进展,让我们看到了在未来十年内提高RIT疗效和扩大实体瘤应用的希望。
参考文献:
1.Radioimmunotherapy in Oncology: Overview of the Last Decade Clinical Trials. Cancers (Basel). 2021 Nov; 13(21): 5570.
公众号内回复“肿瘤免疫”或扫描下方图片中的二维码免费下载《小药说药肿瘤免疫全集》的PDF格式电子书!

公众号已建立“小药说药专业交流群”微信行业交流群以及读者交流群,扫描下方小编二维码加入,入行业群请主动告知姓名、工作单位和职务。





































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论