本文作者 | 郭维;郭允乐
本文来源 | 维渡纵横
作者微信 | Yunle_G
目 录
[向上滑动阅览]
TCR疗法起源于1986年,巴塞尔免疫研究所Michael Steinmetz博士首次将一个T细胞的TCR基因转移到另一个T细胞中,从而赋予第二个T细胞相同的抗原特异性。2002年,Rosenberg团队率先从黑色素瘤组织中分离出肿瘤浸润淋巴细胞(Tumor infiltrating lymphocyte,TIL),体外扩增回输后特异性杀伤黑色素瘤细胞,但由于TIL的提取扩增工艺等难点,科学家开始探究能否在正常外周血淋巴细胞(Peripheral blood lymphocyte,PBL)上导入已知的抗原特异性TCR基因进行治疗。2004年,Rosenberg团队首次将靶向MART-1的自体TCR-T进行回输,参与试验的17名患者中有2人出现了肿瘤缩小,证明了基因改造TCR用于肿瘤治疗的可行性(Science 2006, 314, 126),拉开了TCR疗法的帷幕。
TCR疗法已经演变成基于peptide-MHC(pMHC)识别为主的“TCR-T细胞疗法”、“TCR蛋白药”、“TCR类抗体药”三种疗法,其中,TCR-T细胞疗法领域于2024年8月1日获批一款上市,TCR蛋白药领域于2022年1月27日获批一款上市。
Vol.1
TCR的结构和工程化
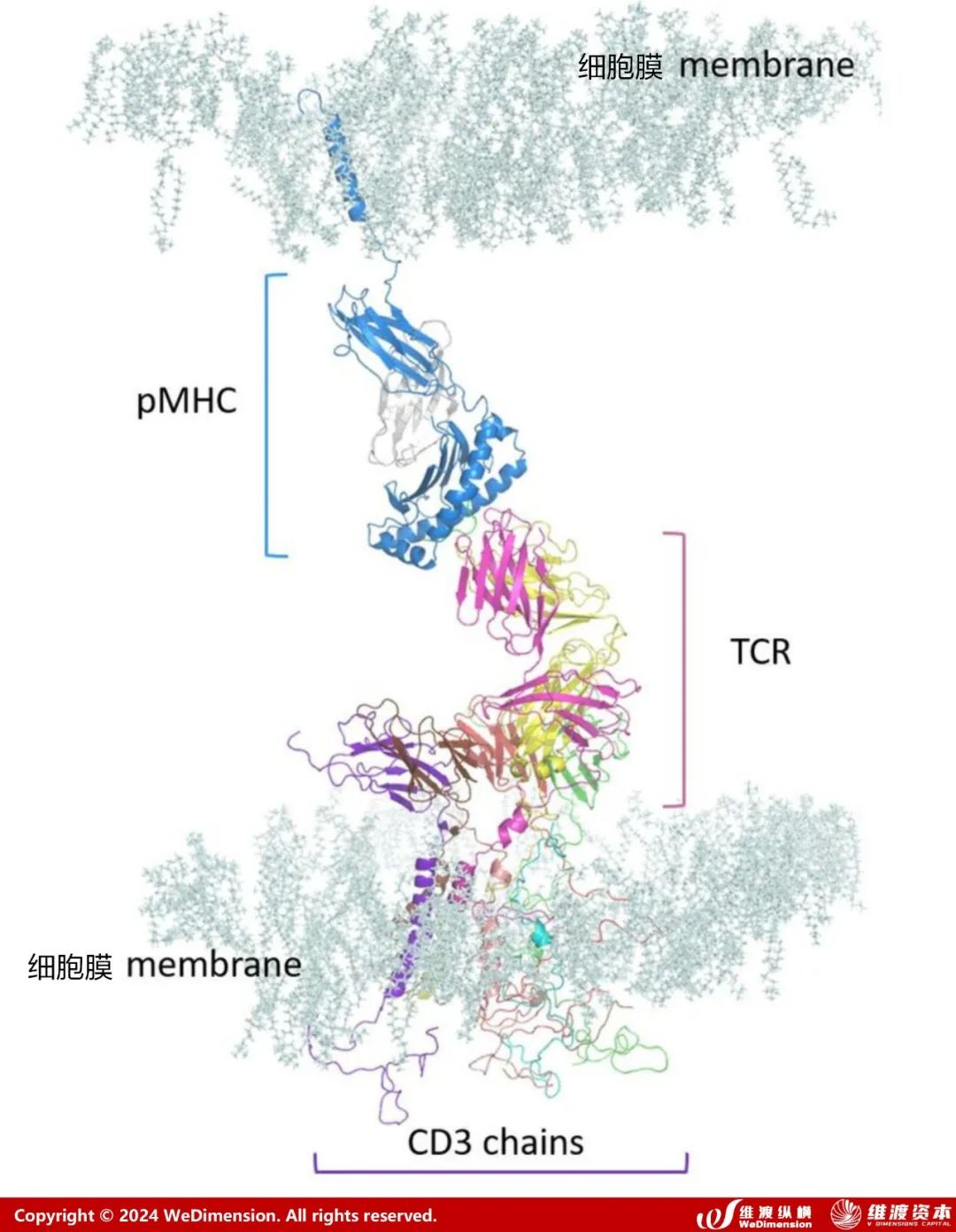
TCR是T细胞表面的特异性受体,以非共价键与CD3结合,形成TCR-CD3复合物,通过识别并结合MHC呈递的抗原,从而激活T细胞,促进T细胞的分裂与分化。MHC(Major Histocompatibility Complex,MHC)即主要组织相容性复合体,是一组编码动物主要组织相容性抗原的基因群的统称,人类的MHC被称为HLA,可将细胞内蛋白分解后的片段呈现在细胞表面,TCR通过与MHC相结合来判断靶细胞是否正常,如果T细胞发现MHC呈现出的蛋白片段是变异的,就会杀死该靶细胞。
1.1 TCR功能和信号转导
MHC
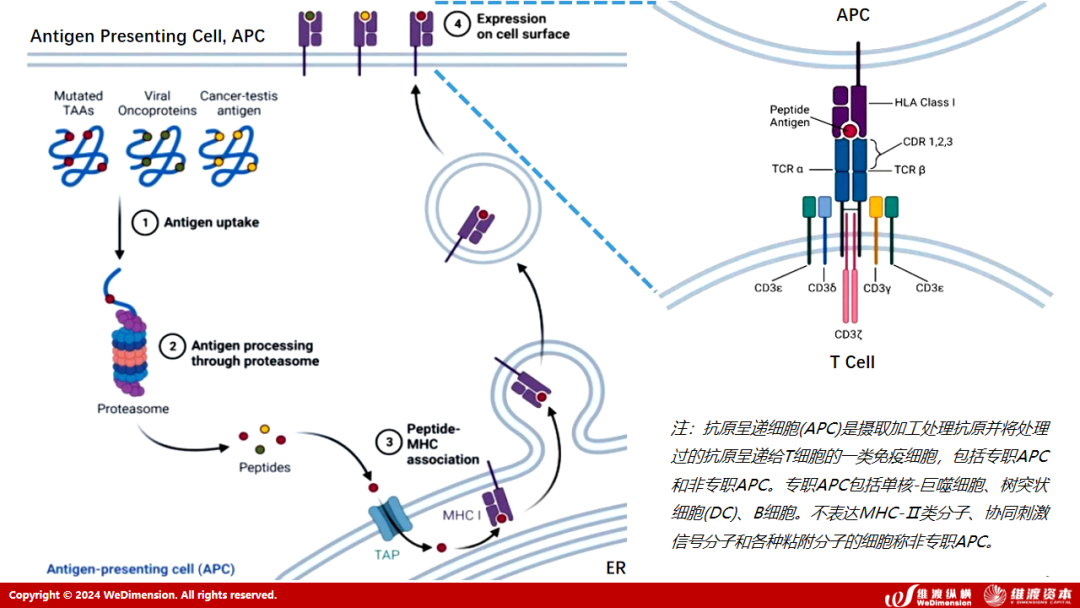
MHCⅠ位于一般细胞表面上,提供一般细胞内部的特殊状况。比如该细胞遭受病毒感染,则将病毒外膜碎片之氨基酸链透过MHC提示在细胞外侧,可以供CD8+ T细胞等辨识以进行杀伤。
MHC Ⅱ大多位于抗原呈递细胞(APC)上,如巨噬细胞、DC等,提供细胞外部的状况,如组织中有细菌侵入,则巨噬细胞进行吞噬后,把细菌碎片利用MHC提供给辅助T细胞,启动免疫反应。
MHC Ⅲ 主要编码补体成分、肿瘤坏死因子(TNF)、热休克蛋白70(HSP70)、21羟化酶基因(CYP21A、CYP21B)等。
HLA是人类多态性最丰富的遗传系统,位于第6号染色体短臂6P21.31区,长3600kb。1999年已完成全部序列分析及基因定位,在此区域内共确认了224个基因座位,其中128个为功能性基因,其中39.8%和免疫功能相关。HLA基因根据其编码分子的分布与功能不同分为3个区,即Ⅰ类基因区,Ⅱ类基因区,Ⅲ类基因区。

1.2 TCR的结构组成

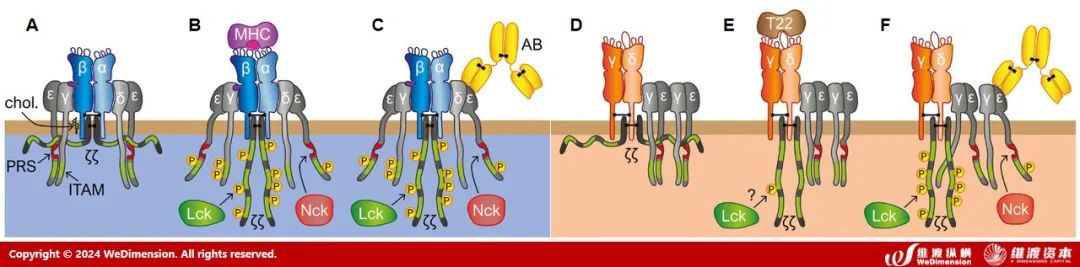
αβTCR和γδTCR的配体识别涉及α、β、γ、δ链的CDR1、CDR2和CDR3,CDR3是配体结合TCR链中变化最大的区域。αβTCR的激活配体为pMHC,通常CD4+ T细胞识别MHC II类上呈递的肽,CD8+ T细胞识别MHC I类上呈递的肽。相反,大多数γδTCR无法识别MHC分子,其配体是多种多样的,缺乏共同性质,不像αβ TCR的配体那样遵循一般原则,包括脂质呈递、应激诱导的MHC样分子、其他非MHC细胞表面分子、可溶性蛋白质、小肽,导致γδTCR活化的分子机制复杂,这与大多数γδT细胞缺乏CD4和CD8表达高度相关。
CD4+/CD8+
αβTCR识别pMHC可能是使CD4/CD8偶联Lck靠近αβTCR所必需的,以启动信号转导。由于γδT细胞缺乏CD4和CD8,γδTCR可以形成大量游离Lck池,以诱导对任何抗原的反应信号转导。这表明,如果Lck未被CD4或CD8隔离,则可以正向选择识别除pMHC之外的抗原的αβT细胞。
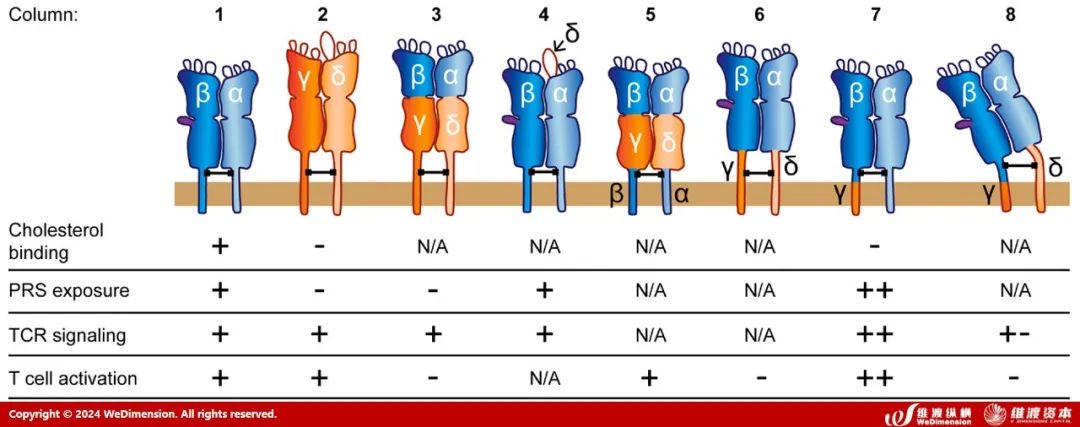
来自αβTCR的区域以蓝色表示,来自γδTCR的区域以橙色表示。第1、3、5、6、7、8列中的TCR的天然配体是pMHC,而第2和第4列中的TCR天然配体是T22 (图5、图4)。这为TCR工程化提供了一定的设计基础。
1.3 工程化TCR技术
1.3.1
ImmTAC
ImmTACs (免疫激动单克隆T细胞受体) 是使用工程化、可溶性、亲和增强的单克隆TCRs (mTCRs) 设计的。ImmTACs是一种新型的双特异性生物大分子,基本上是融合蛋白,结合了工程化的TCR靶向系统和单链抗体片段 (scFv) 效应器功能。Immunocore公司的核心技术就是ImmTACs,由工程化改造的TCR以及抗CD3的scFv组成,改造后的TCR显著提高亲和力,比抗原抗体亲和力高出9倍,特异性识别并结合肿瘤细胞表面的pHLA,抗CD3的scFv则能够吸引、招募T细胞至肿瘤细胞周围并激活T细胞发挥肿瘤杀伤作用。2022年美国和欧盟分别批准了Immunocore公司的全球首个TCR蛋白药物tebentafusp,用于治疗转移性葡萄膜黑色素瘤。2023年该药物销售额高达2.387亿美元(折合人民币约17.37亿元),其中1.698亿美元来自美国,6760万美元来自欧洲,130万美元来自其它地区。

图7. 免疫激动单克隆T细胞受体(ImmTAC)
在ImmTACs的构建中, TCR能够识别来自人类白细胞抗原 (HLA) 呈递的细胞内靶点的肽。ImmTAC通过特异性靶向肿瘤细胞表面的HLA-肽复合物,并通过scFv抗体片段与CD3的相互作用促进T细胞介导的效应器功能。ImmTAC还以剂量依赖性方式激活CD8+ T细胞,并能有效地重定向和激活效应和记忆CD8+和CD4+细胞。ImmTAC通过分泌多种细胞因子表现出多功能反应,如TNF-α、IFN-γ、IL-6、MIP1α-β和IFN-γ诱导蛋白10。
选择合适的"靶抗原"是ImmTACs的关键,质谱技术、pMHC多聚体技术有助于识别合适的抗原。值得注意的是,TCR工程化T细胞也表现出非预期靶向毒性。总的来说,ImmTACs已被证明能增强TCR-T细胞的抗肿瘤反应,但其安全性有待进一步研究。
1.3.2
TCR mimic
除了ImmTACs,另一类双特异性T细胞结合蛋白称为TCR mimic(TCRm),使用两个抗体来源的单链抗体,通过多肽接头共价连接。一个scFv与癌细胞上的pHLA分子表位结合,而另一个scFv与T细胞上CD3复合体的成员结合。使用单链抗体作为抗原结合域的一个优点是,它们可以使用高通量技术如噬菌体和酵母展示文库从头产生。TCR mimic很小(~55 kDa),使靶细胞和T细胞之间能够密切相互作用。TCR mimic的形式更多样,包括TCRm-CD3双特异性抗体形式、TCRm-ADC形式、CAR形式 [Front Oncol. 2022,12:1027548]。
TCR和TCR mimic的功能、结构和分子动力学比较表明,这两种抗原受体以不同的方式结合他们的靶标,这些差异部分归因于抗体的可变区与TCRs的取向不同。TCR通常结合pHLA复合体的广泛区域,以肽的核心为中心;许多TCR mimic偏向于HLA结合肽的末端或HLA螺旋。

图8. TCRmimic
1.3.3
TRuC
TRuC (T细胞受体融合结构) 是一种与T细胞受体亚单位融合的抗体结合域,设计用于有效识别肿瘤表面抗原。TRuCs由靶向肿瘤相关抗原的特异性抗体融合到5个TCR亚基(TCRα、TCRβ、CD3ϵ、CD3γ和CD3δ)的胞外N-末端组成,为工程化T细胞提供了新的靶向特异性和HLA非依赖性靶细胞清除能力,可被相应的靶细胞激活。
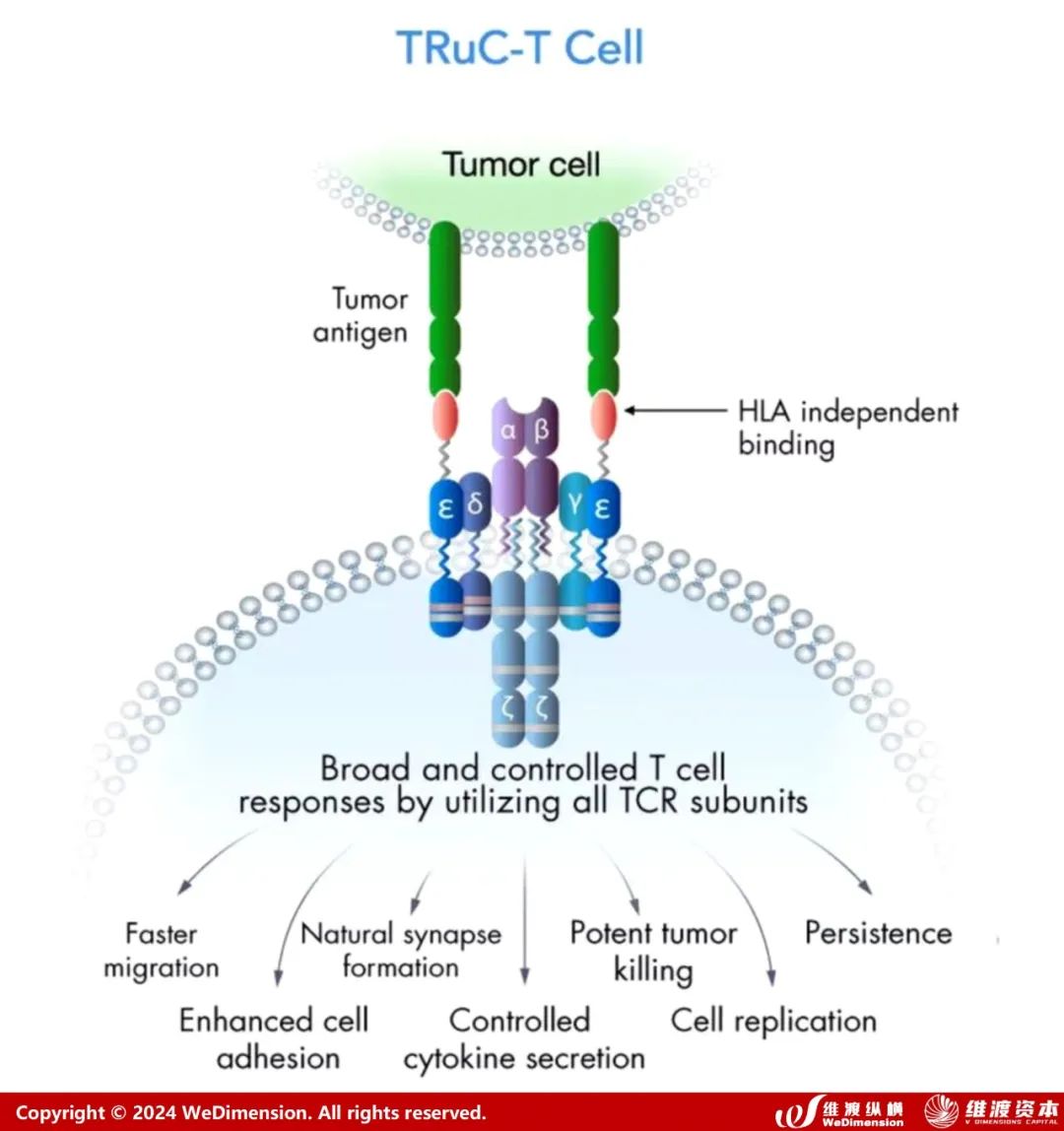
图9. T细胞受体融合结构 (TRuC)
与第二代CAR-T细胞相比,该方法显示出更好的抗肿瘤效果。此外,TRuCs支配TCR复合体的全部信号机制,而CARs仅利用分离的CD3ζ胞内段的有限信号。
1.3.4
TAC
TAC (T细胞抗原偶联剂) 是另一个工程化TCR细胞,以非MHC依赖性方式诱导更有效的抗肿瘤反应并降低毒性。TAC嵌合蛋白通过与CD3结构域的结合,从而形成TCR/CD3复合物并获得更多的T细胞应答。
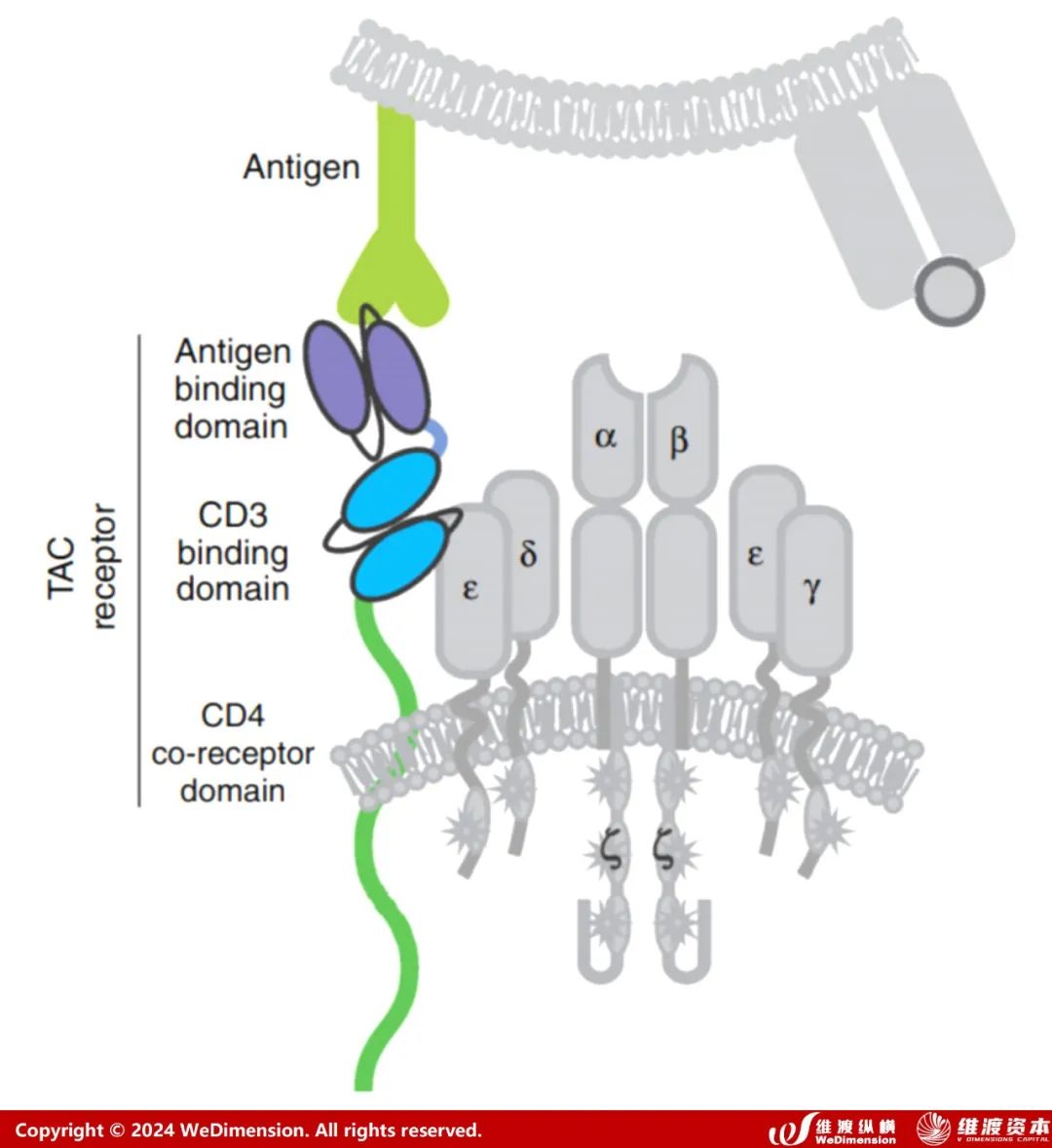
图10. T细胞抗原偶联剂 (TAC)
TAC受体的活性与CD3结合域的选择密切相关。例如,与UCHT1相比,来自OKT3(muromonab-CD3)的单链抗体具有较低的细胞因子产生和细胞毒性,这可能导致实质上不同的功能结果。与第二代CARs相比,TAC基因工程化的T细胞不仅有利于过继后在实体瘤的更大浸润,而且减少了T细胞在表达抗原的健康组织中的扩增和肿瘤外毒性。
1.3.5
STAR/HIT
合成TCR抗原受体(STAR)/HLA非依赖性TCR(HIT)是一种非HLA限制性受体,是一种异源二聚体,它用抗体的VH/VL结构域取代TCR的可变区(图11g)。由于TCR可变区与VH/VL结构域具有相似的大小和三维折叠,可以互换替换。通过保留TCR恒定域,STAR/HIT受体重新招募CD3信号分子的完整复合体。在抗原刺激后,STAR/HIT受体诱导TCR-like信号,使对抗原位点密度较低的靶细胞的反应性增强。
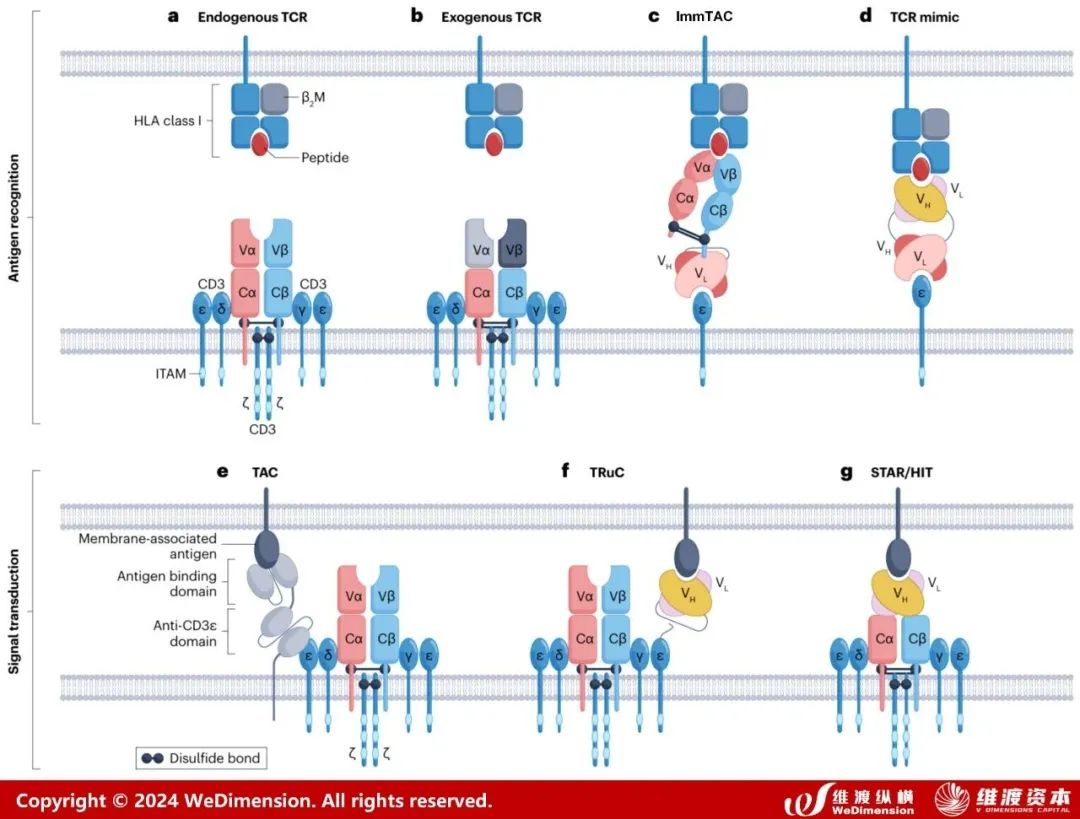
Vol.2
TCR的抗原筛选技术
近年来,随着高通量测序技术、质谱流式细胞技术、计算生物学的快速发展,研究人员开发了多种TCR抗原筛选技术用于解析TCR及其特异性识别的抗原信息。
2.1 抗原筛选靶向TCR
2.1.1
细胞杀伤/因子筛选法
酶联免疫斑点检测 (ELISPOT技术) 通过抗体检测T细胞受到抗原刺激后分泌的细胞因子的变化来评估TCR的抗原反应性,该方法操作简单,灵敏度高,但计数误差、抗体特异性等对筛选结构影响较大。
铬释放法是一种细胞毒测定方法,将T细胞与放射性同位素51Cr标记的靶细胞共培养,检测上清中靶细胞裂解后所释放的51Cr放射脉冲数,量化T细胞对靶细胞的特异性杀伤。该法51Cr半衰期较短,难以多次测定。
NFAT-荧光素酶筛选技术是在T细胞中表达活化T细胞核因子(NFAT)-荧光素酶报告基因,靶细胞与T细胞共培养时,抗原与特异性TCR的结合启动NFAT信号通路,激活下游荧光素酶的表达,荧光素酶催化底物的氧化反应,产生荧光,通过检测荧光强度来测定T细胞中荧光素酶活性,以此评估T细胞的抗原特异性。该法灵敏度高、结果重复性好、易于检测且相对安全。
2.1.2
基于pMHC筛选法
基于TCR-pMHC识别特异性,一系列TCR抗原筛选技术被开发出来,由于可溶性pMHC单体与TCR的亲和力较弱,通过pMHC多聚化可增强pMHC与TCR之间的结合稳定性,其中pMHC四聚体是由四个pMHC单体分子通过链霉亲和素聚合形成可溶性的四聚体,已成为鉴定抗原特异性T细胞的“金标准”,具有较高的特异性和敏感性。研究者们开发了多种携带不同标记、标签的pMHC多聚体技术用于高通量抗原特异性TCR的筛选,如荧光标记的pMHC多聚体、重金属离子标记的pMHC多聚体、DNA条形码标记的pMHC多聚体,其中DNA条形码标记的pMHC多聚体可实现高通量TCR抗原筛选。pMHC四聚体已广泛应用于疫苗研发、细胞治疗研究等,并具备诊断试剂开发潜能。但这一技术需要预先确定的抗原肽信息,需要合成多肽文库和pMHC多聚体组装。
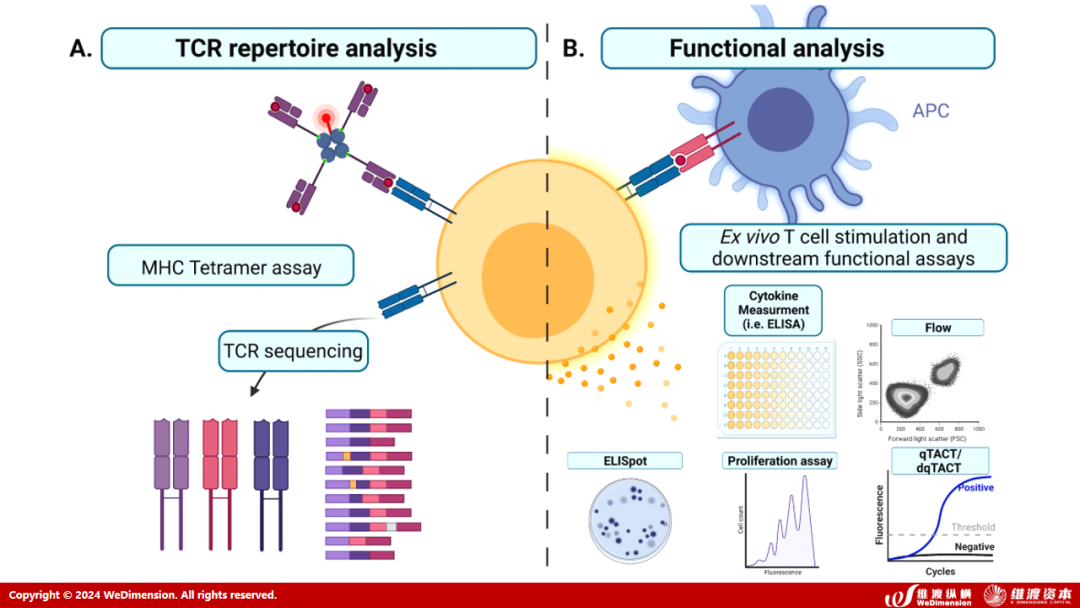
2.1.3
微流控和单细胞测序筛选法
结合液滴微流控与单细胞测序技术,为TCR抗原筛选提供了新的策略和方向,同时获得了抗原特异性TCR的序列信息。微流控系统生成的微液滴可作为细胞反应容器,每个微液滴都是独立的反应单元,将T细胞与靶细胞包裹其中,避免细胞间相互干扰,独立地进行相互作用,再通过单细胞测序获得序列信息,大大提高了检测的灵敏度和TCR筛选通量。
2.2 TCR定向筛选抗原
2.3 库对库双向筛选
2.3.1
基于慢病毒感染的筛选技术
研究人员开发了一种携带荧光蛋白基因的突变型VSV-G假型慢病毒感染体系,使其失去与细胞表面低密度脂蛋白受体结合的能力,无法感染靶细胞,但保留了膜融合能力。通过在体外病毒生产过程中共表达特定表面结合蛋白的方式,将外源蛋白展示在病毒表面,成为以外源蛋白承担受体结合作用的病毒抗原展示系统。改造后的慢病毒通过其表面展示的靶蛋白与细胞膜上受体相互作用实现细胞特异性感染。将多种携带不同pMHC的突变型VSV-G病毒混合后,感染表达TCR文库的T细胞群,通过流式细胞术分离被感染的细胞并进行测序,同时获得配对的TCR和抗原的序列信息。
研究者进一步将“荧光蛋白”与“病毒结构蛋白”相融合,使得编码荧光蛋白的基因无需整合到细胞基因组中,两小时即可在被感染的细胞表面检测到荧光蛋白,缩短了筛选时间。
该法解决了仅能通过单一抗原或单一TCR筛选的局限性,实现了TCR文库与抗原文库的双向筛选。
2.3.2
YAMTAD筛选技术
酵母抗原展示系统具有较大的展示规模和筛选通量,可与流式细胞术有效结合。研究人员建立了酵母凝集介导的TCR抗原发现系统(YAMTAD)。在MATa酵母和MATα酵母中分别转入TCR-CDR3突变体-报告基因与pMHC突变体基因,同时转入交配启动的荧光报告子。将表达同源TCR与pMHC的酵母细胞共培养,经流式细胞术筛选双荧光的二倍体,通过NGS获得TCR与抗原的基因序列。该法具有更高的展示效率,并可达到10E8的筛选规模。YAMTAD系统对低亲和力相互作用的灵敏度较低,可能会遗漏部分TCR与pMHC的配对信息。
Vol.3
TCR疗法的靶点分布
上述多种TCR抗原筛选技术的升级将TCR疗法靶点选择范围进行了扩容,它不仅可以识别细胞表面抗原,同时也可以识别一些抗体、小分子难以靶向的细胞内抗原。
选择理想的抗原是提高抗肿瘤效率和降低相关毒性的关键,肿瘤特异性、免疫原性是选择抗原的首要考虑因素。人类肿瘤抗原主要分为肿瘤相关抗原(tumor-associated antigen,TAA)和肿瘤特异性抗原(tumor-specific antigen,TSA)两大类。表面抗原通常是TAA,正常组织也可以表达。而近90%的实体瘤靶向依赖于TSA。尽管TCR-T可以靶向所有肿瘤抗原,但迄今为止已确定的有足够安全性和有效性的靶点数量仍然有限,通常选择在肿瘤中高表达但在正常组织中低表达的靶抗原来限制潜在的脱靶效应,导致当下可用的靶点有限,主要集中在NY-ESO-1、MAGE、KRAS、AFP、HBV、HPV、PRAME、WT1、EBV等已被证实的抗原进行开发。
维渡纵横从公开信息总结TCR疗法的靶点分布统计如下表所示。


Vol.4
TCR疗法的药物类型
随着研究的不断深入,TCR疗法呈现出不同的药物类型,包括TCR-T细胞疗法、TCR蛋白药、类TCR抗体药物,并逐渐成为国内外药企的热门布局方向。
4.1 TCR-T细胞疗法
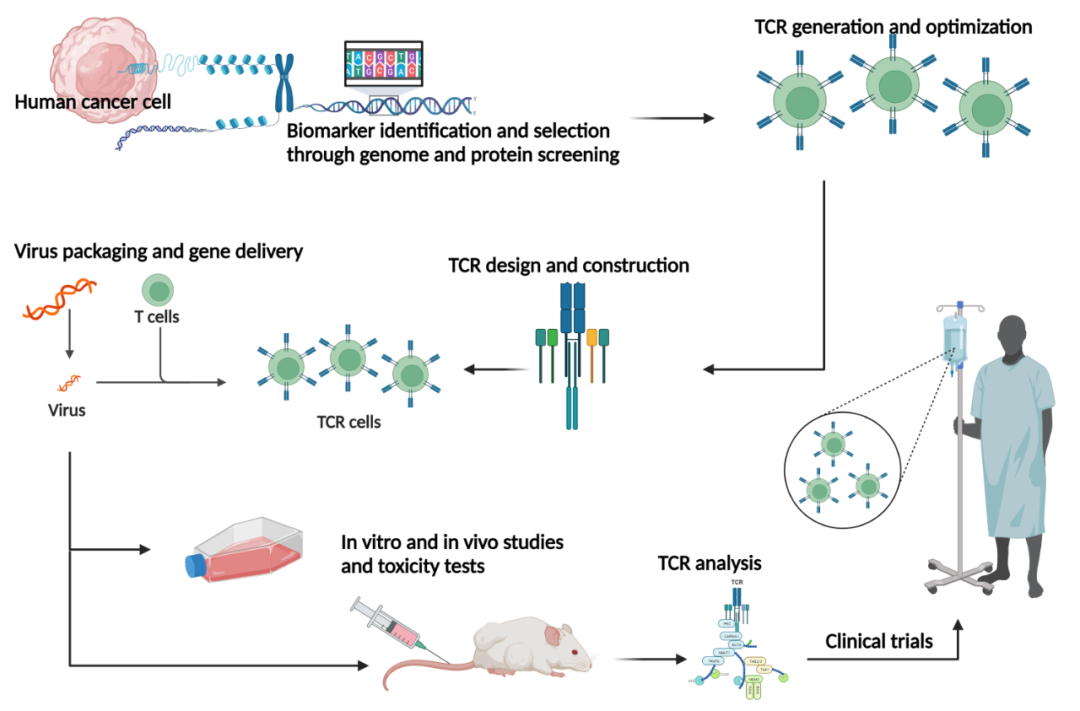
图13. TCR-T治疗流程
4.2 TCR蛋白药物


2022年1月27日FDA批准的全球第一款治疗不可切除或转移性葡萄膜黑色素瘤疗法Kimmtrak(tebentafusp)就是在天然的TCR上进行亲和力优化,通过识别靶抗原gp100-pHLA并结合T细胞上的CD3募集T细胞,来实现肿瘤杀伤作用,打破了眼睛来源黑色素瘤近40年的新药空窗期。

4.3 TCR类抗体药物
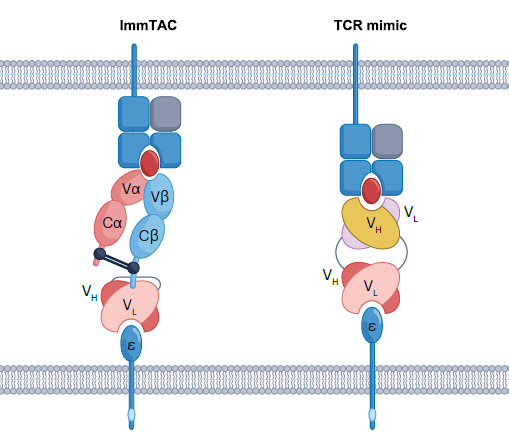
图18. TCR蛋白和TCR类抗体的结构差异
Vol.5
TCR疗法临床进展
5.1 海外TCR疗法临床进展

TCR疗法的疾病领域主要聚焦在肿瘤领域、罕见病领域、血液领域。已经获批适应症分别为滑膜肉瘤、葡萄膜黑色素瘤;其余适应症处于临床试验阶段,包括非小细胞肺癌、黑色素瘤、卵巢癌、HPV相关癌症、多发性骨髓瘤、肝细胞癌、肛门癌、宫颈癌、骨髓增生异常综合征、滑膜肉瘤、急性髓系白血病、急性淋巴细胞白血病、胃癌、结直肠癌、黏液样/圆细胞型脂肪肉瘤、胰腺癌、尿路上皮癌、乳腺癌、头颈癌、食管癌、头颈部鳞状细胞癌、子宫内膜癌等。
维渡纵横根据公开信息整理海外进入注册制临床试验的产品如下表所示。


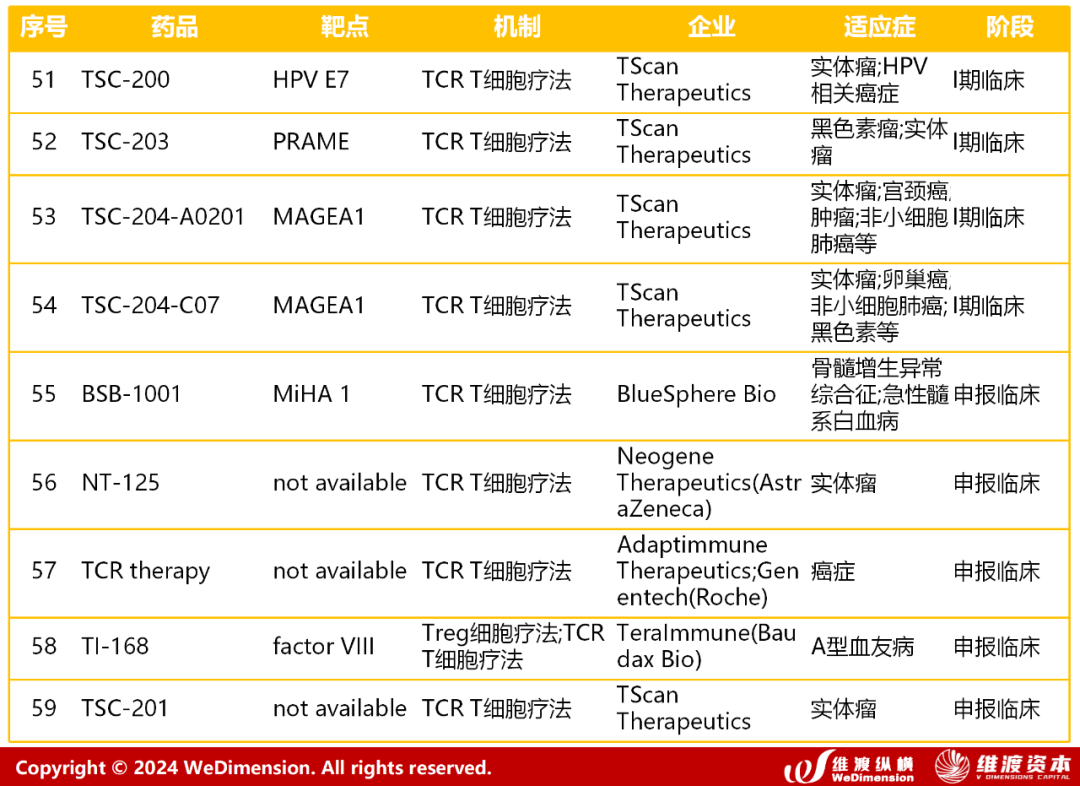
5.2 国内TCR疗法临床进展
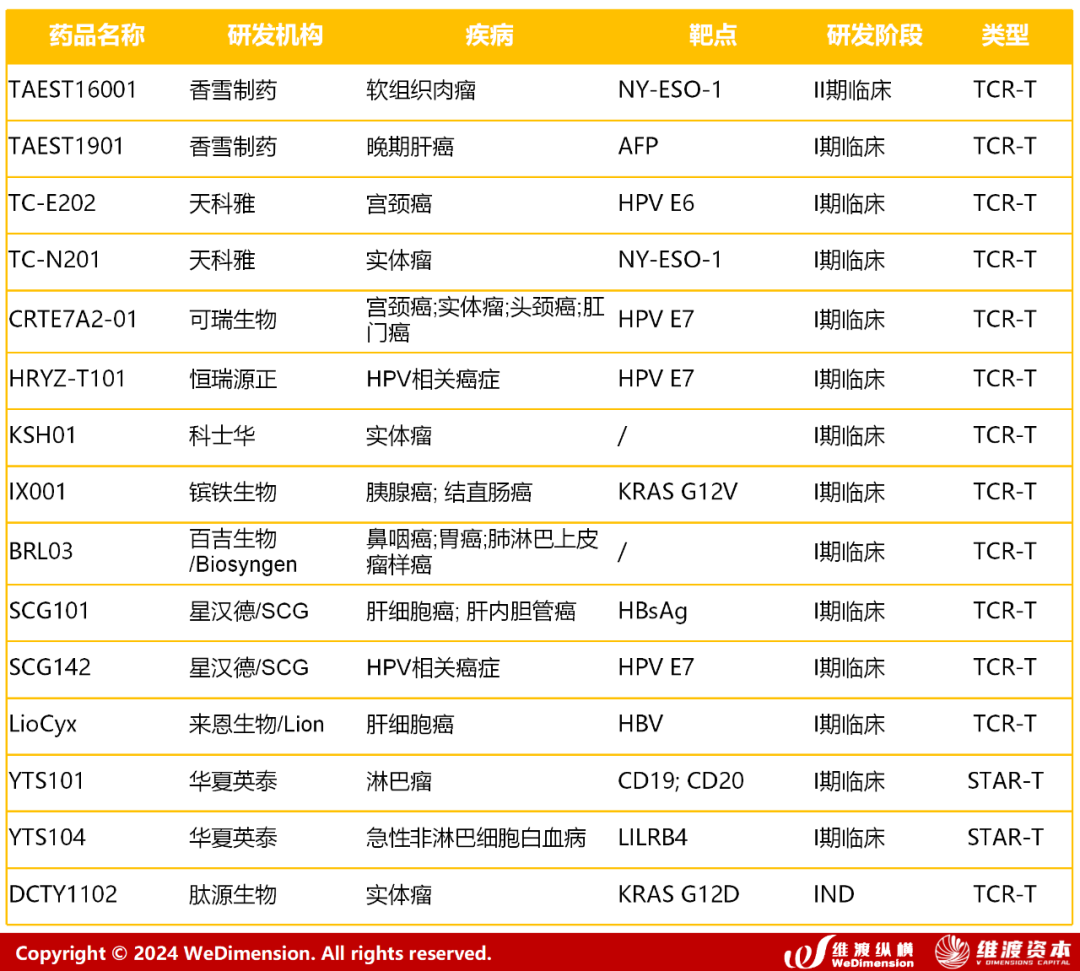
Vol.6
TCR疗法生产流程
6.1 TCR-T生产工艺流程

具体步骤如下:
① 筛选和确定肿瘤上合适的特异性抗原,以及对抗原有高度特异性的TCR αβ链序列;
② 从患者体内分离出T细胞;
③ 将TCRαβ序列包入病毒基因组,构建病毒载体;
④ 病毒转染T细胞,将目标TCR序列引入T细胞,从而获得特异性TCR-T细胞;
⑤ TCR-T细胞体外培养、大量扩增;
TCR-T产品的上游研发工作是"筛选"及"亲和力优化"针对肿瘤抗原特异性的TCR,该TCR分子决定了TCR-T细胞安全有效的抗肿瘤能力;下游的TCR-T"细胞制备"和"质量控制"则决定了TCR-T终产品质量。
TCR-T制备工艺与质量研究仍处于起步阶段,国内工业界仍没有成熟的体系可以借鉴套用。建立完整的工艺及质控体系是保障TCR-T产品的有效性、稳定性和一致性的关键。TCR-T产品在生产原材料、生产工艺、过程控制、辅料、包装容器、稳定性等方面与CAR-T细胞产品有相似之处,在质量评价方面可参考相关的指导原则和考虑要点及国外如美国FDA和欧盟EMA先进疗法相关的指导原则。
6.2 TCR蛋白药生产流程
TCR蛋白药弥补了TCR-T细胞治疗的一些局限性。首先,自体TCR-T往往成本高昂,制备复杂,部分患者不适宜单采,导致这一方法可及性较差。TCR蛋白药在成本、生产、可及性、PK特性、安全性方面都更具有优势,并且能够应用到更多疾病领域。
TCR蛋白药的开发需要极高的"TCR亲和力优化",高技术门槛限制了大部分公司进入该领域,全球只有少数几家公司如Immunocore、Immatics、可瑞生物具有TCR蛋白药管线。可瑞生物长期致力于高通量天然TCR筛选平台和SMART-TCR亲和力优化体系,是国内最早开展和进展最快的TCR蛋白药生物科技公司。
TCR蛋白药开发的核心技术是TCR亲和力优化,然后经由工程化改造的高亲和力及特异性的TCR和抗CD3的scFv组成双特异性融合蛋白分子,通过重组蛋白生产工艺即可完成,具体开发流程如下:
① 利用超灵敏质谱等手段确定样本库中最佳的肽-人类白细胞抗原(pHLA);
② 利用专有的亲和力优化技术筛选更高特异性的TCR;
③ 利用TCR质量评估平台确保只有最佳的TCR才会进入到亲和力优化步骤;
④ 在有六个pHLA结合区域的数十亿个离散突变的TCR中利用专有的筛选技术如噬菌体展示技术等筛选亲和力高达百万倍同时特异性高的TCR;
⑤ 利用体外毒理性评价平台评估分子潜在脱靶结合或交叉反应性,以确定治疗窗口,并提供首次入人体的起始剂量;
⑥ 利用基于大肠杆菌等微生物发酵制造平台规模化生产重组蛋白,商业化推出TCR蛋白药产品。
Vol.7
产 业 链 分 析
7.1 TCR-T细胞药产业链
7.1.1
上游分析
上游包括细胞资源库、仪器设备、试剂耗材、模式动物,是行业的基石,为中下游提供了必要的资源和支持。
细胞资源库的建立是免疫细胞治疗的第一步。这些库存储了大量的免疫细胞,可以在需要时迅速提供。目前,中国已有多家企业如中源协和、南京新百等在全国范围内建立了细胞资源库,为研究和治疗提供了强大的支持。
仪器设备、试剂耗材和模式动物是研究的另一大支柱。细胞治疗中使用的仪器设备和试剂耗材大多依赖进口,如生物反应器、细胞分离设备、检测设备、培养基等,国际知名品牌如通用、贝克曼、赛默飞、思拓凡、安捷伦等都在中国市场有着广泛的业务。 模式动物和类器官研究目前正实现国产化替代,国内企业包括昭衍新药、药康生物、大橡科技等。
7.1.2
中游分析
免疫细胞治疗的中游是行业的核心,直接决定了治疗的效果和前景。中国已经在全球免疫细胞治疗研究领域中占据了重要的位置,处于第一梯队。特别是基于CAR-T、TCR-T、TIL、CAR-NK、CAR-M等技术的研究,中国在这一领域的研究已经达到了国际先进水平。
CAR-T领先企业包括传奇生物、科济生物、驯鹿生物、恒润达生、合源生物、艺妙神州等;
TCR-T领先企业包括香雪制药、可瑞生物、天科雅、恒瑞源正、科士华、镔铁生物、肽源生物(鼎成肽源)、呈源生物等;
TIL领先企业包括沙砾生物、君赛生物、西比曼、卡替医疗、劲风生物、智瓴生物、循生生物、蓝马医疗、华赛伯曼等;
CAR-NK/NK领先企业包括英百瑞、先博生物、国健呈诺、达博生物、晨泰医药、中盛溯源、启函生物、星奕昂、恒润达生、传奇生物、恩瑞恺诺、贝斯昂科、恩凯赛药、优凯瑞等;
CAR-M领先企业包括赛元生物、元迈细胞、鲲石生物、巨世康济等。
7.1.3
下游分析
免疫细胞治疗的下游是行业的终端即临床应用,直接关系到治疗的普及和应用。截止目前,中国市场只有CAR-T产品获批上市,其他领域尚未获批。随着政策的支持和医疗机构的参与,免疫细胞治疗在中国的临床应用也将得到更广泛的推广,不仅为患者带来了新的治疗机会,也为整个行业带来了巨大的市场潜力。
7.2 TCR蛋白/TCRm产业链
Vol.8
市场规模和商业化
8.1 市场规模
8.2 TCR疗法商业化
首个获批的TCR疗法是Immunocore公司的TCR蛋白药Tebentafusp,商品名为Kimmtrak,于2022年1月获批上市,是一款靶向gp100的TCR与靶向CD3的scFv的融合蛋白,在III期临床数据中打败了K药和CTLA-4单抗,获FDA批准用于治疗HLA-A*02:01基因型、转移性或不可切除的葡萄膜黑色素瘤,美国定价为40万美元/年。2022年首年销额达1.41亿美元,2023年销售额达2.49亿美元;2024年第一季度净销售额达到7034.2万美元,同比增长36%,在获批的38个国家和地区中,美国净销售额占比71.1%,欧洲占比26.9%,欧美销售合计占比98%,是绝对主战场。
第二个获批的TCR疗法是Adaptimmune的TCR-T细胞药物Afami-cel (afamitresgene autoleucel),商品名Tecelra,FDA于2024年8月1日批准用于二线治疗既往接受过化疗治疗的不可切除或转移性滑膜肉瘤成人患者,且肿瘤表达MAGEA4,同时HLA-A*02:01P阳性、HLA-A*02:02P阳性、HLA-A*02:03P阳性、HLA-A*02:06P阳性。Tecelra定价为72.7万美元,公司预计该产品的年销售峰值可能高达4亿美元。
Vol.9
资 本 市 场 表 现
近期,香雪制药发布其TCR-T细胞疗法纳入优先评审后,在九个交易日股价涨幅超过210%;东北制药收购TCR-T细胞疗法企业肽源生物(鼎成肽源),连续两个交易日股价涨幅21.22%。可见国内资本对TCR疗法的热度颇高。
截至2024年8月,涉及到TCR疗法的相关公司共计10家上市公司:Immunocore (IMCR) 是一家纳斯达克上市公司,聚焦于TCR蛋白药物的开发,市值18.5亿美元;Immatics (IMTX) 是一家纳斯达克上市公司,具有TCR-T和TCR蛋白药双平台,市值12.1亿美元;东北制药 (000597) 通过并购方式进入到TCR-T和TCR蛋白药领域,市值62.2亿元;香雪生命是创业板上市公司香雪制药 (300147) 的控股子公司,香雪制药市值为53.2亿元;Lyell Immunopharma (LYEL) 是一家纳斯达克上市公司,具备TIL、CAR-T和TCR-T平台,市值3.7亿美元;TScan (TCRX) 是一家纳斯达克上市公司,公司对T细胞的生理靶点进行迅速和无偏倚筛选来开发治疗癌症和传染病的TCR药物,市值3.18亿美元;百奥赛图 (HK2315) 是一家港股上市公司,主要技术平台为抗体技术,包括TCR抗体,市值24.4亿港币;Adaptimmune (ADAP) 是一家纳斯达克上市公司,聚焦于TCR-T疗法,市值2.9亿美元;永泰生物 (HK6978) 是一家港股上市公司,主要技术平台为EAL和CAR-T疗法,同时拓展到TCR-T领域,市值15.9亿港币;Tevogen (TVGN) 是一家纳斯达克上市公司,主营未经基因修饰的现成T细胞治疗产品,市值1.1亿美元;
从2020年至2024年8月20日,共有57家TCR相关概念的公司获得多轮融资,主要地区在美国和中国,维渡纵横统计了涉及TCR概念的生物科技公司近年来的最新融资情况,如表4所示。
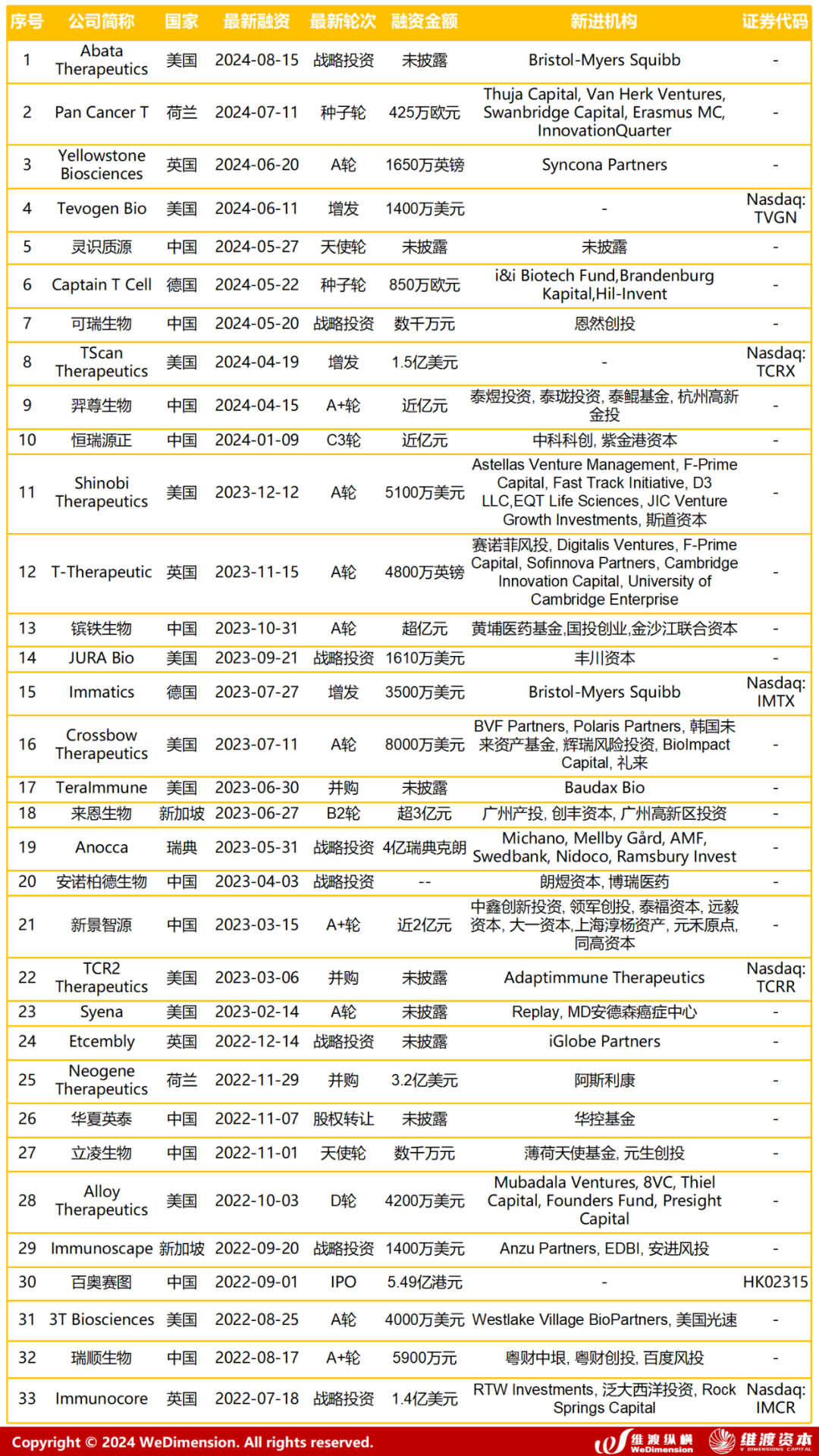
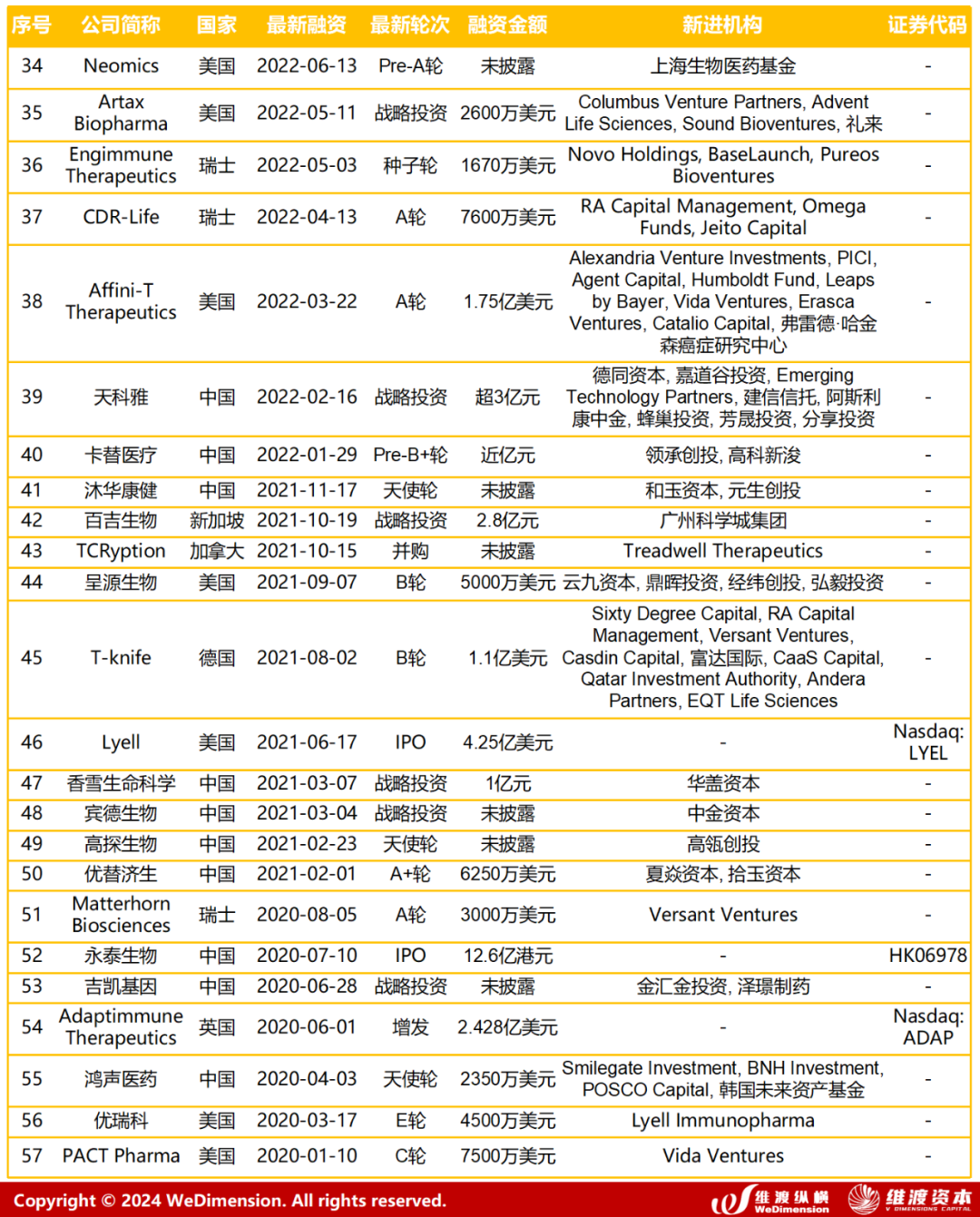
Vol.10
总 结 与 展 望
E.N.D

往期文章推荐:
北京发布《高质量建设细胞与基因治疗产业集群实施方案(2024-2026年)(征求意见稿)》
总投资1.28亿,国内这一细胞与基因治疗CDMO平台正式揭牌
全球领先重大突破!20名难治性红斑狼疮患儿在浙大儿院接受CAR-T治疗后,全部停用激素及所有免疫制剂
诺思兰德上海分公司开业,全面布局基因治疗药物NL003商业化
广东发布新政,支持基因治疗、细胞治疗等创新生物制品研发,重点发展基因技术、细胞治疗、合成生物学等新领域新赛道
Nature官网头条!中国学者发表国际首个通用CAR-T治疗成果
复星医药将在上海打造国内乃至全球最强大、最全面的细胞治疗管线,持续加强肿瘤创新药研发
卫健委:医疗卫生机构开展IIT研究管理办法10月1日起施行(附解读)




































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论