近年来,细胞治疗成为明星研发方向,其涉及到抗衰、再生、修复等多个领域。科学家在探索细胞巨大潜力的同时,关注到细胞副产物外泌体这种无细胞治疗工具。外泌体以其携带丰富的活性分子和较低的免疫原性成为极具前景的药物递送载体。
药学界始终为药物递送效率和药物精准靶向病灶器官这两个重点问题所困扰。外泌体研究者致力于寻找一种稳定的策略改造工程化外泌体,以便精准靶向目标器官并携带更多有效药物成分。截至目前外泌体研究界已开发出RVG29多肽脑靶向、CAP多肽骨靶向、CTP心脏靶向亲和肽等工程化外泌体,其稳定性也在逐步优化中。
综上,外泌体正在成为下一代药物安全精准递送平台。
来自皖南医学院与蚌埠医科大学的团队紧抓热点锐意创新,于近期在ACS Nano外泌体权威杂志发表了工程化细胞外囊泡治疗病毒性心肌炎的相关文章。

在本研究中,通过工程化细胞外囊泡对病毒性心肌炎进行多靶点免疫调节治疗。研究者提出了一种多靶点修饰的针对M1型巨噬细胞的细胞外囊泡疗法。
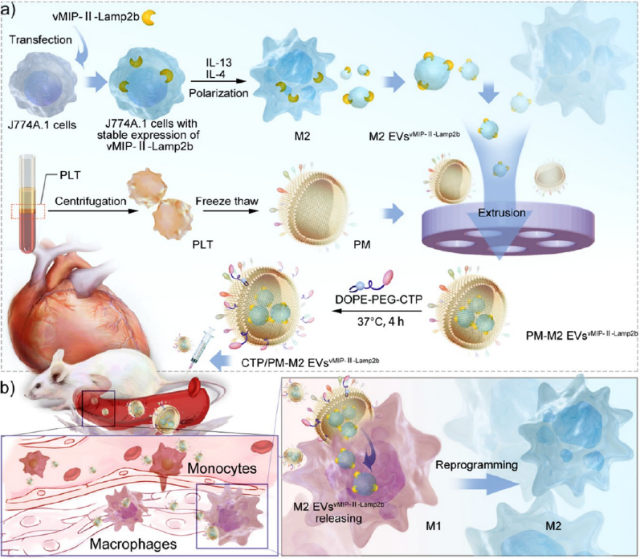
通过vMIP-II基因(趋化因子受体拮抗肽)修饰获得的高表达vMIP-II的M2型EVs,不仅有助于提高M2型EVs的靶向能力,还可与M2型EVs协同调节炎症微环境中的M1型巨噬细胞,下调心脏组织中炎症因子表达,有助于改善心脏炎症。研究者进一步开发了CTP(心脏亲和肽)和PM(血小板质膜)工程化的靶向细胞外囊泡,以改善目标物向心脏组织的输送。
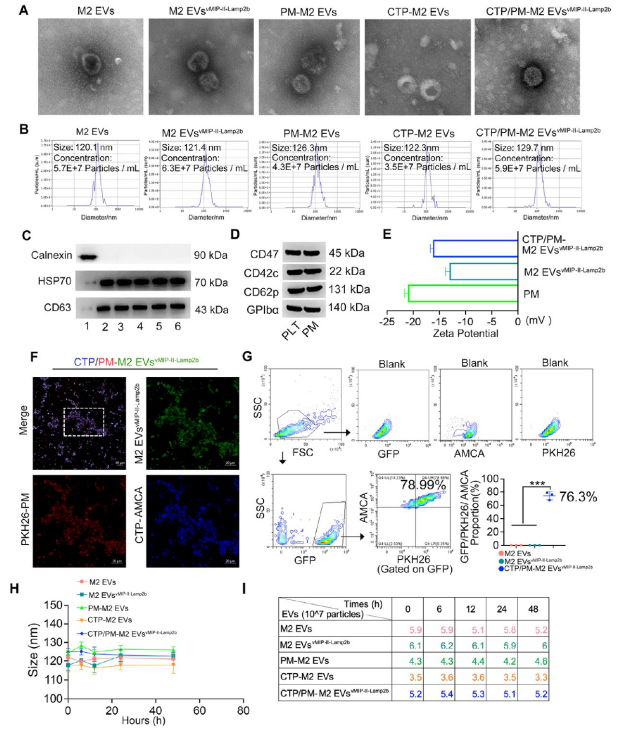

文章中,研究者通过尺寸排阻法色谱法分离出细胞外囊泡EVs,又从富血小板血浆PRP中分离出血小板质膜PM,应用TEM、NTA、zeta电位、纳米流式NanoFCM等手段对EVs进行表征。后续又采用流式标记及共聚焦对细胞摄取EVs的效率进行分析,并结合离体器官活体成像对动物体内各脏器的EVs分布进行对比分析。最后,研究者成功在小鼠病毒性心肌炎动物疾病模型中观察到工程化EVs被心脏摄取并显著改善射血分数等各项心脏功能。
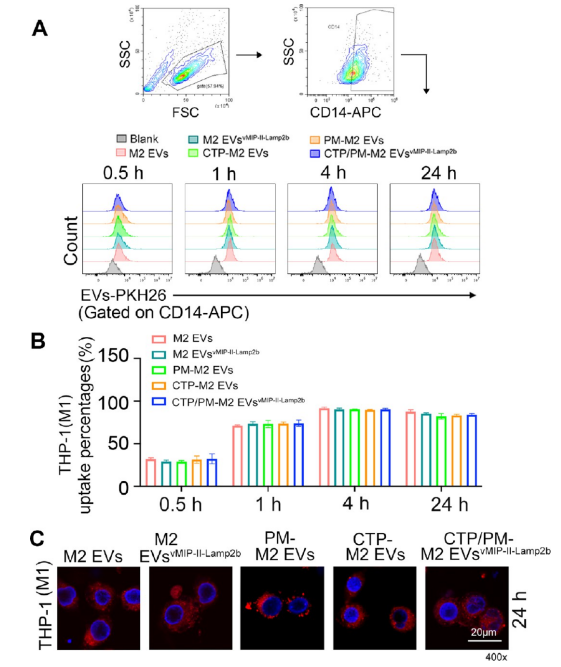
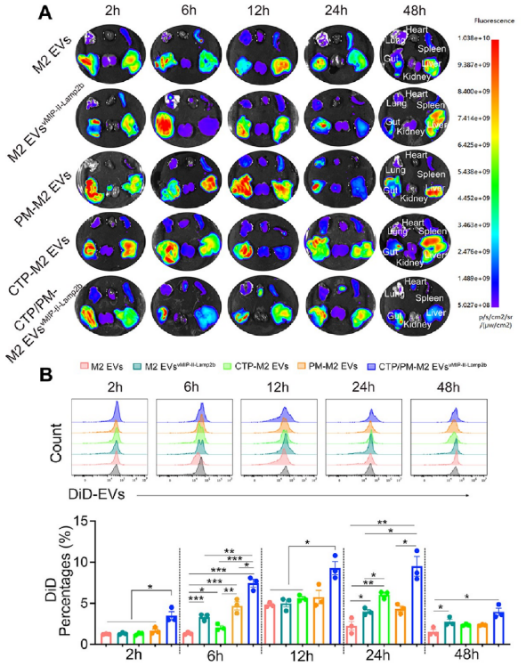
综上,该文章构建了表面携带趋化因子受体拮抗肽的CTP心脏靶向工程化细胞外囊泡CTP/PM-M2 EVsvMIP‑II‑Lamp2b,经文章验证能够靶向递送至心脏炎症微环境中的巨噬细胞M1,进而减轻病毒性心肌炎的爆发性炎症心肌损伤。


和元服务
和元生物技术(上海)股份有限公司多年来聚焦于病毒基因治疗领域,具有丰富的基因治疗先导研究和药物临床前研究经验。能够提供基于AAV腺相关病毒外泌体工程化的改造与探索性研究服务。
业务咨询



和元生物成立于2013年,作为深耕细胞和基因治疗核心领域的高新技术企业,专注于为细胞和基因治疗的基础研究提供基因治疗载体研制、基因功能研究、药物靶点及药效研究等CRO服务;为细胞与基因治疗药物的研发提供工艺开发及测试、IND-CMC药学研究、临床样品及商业化产品的GMP生产等CDMO服务;为再生医学及抗衰领域提供细胞制备、重组蛋白/外泌体等细胞衍生物生产、细胞存储等技术服务。致力于推动细胞和基因治疗及相关健康产业的技术开发及转化应用,造福生命健康。



































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论