
导语
HP双靶治疗原发耐药,如何快速控制疾病?
案例概述
案例讨论
HP双靶治疗原发耐药,如何选择后续治疗方案快速控制疾病进展?
病例展示
患者女,51岁,既往史、家族史无特殊。
现病史 手术:患者于2022-09-01行“左乳区段切除+左侧乳房根治性切除术伴同侧腋窝前哨淋巴结活检+腋窝淋巴洁清扫术”,术后病理示:(左乳)浸润性导管癌2-3级,伴高级别导管内癌;切面见质韧区长径3cm,各组淋巴结7/23(冰冻前哨2/4,腋下5/19)。免疫组化:ER(-),PR(-),HER2(2+),FISH检测阳性,Ki-67指数约25%,P63(-),部分导管周(+),E-cadherin(+),CK7(+),CD117(-),S-100(-),CD31/D2-40脉管染色未见明确脉管瘤栓。
术后辅助治疗:于2022-09至2023-12行AC-THP方案化疗8周期及靶向治疗17次。于2023-04行辅助放疗25次。
复发转移:2024-02患者发现皮肤癌结节进行性增长,左侧胸壁瘙痒、针扎样刺痛。于2024-03-26行乳腺彩超示:左侧胸壁皮下软组织增厚,回声欠均匀。2024-03-28行胸壁皮肤切检:(左侧)胸壁皮肤内见浸润性癌。免疫组化:ER(-),PR(-),HER2(3+),Ki-67指数约50%,CD31、D2-40染色可见广泛脉管瘤栓。
晚期一线治疗:于2024-04-10行T-DXd(300mg ivgtt)治疗至今,2周期治疗后皮肤红斑和溃烂明显好转,8月已基本恢复正常,现已治疗6周期,期间疗效评估为CR。
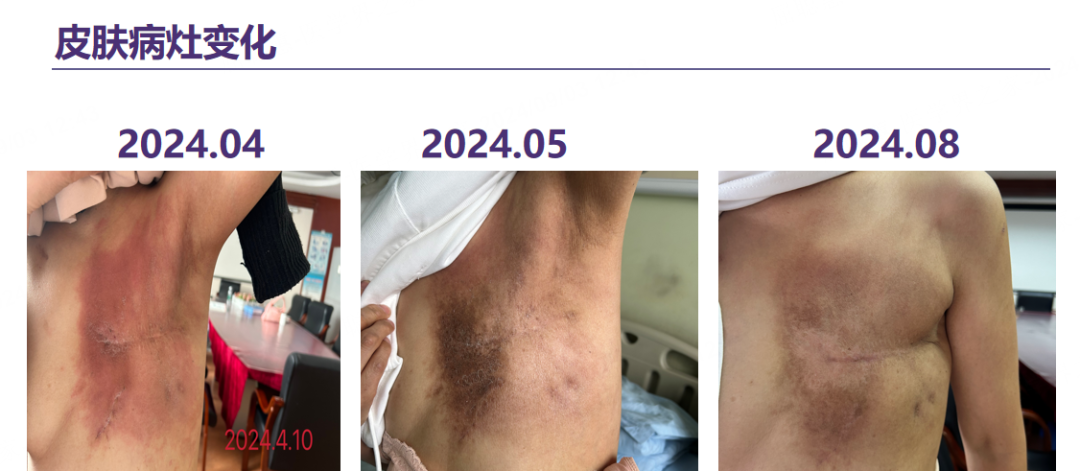
图1. 皮肤病灶变化

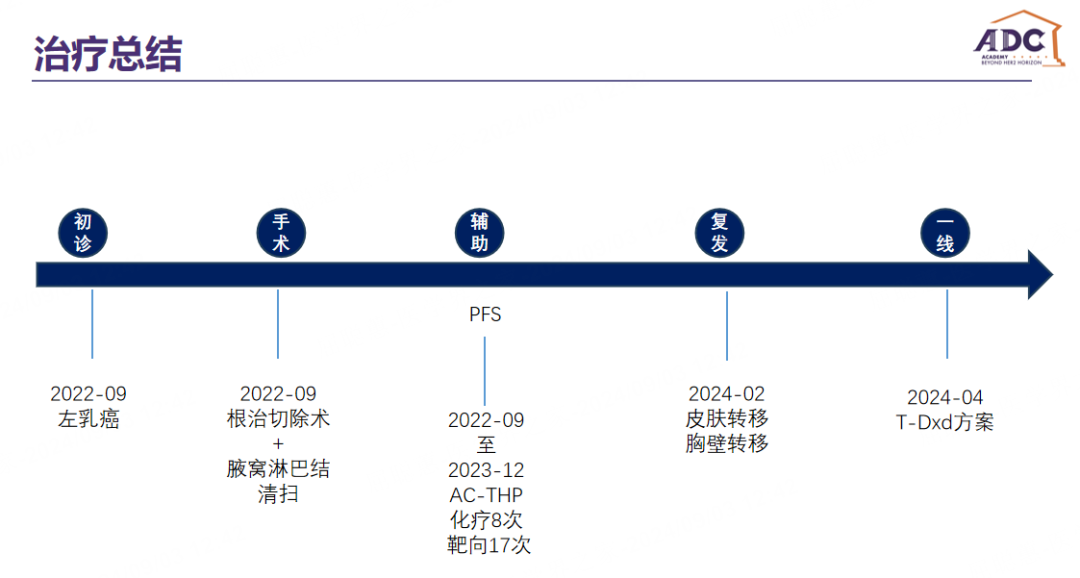
图2. 病例治疗经过
病例展示
患者女,51岁,既往史、家族史无特殊。
手术:患者于2022-09-01行“左乳区段切除+左侧乳房根治性切除术伴同侧腋窝前哨淋巴结活检+腋窝淋巴洁清扫术”,术后病理示:(左乳)浸润性导管癌2-3级,伴高级别导管内癌;切面见质韧区长径3cm,各组淋巴结7/23(冰冻前哨2/4,腋下5/19)。免疫组化:ER(-),PR(-),HER2(2+),FISH检测阳性,Ki-67指数约25%,P63(-),部分导管周(+),E-cadherin(+),CK7(+),CD117(-),S-100(-),CD31/D2-40脉管染色未见明确脉管瘤栓。
术后辅助治疗:于2022-09至2023-12行AC-THP方案化疗8周期及靶向治疗17次。于2023-04行辅助放疗25次。
复发转移:2024-02患者发现皮肤癌结节进行性增长,左侧胸壁瘙痒、针扎样刺痛。于2024-03-26行乳腺彩超示:左侧胸壁皮下软组织增厚,回声欠均匀。2024-03-28行胸壁皮肤切检:(左侧)胸壁皮肤内见浸润性癌。免疫组化:ER(-),PR(-),HER2(3+),Ki-67指数约50%,CD31、D2-40染色可见广泛脉管瘤栓。
晚期一线治疗:于2024-04-10行T-DXd(300mg ivgtt)治疗至今,2周期治疗后皮肤红斑和溃烂明显好转,8月已基本恢复正常,现已治疗6周期,期间疗效评估为CR。

图1. 皮肤病灶变化


图2. 病例治疗经过
专家点评
该病例为HER2阳性乳腺癌,接受AC-THP方案辅助治疗结束不满1年复发转移,属于曲妥珠单抗治疗失败人群。根据《中国临床肿瘤学会(CSCO)乳腺癌诊疗指南2024》,在曲妥珠单抗治疗失败的患者中,T-DXd和吡咯替尼联合卡培他滨均作为I级推荐方案(1A)[1]。T-DXd的这一推荐基于其关键III期DESTINY-Breast03研究(DB03),既往公布数据显示,在曲妥珠单抗和紫杉烷经治的HER2阳性晚期乳腺癌患者中,T-DXd组中位无疾病进展生存期(mPFS)历史性的延长至28.8个月,是T-DM1组6.8个月的4倍[2],也远高于PHOEBE研究中吡咯替尼联合卡培他滨的12.5个月[3],T-DXd以其前所未有的PFS获益,奠定了其抗HER2治疗二线标准治疗地位。因此,基于DB03研究中T-DXd的突破性疗效,该患者选用T-DXd方案治疗。


图3. T-DXd大幅提高二线治疗的PFS,远超既往研究数据
此外,2024年ASCO年会中公布的DB03研究OS数据显示,T-DXd的mOS长达52.6个月,相较于T-DM1的42.7个月延长了近10个月,几乎可以媲美CLEOPATRA研究中曲帕双靶方案一线治疗的生存数据;PFS数据也进一步更新,T-DXd组研究者评估的mPFS相较于T-DM1延长了21.8个月(29.0个月 vs 7.2个月),与既往结果保持一致[4]。T-DXd不仅大幅延长PFS并且可使患者生存期显著延长,进一步支持了其二线治疗优选地位,这无疑为HER2阳性晚期乳腺癌患者带来了极大的治疗希望。


图4. T-DXd突破二线治疗生存时长,刷新二线治疗最长OS
基于DB03研究的突破性获益以及T-DXd可及性的提高,包括CSCO、CACA-CBCS、NCCN、ESMO、ASCO和ABC7等国内外权威指南均一致推荐T-DXd作为HER2阳性晚期乳腺癌二线治疗优选方案[1,5-9]。尤其是在今年更新的《CSCO乳腺癌诊疗指南2024》中,T-DXd取代了T-DM1成为经曲妥珠单抗治疗失败的HER2阳性晚期乳腺癌二线治疗的I级推荐方案(1A)。
该病例疾病进展距曲帕双靶辅助治疗结束未满1年,属于原发性耐药,且肿瘤转移至皮肤病灶,出现明显的红斑和溃烂,严重影响患者生活质量,需要一种快速起效控制肿瘤的治疗方案。
在2022年SABCS大会中公布的DB03研究疗效数据中,T-DXd组确认的客观缓解率(ORR)达到78.5%,BICR评估的完全缓解(CR)率高达21.1%[10],也就是说有超过1/5的患者达到肿瘤完全缓解,即影像学上肿瘤完全消失,显示出其极高的抗肿瘤作用和高效的疾病控制,这意味着绝大部分接受T-DXd治疗的患者都能获得肿瘤病灶的明显缩小,甚至1/5的患者肿瘤可以完全消失,显示出T-DXd绝佳的临床治愈能力。同时,数据显示接受T-DXd治疗的患者中位至肿瘤缓解时间为1.64个月,起效迅速,可以对患者病灶实现快速控制。


图5. DB03研究中,T-DXd治疗组大部分患者肿瘤缩小,ORR高达78.5%
结合该病例4月开始接受T-DXd治疗约2周期后,5月皮肤红斑和溃烂明显好转,8月已基本恢复正常达到CR,表现出与DB03临床研究一致的疾病快速缓解时间,显示出T-DXd高效且快速的疾病控制能力。
DB03研究奠定T-DXd作为HER2阳性晚期乳腺癌二线治疗标准方案的坚实地位,不仅为患者提供可持续控制疾病(PFS达到28.8个月)和更长的生存期(OS达到52.6个月),并且T-DXd能够快速控制疾病,为患者提供快速疾病控制的方案。结合该病例患者晚期一线接受T-DXd治疗6周期后达CR状态,从真实世界角度显示出T-DXd高效且快速的疾病控制,再度证实了T-DXd在HER2阳性晚期乳腺癌治疗领域的卓越疗效,为临床实践提供了有力支持。
点评专家简历
庞慧 教授
病例提供专家简历
郭婷 医师
哈尔滨医科大学附属肿瘤医院肿瘤科住院医师、硕士研究生
中国抗癌协会整合肿瘤心脏病分会 会员

ADC Academy Online
ADC Academy Online是聚焦于抗体偶联药物的学术交流平台。平台紧跟相关领域的最新进展,致力于促进相关专业人士的科学交流和继续医学教育。






































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论