近日,广州百暨基因科技有限公司和深圳市南山区人民医院、香港中文大学在国际著名顶级期刊《Advanced Materials》(影响因子:27.4),合作发布关于铬金属免疫协同CAR-T细胞治疗实体瘤的研究性论文“Photo-metallo-immunotherapy: Fabricating Chromium-Based Nanocomposites to Enhance CAR-T Cell Infiltration and Cytotoxicity against Solid Tumors”( 激光金属免疫:铬基纳米复合材料增强 CAR-T 细胞实体瘤浸润与细胞毒性杀伤能力)。该研究公布了铬金属免疫在CAR-T疗法中的前沿研究成果,展现了铬金属免疫在提升CAR-T细胞对实体瘤治疗效能方面的潜力,为肿瘤治疗领域带来了创新性的思考与启示。


【文章要点】
该研究发现,铬纳米粒子与Cr3+离子在推动针对B7H3的CAR-T细胞迁移及促进穿孔素与颗粒酶释放方面展现出显著作用。研究团队成功设计出一种表面覆盖有生物可降解聚多巴胺的铬纳米光敏药物体系。在近红外激光的精准照射下,该铬复合纳米材料能够借助光热疗法(PTT)机制,于局部区域诱发高温效应,有效杀灭实体肿瘤细胞。此策略不仅显著遏制了肿瘤的生长进程,还积极促进了血清中关键细胞因子(包括IL-2、IFN-γ、TNF-α)的分泌,进而增强了机体的免疫反应。
值得注意的是,该纳米复合物的主要降解产物Cr3+在生理环境中亦扮演了重要角色,其能够提升CXCL13与CCL3趋化因子的表达水平,并在肿瘤组织内部诱导形成三级淋巴样结构(TLSs)。这一变化对于优化CAR-T细胞在肿瘤部位的浸润深度与杀伤效能具有深远影响,为实现更为高效的肿瘤免疫治疗提供了新的思路与策略。
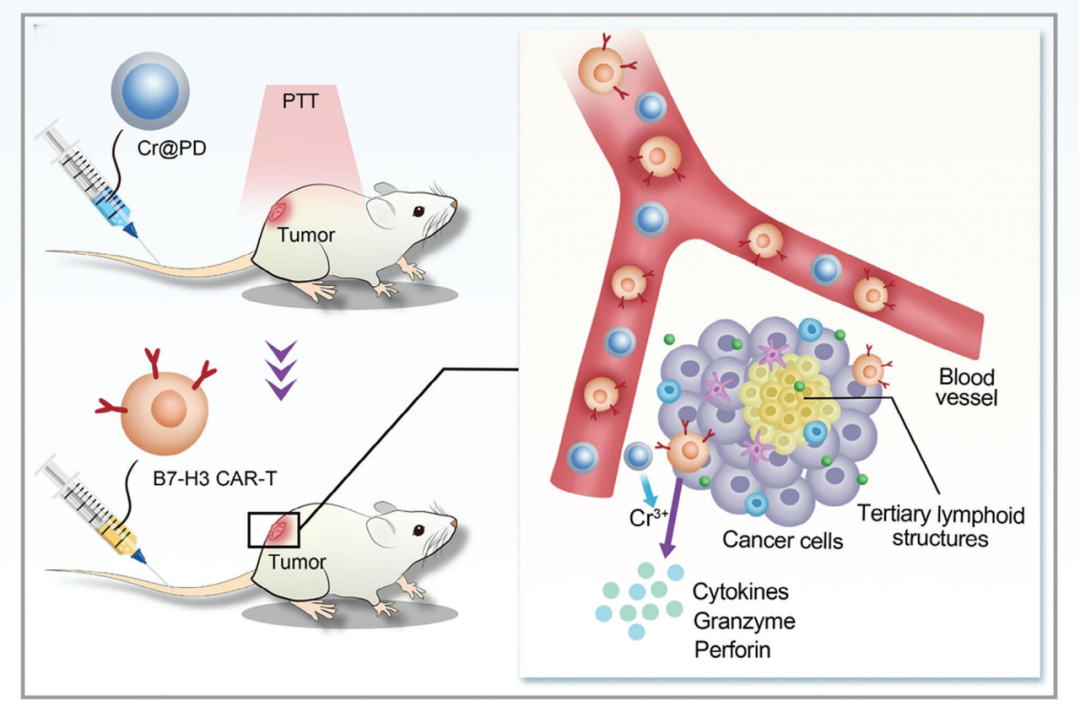
图1. 铬复合纳米结合光热疗法(PTT)增强CAR-T浸润和杀伤能力

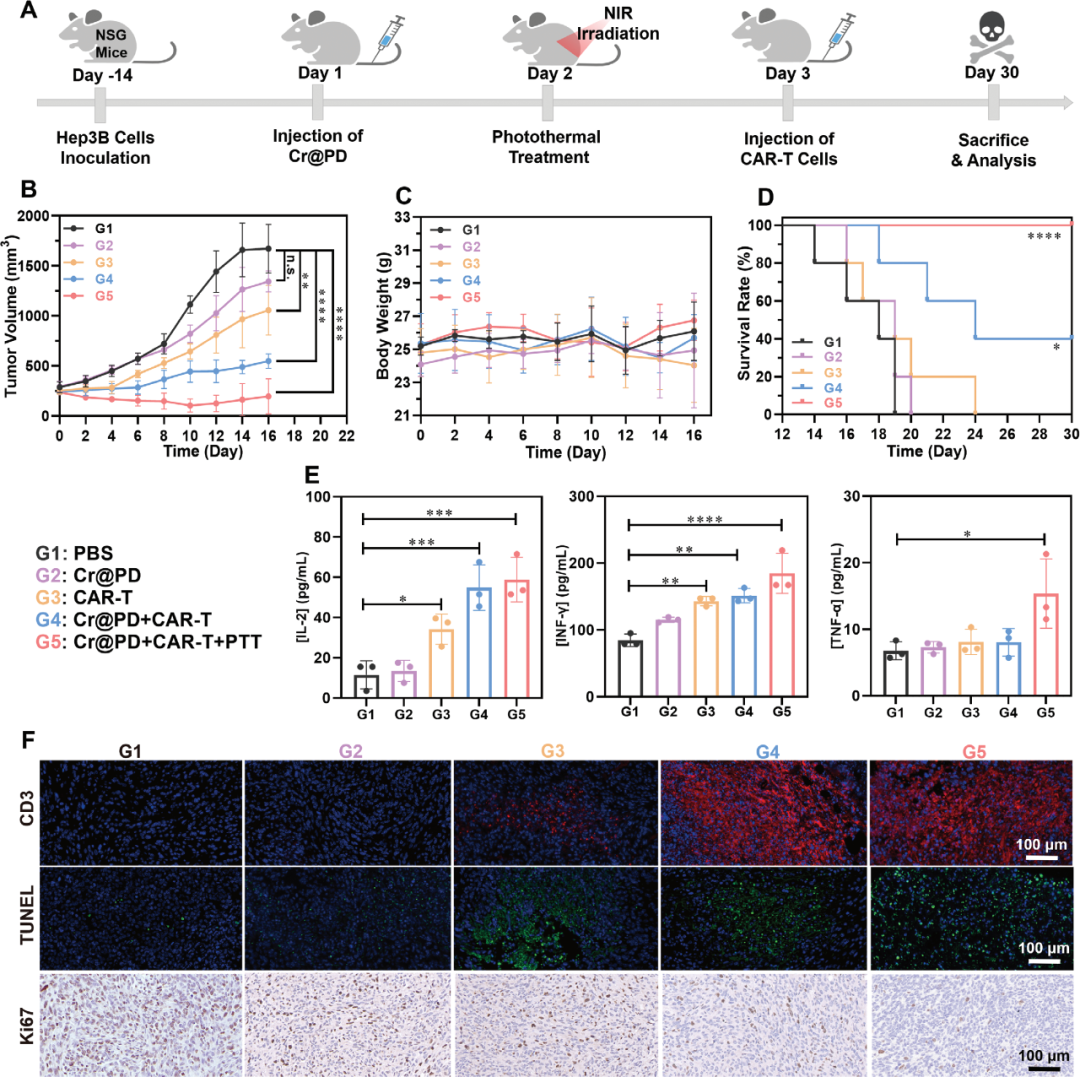
图3. 铬复合纳米增强CAR-T细胞的体内抗肿瘤作用
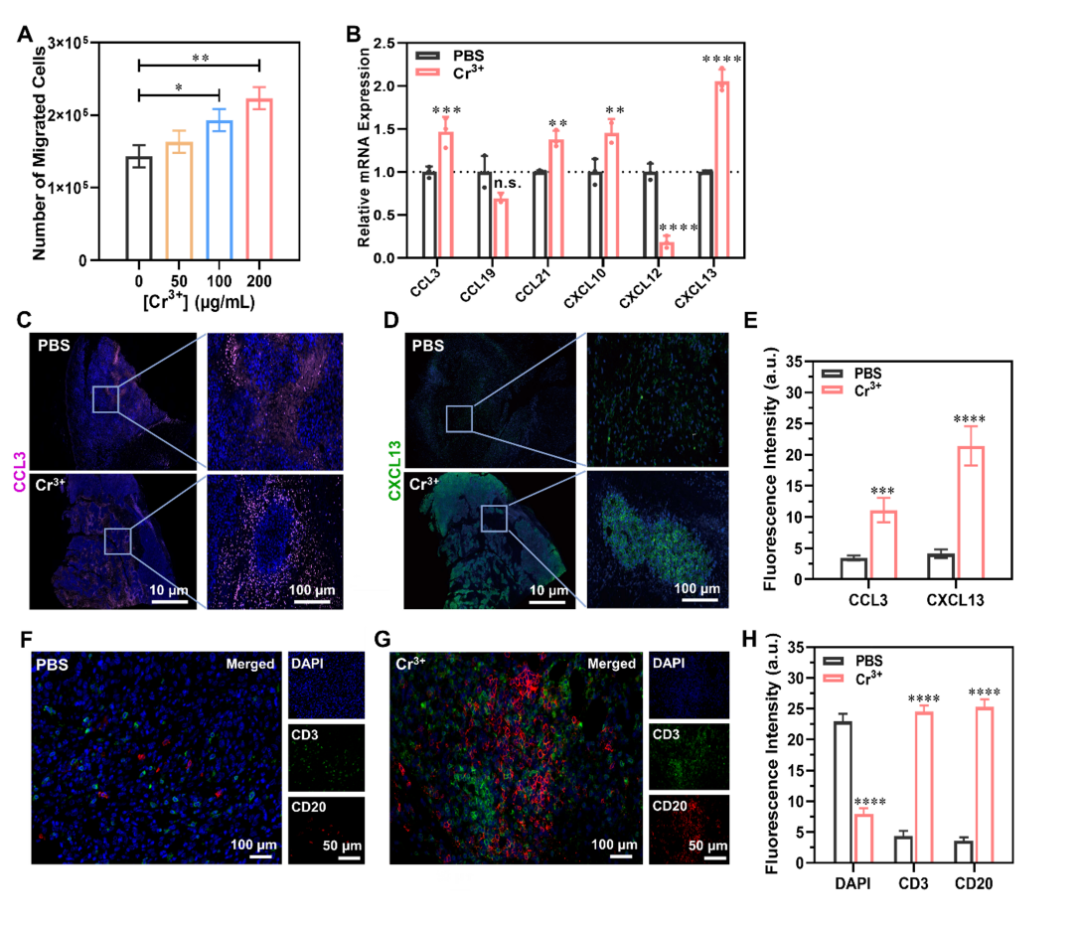
图4. 铬金属/离子促进肿瘤三级淋巴结构TLS新生成
【结论与未来】
该研究率先揭示了铬金属免疫在肿瘤免疫治疗中的潜在价值,并创新性地提出了铬激光金属免疫的概念,成功将光敏智控技术引入肿瘤金属免疫领域。该研究不仅为金属元素在肿瘤治疗中的应用奠定了坚实的原创基础,更展现出深远的启发与引领作用,同时也是科研院校、临床一线与医药企业间开放合作、协同创新的典范。


百暨基因致力于研发新一代免疫细胞疗法,其自主研发的Anti-CLL1 CAR-T(BG1805)已于2022年获得IND批件,正在开展针对急性髓系白血病(AML)的临床试验。该药物还荣获了FDA与EMA授予的孤儿药资格,进一步证明了其在AML治疗领域的潜力与价值。目前,百暨基因已与全国超过30家顶尖三甲医院建立了稳固的临床合作关系。未来,公司将继续依托其强大的临床转化经验,与各方团队紧密合作,实现优势互补,共同推动粤港澳大湾区在科技创新与产业创新方面的深度融合与发展,进一步提升大湾区在医药领域的国际影响力与创造力,为广大肿瘤患者带来实质性的福音。

论文链接:
https://onlinelibrary.wiley.com/doi/full/10.1002/adma.202407425




































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论