Interius BioTherapeutics(以下简称“Interius”)公司近期宣布其首次为患者注射了一种新型体内嵌合抗原受体(CAR)基因疗法 INT2104。该疗法旨在通过静脉注射将CAR基因直接递送到患者体内,从而在体内生成CAR-T和CAR-NK细胞,用于治疗B细胞恶性肿瘤。
Interius总裁兼首席执行官Phil Johnson博士表示,公司成立的目的在于为患者提供一种新的治疗选择,这种选择不需要预处理或长时间的制造和等待期。Interius 的突破性技术允许通过静脉给药精确地将目的基因靶向特定细胞。这是一个重要的里程碑,标志着首次在Ⅰ期临床上使用持久性的体内CAR疗法。INT2104有潜力克服现有的体外CAR-T细胞基因疗法所面临的挑战,该疗法有望成为一种单剂量、“现货通用型”、广泛可及的治疗B细胞恶性肿瘤的疗法。Michael Dickinson医生(此临床试验主要研究者之一)补充道:“为癌症患者提供新的、易于获得的治疗选择至关重要。像体内CAR基因疗法这样的创新方法有可能改变我们治疗癌症的方式,提供更快、单剂量的解决方案,减少对患者和医疗机构的负担。”INT2104是一种基于慢病毒载体的体内基因疗法,靶向感染CD7阳性的T细胞和自然杀伤细胞(NK细胞),并转导CAR转基因以体内生成效应CAR-T细胞和CAR-NK细胞,生成的效应CAR细胞将靶向CD20阳性的B细胞来治疗B细胞恶性肿瘤。INT2104设计示意图(图片来源公司官网)
不同于体外CAR-T疗法,INT2104是一种现成的、单剂量治疗方式,通过静脉注射全身给药,无需淋巴耗竭和大型或昂贵的治疗设备。在临床前研究中,该疗法显示出了良好的有效性和安全性。
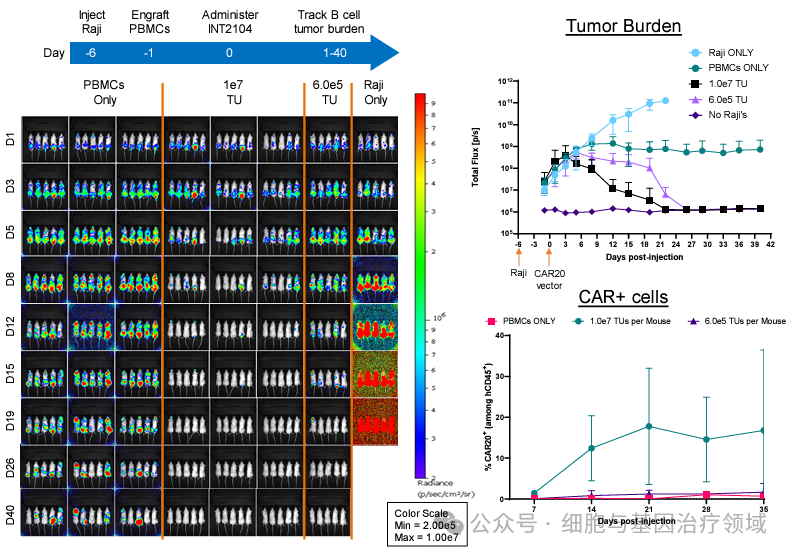
INT2104的部分临床前实验数据(图片来源公司官网)
据悉,INT2104的此临床试验是一项全球性的、多中心、开放标签的试验,其临床试验名称为INVISE(Injectable Vectors for In Situ Engineering),将评估单次INT2104输注在复发/难治性B细胞恶性肿瘤成人患者中的安全性。其中,剂量递增部分所获得的数据将用于确定后续剂量确认研究和未来研究中使用的INT2104剂量。声明:内容来源于公司官网等处,本文旨在知识共享,所有内容仅供参考,不构成任何建议。
<END>
*版权声明:本网站所转载的文章,均来自互联网,旨在传递更多信息。鉴于互联网的开放性和文章创作的复杂性,我们无法保证所转载的所有文章均已获得原作者的明确授权。如果您是原作者或拥有相关权益,请与我们联系,我们将立即删除未经授权的文章。本网站转载文章仅为方便读者查阅和了解相关信息,并不代表我们认同其观点和内容。读者应自行判断和鉴别转载文章的真实性、合法性和有效性。








































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论