
内容来源:爱医时空
前言
近期,一项国际多中心、前瞻性Ⅰ期临床研究——SHR-A1811-I-101正式见刊国际肿瘤学领域顶尖期刊《Journal of Clinical Oncology》(JCO,IF=42.1,Q1)1。该研究首开先河,验证了新一代抗体缀合药物(ADC)SHR-A1811在针对晚期实体肿瘤、且历经多线治疗失败的患者群体中安全性、抗肿瘤活性以及药代动力学特性,为HER2靶向ADC药物阵营增添了又一强效成员。

SHR-A1811-I-101研究见刊肿瘤学领域顶尖期刊JCO
回顾此前,SHR-A1811的初步研究数据已在多个国际权威学术会议上大放异彩:2023年美国癌症研究协会(AACR)年会上,恒瑞医药首次披露了SHR-A1811的临床前及临床研究数据,其强劲的治疗潜力引起了广泛关注。随后,在同年举行的欧洲肿瘤内科学会(ESMO)大会上,SHR-A1811在非乳腺癌晚期实体瘤治疗中的详细数据以Mini Oral报告的形式亮相,进一步向全球展示了其广泛的应用潜力和独特的临床价值。
研究背景
人表皮生长因子受体2(HER2)靶向疗法的出现,彻底颠覆了HER2过表达或突变肿瘤的治疗格局,显著延长了患者的生存期,成为肿瘤治疗领域的一大里程碑2。尽管在HER2阳性乳腺癌的治疗上取得了辉煌成就,但将该类成功策略拓展至其他HER2驱动的非乳腺癌肿瘤类型时,却遭遇了技术瓶颈与临床实践的复杂挑战,这进一步强调了乳腺癌领域之外,针对此类分子特征肿瘤治疗的迫切未竟需求。
ADC药物技术在乳腺癌及非乳腺癌的HER2靶向治疗中掀起了一场革命。DS-8201a(又称T-DXd),作为ADC的杰出代表,展示了在HER2阳性及低表达乳腺癌、特定HER2突变型非小细胞肺癌(NSCLC)、HER2阳性胃或胃食管结合部(G/GEJ)腺癌以及HER2阳性实体瘤中的广泛治疗潜力,标志着治疗策略的重大飞跃。然而,ADC药物的广泛应用亦伴随着挑战,如间质性肺疾病(ILD)风险的增加及耐药机制的显现等3-4,这些挑战迫切要求我们不断探索,以克服ADC疗法的局限性,进一步优化治疗策略。
在此背景下,SHR-A1811作为一种新型ADC药物应运而生,它由抗HER2抗体曲妥珠单抗、可裂解连接子及拓扑异构酶I抑制剂有效载荷SHR169265精妙组合而成,展现了治疗潜力。SHR-A1811的有效载荷SHR169265不仅具有更高的膜穿透能力,还显著增强了细胞杀伤效果。尤为关键的是,该药物在连接子与毒素之间创新性地引入了手性环丙基设计,这一举措极大地提升了药物化学稳定性,有效控制了毒素的精准释放,并显著降低了早期释放可能引发的副作用5。
鉴于此,I期首次人体临床试验被启动,旨在深入评估SHR-A1811在经标准治疗失败、HER2表达或突变的不可切除、晚期或转移性实体瘤患者中的安全性、耐受性、疗效及药代动力学(PK)特性。此项研究不仅是对新型ADC药物潜力的一次深入探索,更是向优化HER2靶向治疗、提升患者预后迈出的重要一步。
研究方法
本研究是一项国际多中心、首次在人体中进行的I期试验,在33个中心开展。纳入了HER2表达或突变的不可切除、晚期或转移性实体瘤,并且对标准治疗无效或不耐受的患者。SHR-A1811通过静脉注射给药,每3周1次,每公斤体重剂量从1.0-8.0mg进行剂量爬坡,选择4.8-8.0mg进行PK拓展,选择4.8和6.4mg进行疗效拓展。主要研究终点为剂量限制性毒性、安全性和Ⅱ期推荐剂量。
纳入标准:
患者年龄为18岁及以上,患有不可切除、晚期或转移性实体瘤,对标准治疗难治性或不耐受;
在剂量递增和PK拓展阶段,纳入经组织学证实的HRE2表达或突变的实体瘤患者;
在疗效扩展阶段,符合条件的患者为HER2阳性乳腺癌(A组)、HER2阳性G/GEJ腺癌(B组)、HER2低表达乳腺癌(C组)、HER2表达或突变的非小细胞肺癌(D组)或其他HER2表达或突变的实体肿瘤(E组)。
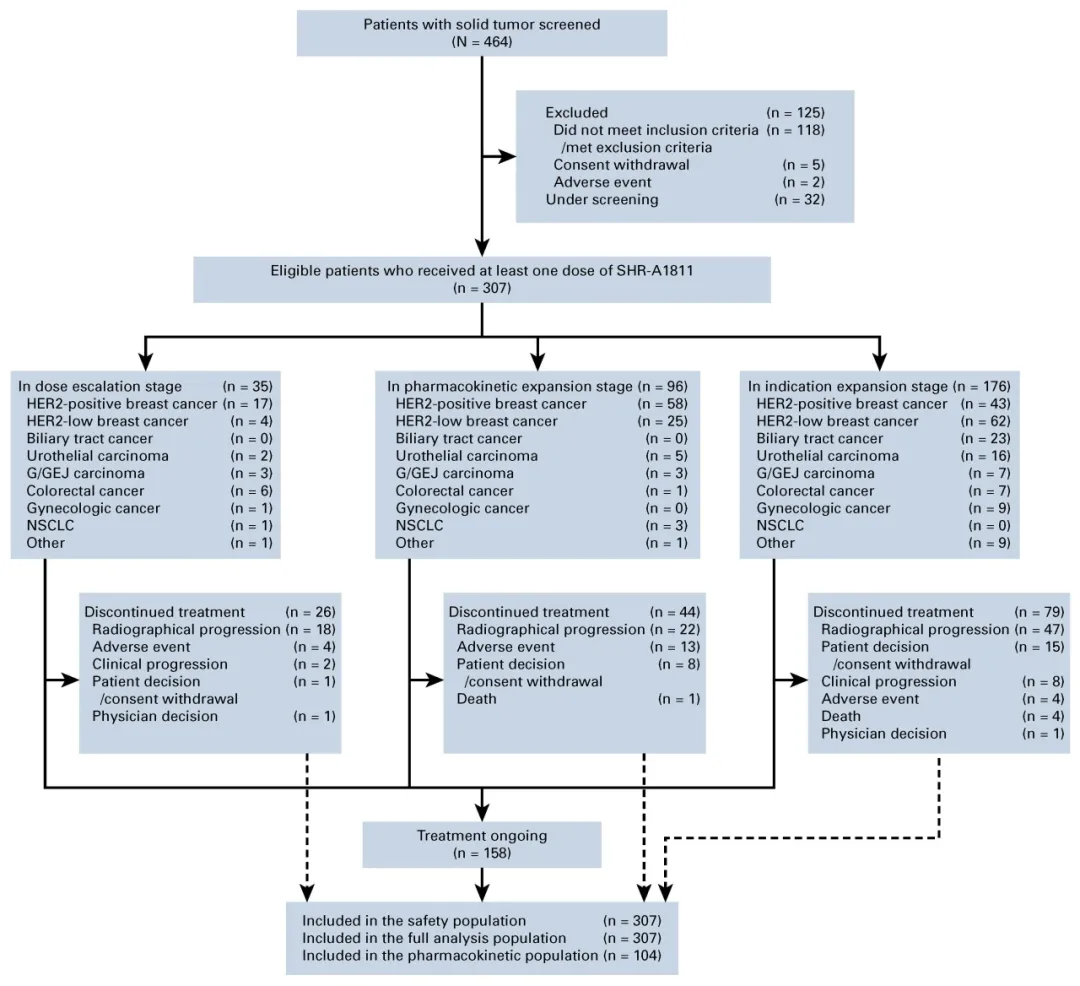
图1. SHR-A1811-I-101研究受试者分布图
研究结果
从2020年9月7日至2023年2月27日,共有307名既往在转移性阶段接受过中位3个(IQR,2-5)系统性治疗的患者接受了SHR-A1811治疗,安全性可控。
SHR-A1811在多种既往多线治疗失败的晚期实体瘤中均有显著的肿瘤应答,307例实体瘤患者的总体客观缓解率(ORR)为59.9%(184/307;95% CI,54.2-65.5);HER2高表达乳腺癌患者ORR为76.3%(90/118;95% CI,67.6-83.6);HER2低表达乳腺癌患者ORR为60.4%(55/91;95% CI,49.6-70.5)。
98例非乳腺实体瘤患者中位随访时间为4.1个月(IQR,2.3-6.5)。在85例疗效可评估的患者中,有39例达到客观缓解(45.9%;95% CI,35.0-57.0),疾病控制率(DCR)为88.2%(95% CI,79.4-94.2)。中位至缓解时间为1.4个月(95% CI,1.2-2.7)。截至数据截止日期,非乳腺癌患者中只有38例(38/98,38.8%)出现疾病进展或死亡。中位PFS尚未达到,6个月PFS率为52.1%(95% CI,34.3-60.3)。
共有123例患者被纳入药代动力学参数人群。单次给药后,在3.2-8.0mg/kg的剂量范围内,SHR-A1811、总抗体和释放的有效载荷的血清/血浆暴露量(Cmax和AUC0-21d)随剂量呈比例增加(如下图)。在所有剂量水平下,SHR-A1811和总抗体的药动学参数相似,释放有效载荷的血浆暴露量较低。此外,免疫原性分析显示,276例(89.9%)可评价免疫原性的患者样本中,没有一例产生治疗后的抗药抗体。

图2. 单次给药后SHR-A1811、总抗体及释放的有效负荷平均血药浓度随时间变化曲线
研究讨论
SHR-A1811的首次人体临床试验揭示了其在既往多线治疗失败、晚期或转移性实体瘤患者中的安全性。特别值得注意的是,间质性肺疾病(ILD)这一关键安全性指标的发生率极低,仅为2.6%,且绝大多数ILD病例表现为轻度至中度,通过及时的皮质类固醇治疗即可有效控制。这一发现不仅体现了SHR-A1811在安全性方面的显著优势,还减轻了患者及其家属对治疗潜在风险的担忧。
SHR-A1811在多种类型的晚期实体瘤中均展现了显著的抗肿瘤活性,其诱导的肿瘤反应不仅强烈且持久。药代动力学数据的分析进一步揭示了SHR-A1811在体内的高效分布与代谢特性,为其在临床中的有效应用提供了坚实的理论基础。尤为突出的是,SHR-A1811中的活性毒素SHR169265展现了对多种肿瘤细胞系的强大生长抑制作用,其IC50值明显低于同类药物,结合其较高的药物抗体比(DAR=6),使得在保持相似抗肿瘤活性的同时,毒素剂量得以显著降低(减少25%),从而减少了潜在的治疗相关毒性。
在HER2阳性及低表达乳腺癌的治疗中,SHR-A1811的ORR分别达到76.2%和60.4%,这一数据不仅优于或接近当前标准治疗(如T-DXd)的效果,还为患者提供了更多治疗选择。
对于非小细胞肺癌(NSCLC)这一难治性肿瘤,SHR-A1811同样展现出了积极的初步疗效信号,尽管当前研究中的患者数量有限,但已足以激发对其进一步探索的兴趣。
在胃或胃食管结合部(G/GEJ)腺癌的治疗中,SHR-A1811的ORR高达50.0%,与当前标准治疗的ORR相当,提示其在该患者群体中具有广阔的应用前景。
SHR-A1811在胆道癌和妇科癌症中也取得了令人鼓舞的疗效数据,ORR分别为56.3%和44.4%。针对这些疾病的大规模临床试验正在积极招募中,以期进一步验证SHR-A1811的广泛适用性。
总 结
总之,SHR-A1811作为一种新型ADC药物,在多种HER2驱动或表达异常的晚期实体瘤中展现出良好的安全性、耐受性和疗效潜力。尽管当前研究尚处初期,但已展现出积极的前景。未来,随着更多大样本、多中心临床试验的推进,SHR-A1811有望为更多肿瘤患者提供新的治疗选择。
参考文献(上下滑动查看):
2. 恒瑞医药不推荐任何未被批准的药品、适应症的使用。
往期精选
| 研发创新 |
| 国际化 |
海外BD再传捷报!恒瑞医药GLP-1类创新药组合实现海外许可
| 重磅奖项 |
| 社会公益 |
“健康中国行·重走长征路”项目启动仪式圆满举行!恒瑞提供公益支持,助力健康中国
恒瑞医药集团向中国扶贫基金会捐赠3000万设立“健康帮扶基金”





































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论