"日本"相关的结果
-
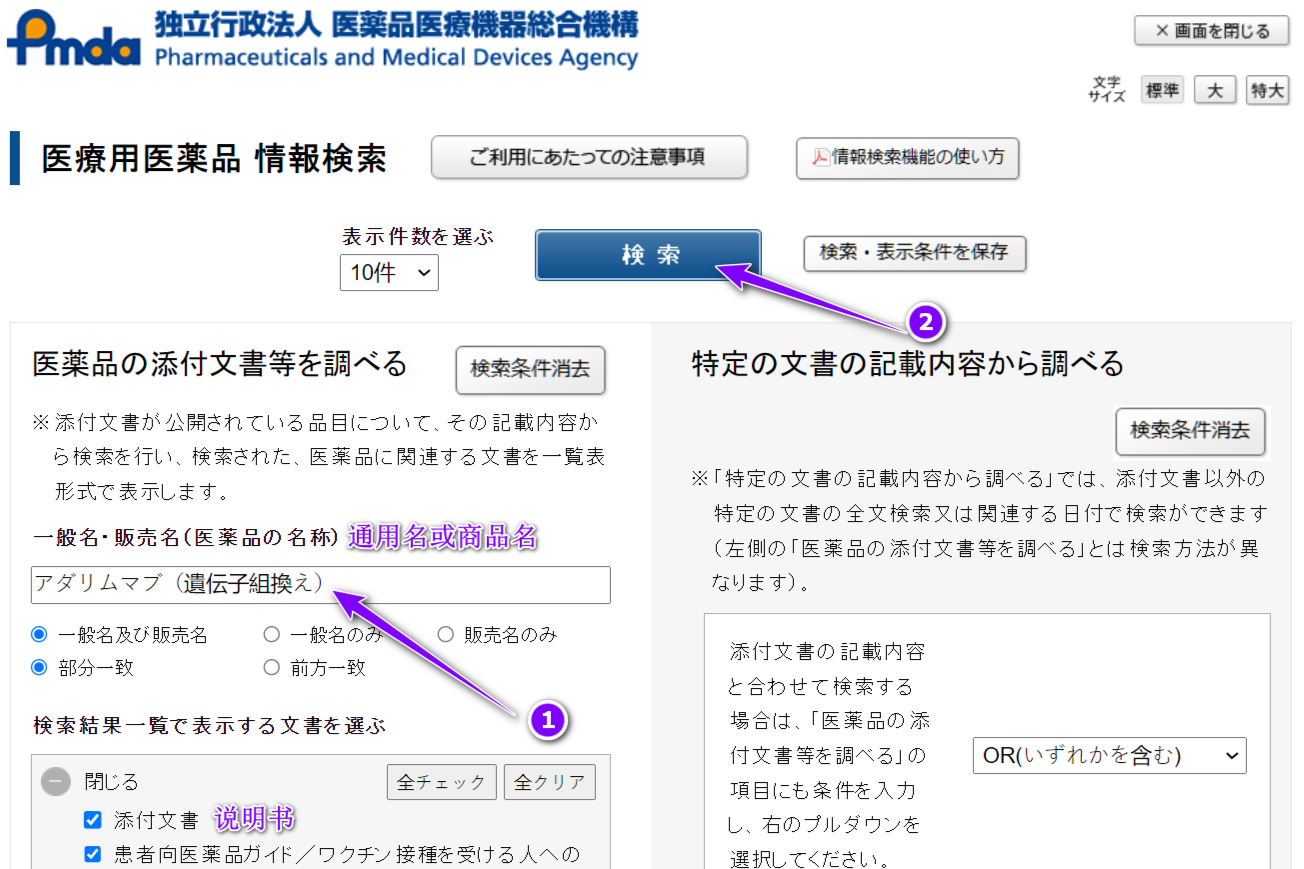
日本药监局(日本药局方)PMDA官网药品查询网站资源介绍,很全!
对于业内人士来说日本药品信息检索能力是一项基本得不能再基本的基本功,但有些新规则、新方法、新工具任值得我们学习探索,进行自我提升。不要求对此有多么高的造诣精深,但需要具备快速对日本药品信息搜集能力,并高效的归纳整合,至此,才能在有限的生命中,挪用更多的时间。日本24301周前 -

日本烟草原研:针对慢性手部湿疹,这款新药中国3期临床中
慢性手部湿疹(CHE,Chronic hand eczema)是指持续三个月以上或一年内复发两次或以上的手部湿疹(HE)。 -
2万美元年!阿尔茨海默病新药Leqembi登陆日本
12月13日,日本卫生部官员表示,阿尔茨海默病的新药lecanemab在日本定价298万日元(20,500美元)/年,该药将于12月20日在日本正式上市。 -

《2020年版医药代表白皮书》 日本刚刚发布!
昨日,日本医药代表认证中心发布了《2020年版医药代表白皮书》,截止 2020 年 3 月 31 日,日本医药代表人数为 57158 人,比去年减少了 2742 人,年度减少人数又创历史新高。 -

肾癌一线治疗 Opdivo+Cabometyx组合在日申请上市
在本月下旬,Cabometyx+Opdivo组合治疗晚期RCC的补充申请获得了美国FDA的优先审查。 -

挂牌上岗 日本医药代表要开始了!
23日,日本医药代表认证中心公布了《医药代表认证纲要》,其中第一条指出,作为一名“专家”,医药代表以患者为中心,开展合理使用药物所必须的信息活动,在职业生涯中不断提高从业资质,从而为人们的健康和卫生状况做出贡献。 -
微芯生物西达本胺在日本上市申请获受理
今日(10月13日),微芯生物发布公告称其合作方沪亚生物近日向日本医药品医疗器械综合机构(PMDA)就西达本胺(海外编号:HBI-8000)单药治疗成年人T细胞白血病 (ATL)递交了新药上市申请(NDA)并获受理。 -

日本批准JYSELECA®(非戈替尼)治疗类风湿性关节炎
吉利德科学公司(纳斯达克:GILD)和卫材株式会社(日本东京)近日宣布,日本厚生劳动省(MHLW)已准予吉利德 K.K.(日本东京)对Jyseleca®(非戈替尼200mg和100mg片剂)的监管批准。 -

梯瓦日本提交Ajovy上市申请 出售合资企业仿制药资产
梯瓦制药(Teva Pharma)和大冢制药(Otsuka Pharma)近日联合宣布,已向日本药品和医疗器械管理局(PMDA)提交了Ajovy(fremanezumab)的上市申请,用于偏头痛的预防性治疗








































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息