
8月2日,卫材公布了2024财年Q1(4-6月)财报:总收入1890亿日元(约12.9亿美元),同比下降4%;毛利润1493亿日元(约10.19亿美元),同比下降2.4%;研发费用417亿日元(约2.85亿美元),同比增长1.5%。

预计2024财年将实现7540亿日元(约51.46亿美元)的总营收。

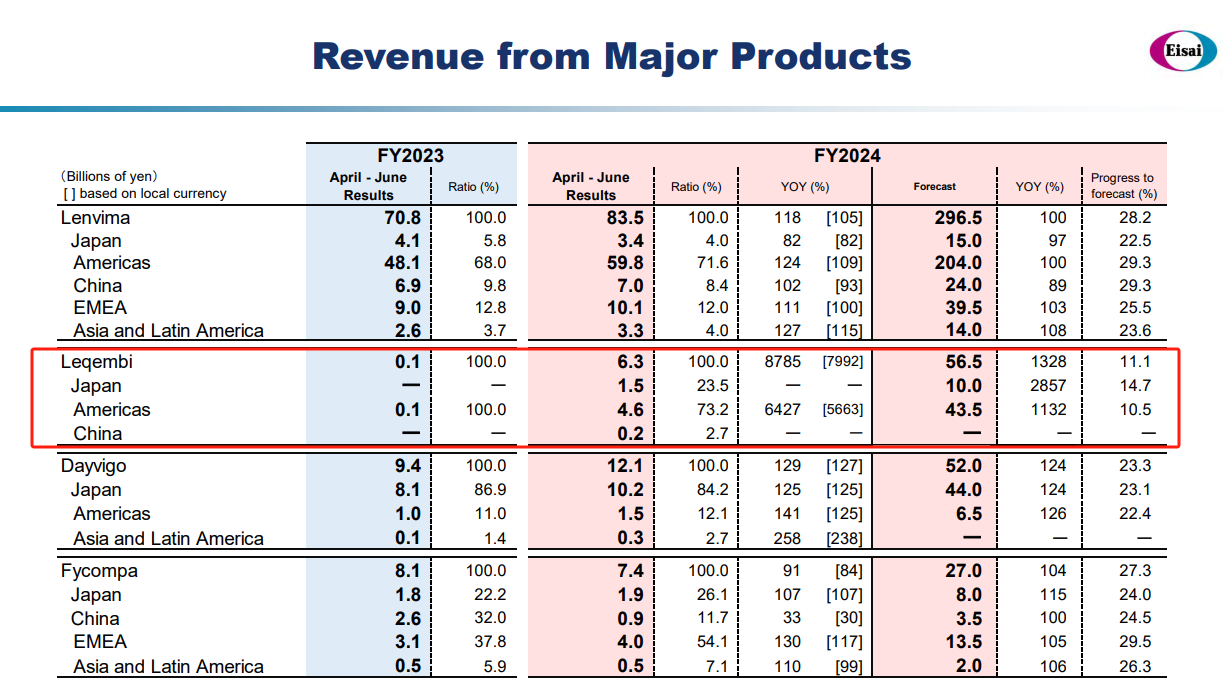
3L(Lenvima、Lemborexant和Leqembi)销售额的增长,实现了制药业务的收入增长,而由于去年同期收到的一次性预付款的影响,收入有所下降。FY2024 Q1,卫材的三款重磅产品Lenvima、Leqembi、Dayvigo共计收入1019亿日元(约6.95亿美元),同比增长27%。

FY2024 Q1,Leqembi销售额为63亿日元(约0.43亿美元),同比增长,其中美国市场收入46亿日元(约0.31亿美元),占比73%;日本市场收入15亿日元(约0.1亿美元),中国地区收入2亿日元(约0.01亿美元)。Leqembi在2024上半年共计收入91亿日元(约0.62亿美元),预计2024财年全年收入565亿日元(约3.9亿美元)。
仑卡奈单抗(Lecanemab)是一种人源化单克隆抗体,与可溶性Aβ原纤维具有较强的结合力。最早由Bioarctic AB发明;后转让权益于Biogen Inc (渤健)和Eisai Co Ltd (卫材)两大CNS巨头。
- 2023年1月,FDA在加速审批途径下批准了Leqembi治疗AD的上市申请。不过,只有在轻度认知障碍或轻度痴呆阶段且在病理学上确认存在Aβ的AD患者中才能进行Leqembi治疗。同年7月,Leqembi的加速批准成功转为完全批准。Leqembi的定价为2.65万美元/年。
- 此前2023年10月,仑卡奈单抗/Lecanemab通过海南省药品监督管理局审核落地海南博鳌乐城先行区,当时的定价每瓶3328元[ 200毫克(2 毫升)].
- 2023年12月13日,日本卫生部官员表示,阿尔茨海默病的新药lecanemab在日本定价298万日元/年,该药将于12月20日在日本正式上市。
- 2024年1月5日,中国国家药监局官(NMPA)批准卫材株式会社的阿尔茨海默病(AD)一类新药仑卡奈单抗注射液(中文商品名:乐意保;英文Leqembi)上市,用于治疗由阿尔茨海默病引起的轻度认知障碍和阿尔茨海默病轻度痴呆。7月11日,中国香港特别行政区政府卫生署已批准仑卡奈单抗用于治疗阿尔茨海默病。Leqembi国内定价为每瓶2508元(规格为200毫克/瓶),年治疗费用约18万元人民币。随着人口老龄化的加剧,到2032财年中国可能成为仅次于美国的第二大市场。

近日,卫材和渤健(Biogen)在2024年阿尔茨海默病协会国际会议(AAIC)上公布Leqembi的三年试验的最新结果。数据显示,与基线相比,接受lecanemab治疗的最早期阿尔茨海默病(AD)患者亚群中,51%在三年内表现出持续的认知和功能改善,这些患者在基线时大脑没有检测到Tau蛋白或Tau蛋白水平很低。
在核心研究和OLE的三年治疗中,与阿尔茨海默病神经影像学倡议(ADNI)组类似患者数据相较,lecanemab将基于CDR-SB的认知衰退幅度平均减少了0.95分。持续三年使用lecanemab治疗未观察到新的安全问题。大多数淀粉样蛋白相关成像异常(ARIA)发生在治疗的首六个月。六个月后,ARIA的发生率较低,与安慰剂组相似。

参考资料:https://www.eisai.com/ir/library/presentations/pdf/e4523_240802.pdf
相关扩展阅读:阿兹海默症药物临床最新进展
<END>
想要解锁更多药品信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药品各国上市情况、药品批文信息、销售情况与各维度分析、市场竞争格局、一致性评价情况、集采中标情况、药企申报审批信息、最新动态与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!

















































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论