
2023H1,Vertex 公司实现营业收入18.05亿美元,同比下降15.92%,实现归母净利润16.16亿美元,同比增长27.28%;研发费用15.28亿美元,同比增长27.23%。单看2023Q2,公司实现营业收入10.26亿美元,同比下降7.2%,环比增长31.76%;实现归母净利润9.16亿美元,同比增长13.0%,环比增长30.85%;研发费用7.86亿美元,同比增长30.93%,环比增长5.85%。
公司在手现金112.36亿美元,环比增长4.25%。整体来看,公司营收有所下降的主要原因是增加了对多个已进入中后期临床开发阶段项目的投资,增加了收购的知识产权和研发费用以及Vertex在全球推出疗法的成本。
产品收入
与2022年第二季度相比,产品收入增长14%,达到24.9亿美元,这主要得益于TRIKAFTA/KAFTRIO在全球多个国家独占鳌头,TRIKAFTA在2至5岁的囊性纤维化(CF)患儿中的上市成绩斐然。与2022年第二季度相比,2023年第二季美国净产品收入增长7%,达到15.1亿美元,美国以外地区增长26%,达到9.85亿美元。

产品收入(单位:百万美元)
IPR&D和SG&A费用
按照美国通用会计准则(GAAP)和非美国通用会计准则(Non-GAAP)计算的研发、收购IPR&D和SG&A费用分别为12亿美元和10亿美元,而2022年第二季度分别为8.77亿美元和7.50亿美元。
GAAP实际税率为21.2%,而2022年第二季度为20.9%。
Non-GAAP有效税率为 21.0%,而2022年第二季度为21.8%。
与2022年第二季度相比,GAAP和Non-GAAP的净收入分别增长了13%和9%。主要是由于强劲的收入增长和利息收入的增加部分抵消了中期和后期临床管道投资的增加,收购的知识产权和研发费用的增加,以及在全球范围内支持Vertex疗法的费用。
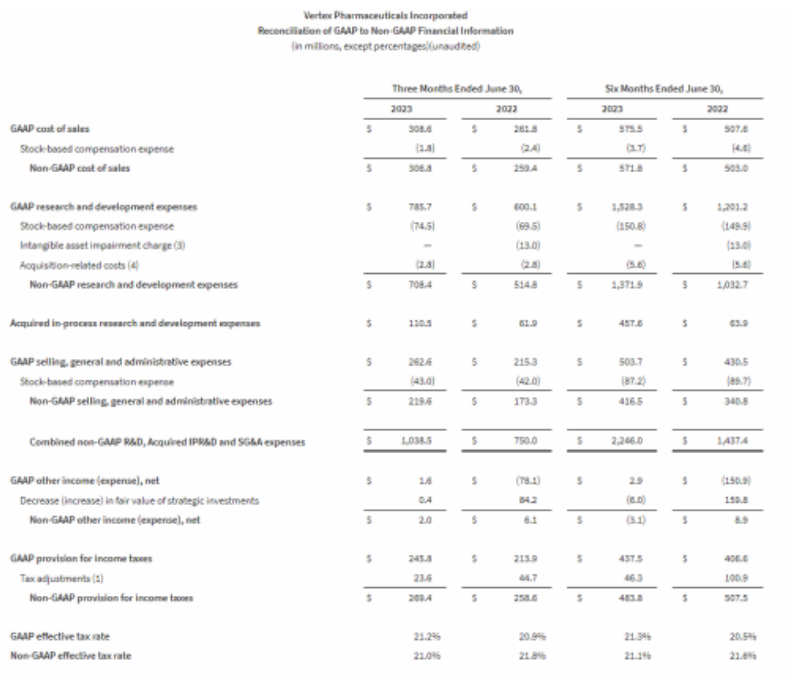
GAAP和非GAAP财务调节表(单位:百万美元)
截至2023年6月30日,现金、现金等价物和有价证券总额为126亿美元,而截至2022年12月31日为109亿美元。这一增长主要是由强劲的收入增长和运营现金流驱动的,但部分增长被我们向Entrada Therapeutics、CRISPR Therapeutics 和其他合作伙伴支付的款项、根据我们的股票回购计划回购的普通股以及所得税支付所抵消。
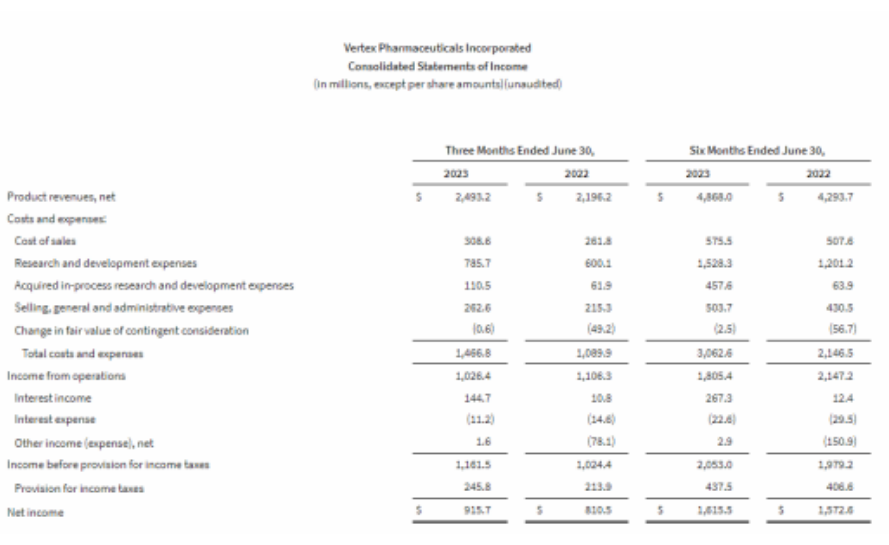
合并损益表(单位:百万美元)
2023年全年财政指导
Vertex公司将2023年全年CF产品收入指导从95.5 亿美元至97 亿美元上调至97 亿美元至98 亿美元,这一增长反映了TRIKAFTA / KAFTRIO在国际上多个国家的强劲业绩和TRIKAFTA在美国的持续表现的预期全年影响。这一指导包括外汇汇率变动带来的约150 个基点的负面影响。此外,Vertex公司还提高了2023年全年的GAAP和Non-GAAP研发、收购的IPR&D和SG&A费用指导。增加的原因是今年迄今为止发生的收购知识产权研发费用增加,其中包括向CRISPR Therapeutics支付的7000万美元里程碑式付款。

财务指引表
产品情况
用于SCD和TDT的Exagamglogene autotemcel (exa-cel):
Exa-cel是一种研究性、自体、体外CRISPR/Cas9基因编辑疗法,通过编辑患者自身的造血干细胞,使得患者血红细胞可以产生高水平的胎儿血红蛋白(HbF),以治疗TDT和SCD。目前正在与CRISPR Therapeutics合作开发该药物,有望成为治疗SCD和 TDT的功能性疗法。
FDA接受了exa-cel的生物制品许可申请(BLA),并指定2023年12月8日为SCD的处方药用户费法(PDUFA)行动日期,2024年3月30日为TDT的PDUFA目标行动日期。Exa-cel的SCD BLA获得了FDA的优先审查。在美国,exa-cel已被授予快速通道、再生医学高级疗法 (RMAT)、孤儿药和罕见儿科疾病称号。
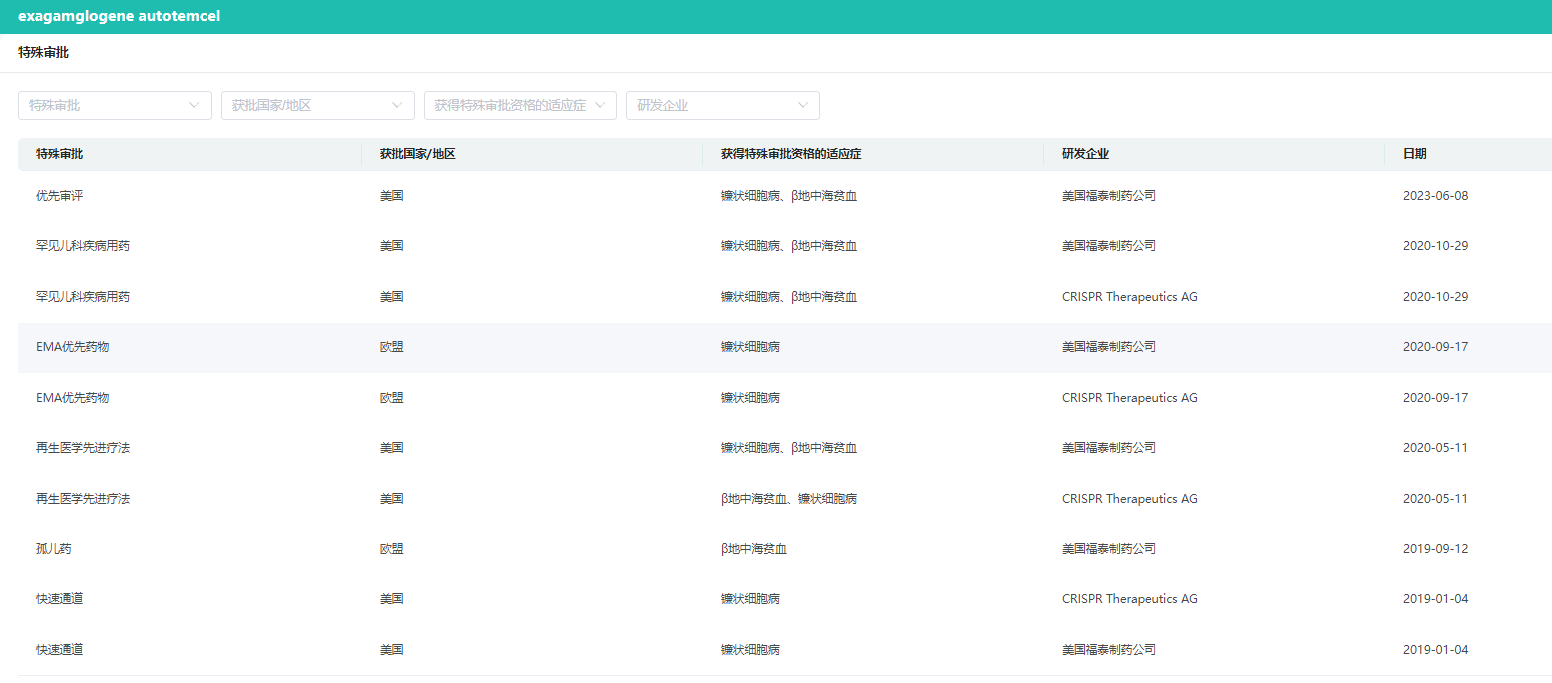
图片来源:药融云全球药物研发数据库
在今年6月举行的2023年欧洲血液学协会(EHA)年会上,Vertex公司公布了exa-cel治疗 SCD和TDT关键试验的积极中期结果,截止日期为2022年9月。这两项试验都在预先指定的中期分析中达到了主要终点和关键次要终点,数据继续显示出变革性、一致性和持久性的益处。Vertex 预计将在未来的医学大会上展示作为FDA申报基础的最新临床数据。

1/2/3期CLIMB-111和CLIMB-121研究的给药正在进行中,Vertex公司将继续在CLIMB-131长期随访研究中招募和跟踪患者。
Vanzacaftor/tezacaftor/deutivacaftor,治疗囊性纤维化的新三联疗法。
2022 年第四季度,Vertex完成了关键的SKYLINE 102和SKYLINE 103试验的入组工作,这两项试验评估了Vanzacaftor/tezacaftor/deutivacaftor相对于TRIKAFTA在12岁及以上CF 患者中的疗效和安全性(NCT0584444)。最近,Vertex 还完成了 Vanzacaftor/tezacaftor/deutivacaftor 用于 6-11岁CF儿童的RIDGELINE研究的入组工作。Vertex 预计在2023年底完成 SKYLINE和RIDGELINE研究,并在2024年初分享这些研究的结果。

VX-548 治疗急性疼痛:
Vertex 发现了多种NaV1.8的选择性小分子抑制剂,目的是创造一类新的止痛药有可能有效缓解疼痛的同时并不受阿片类药物和其他现有药物的限制。
Vertex 公司继续为其治疗中度至重度急性疼痛的主导化合物VX-548进行3期临床试验,包括腹部整形术和拇趾外翻切除术的两项随机对照试验以及一项单臂安全性和有效性试验。
VX-548研发进度查询

图片来源:药融云全球药物研发数据库
Vertex 预计将于2023年底完成关键项目,并于2023年底或2024年初分享这些研究的结果。在美国,VX-548 已获得治疗中度至重度急性疼痛的突破性疗法和快速通道认定。
研发管线
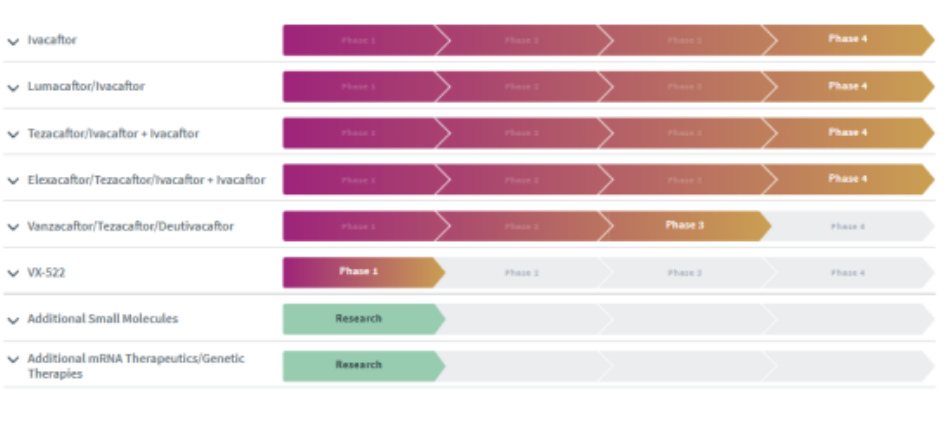
Vertex 正在针对严重疾病开发具有潜在变革性的小分子、mRNA、细胞和基因疗法等多元化产品线。临床开发项目的最新进展和预期进展概述如下。
囊性纤维化
Vertex 正在与 Moderna 合作开发 CFTR mRNA 疗法VX-522。该疗法旨在治疗导致肺囊性纤维化的根本病因,为全球约5000名无法从囊性纤维化跨膜传导调节因子(CFTR)调节剂中获益的CF患者提供治疗选择。Vertex公司正在招募患者参加VX-522的单次剂量递增(SAD)临床试验,预计将于2023年完成SAD试验并启动多次升剂量(MAD)研究。在美国,FDA 已授予 VX-522 快速通道认证。
重症镰状细胞病(SCD)和输血依赖性β-地中海贫血(TDT)
Exa-cel目前正在进行的IIIb期CLIMB-161试验,是为了支持在潜在批准和上市后的扩大生产规模。该试验将招募约12例TDT或SCD患者,年龄在12-35岁之间,患者将在输注后随访约1年。每位患者将被要求参加长期随访试验CLIMB-131。

急性和神经性疼痛
VX-548在糖尿病周围神经病变患者中的2期剂量范围研究已全部入组完成。为期12周的VX-548 2 期研究仍在继续给药阶段,Vertex 预计将于2023年底完成这项研究,并于2023年底或2024年初分享研究结果。
与其整体战略相一致,顶点对所有项目均采用组合方法,并通过疼痛研究和早期开发阶段推进其他 NaV1.8 抑制剂和NaV1.7 抑制剂。

1型糖尿病(T1D)
Vertex公司正在评估细胞疗法,使用干细胞衍生的、完全分化的、产生胰岛素的胰岛细胞来替代 T1D 患者中被破坏的内源性产生胰岛素的胰岛细胞,目标是开发一种潜在的功能性疗法来治疗这种疾病。

其他
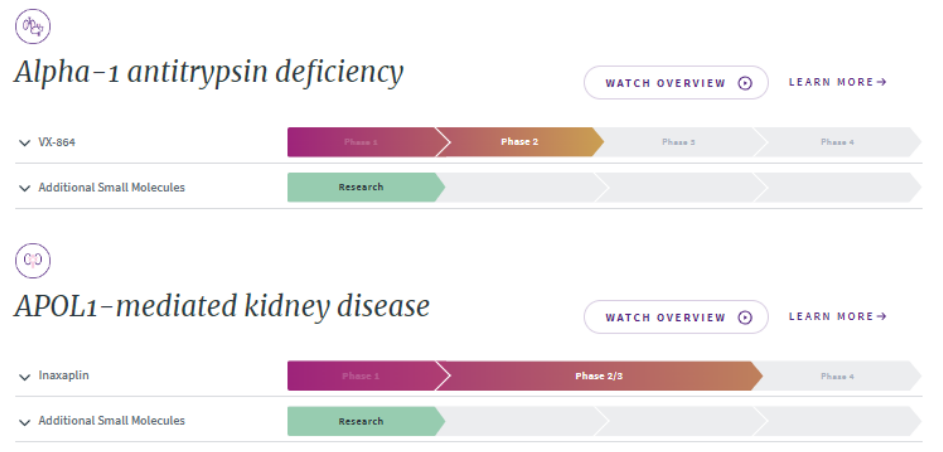
Vertex公司正致力于通过开发Z-AAT蛋白折叠的新型小分子校正剂来解决α-1抗胰蛋白酶 (AAT) 缺乏症的根本遗传原因,其目标是增加功能性AAT向血液中的分泌,同时解决AAT缺乏症的肺和肝脏两个方面。Vertex公司将在inaxaplin的关键项目中继续招募患者,这是一项针对APOL1 导致的肾脏疾病(AMKD)患者的2/3期临床试验,预计将于2023年完成2B期的剂量范围研究。此外,Vertex 公司还在推进肌营养不良症的临床前资产,包括杜氏肌营养不良症(DMD)和强直性肌营养不良症1 型(DM1)。
关于Vertex Pharmaceuticals
Vertex Pharmaceuticals是一家全球生物技术公司,投资于科学创新,为患有严重疾病的人创造变革性药物。 公司于1989年在马萨诸塞州剑桥市成立,其全球总部现位于波士顿的创新区,其国际总部位于伦敦,在北美、欧洲、澳大利亚和拉丁美洲设有研发基地和商业办事处。Vertex致力于开发和商业化用于治疗囊性纤维化,传染性疾病(包括病毒感染,例如流感和细菌感染),自身免疫性疾病(例如类风湿性关节炎,癌症,炎性肠病)和神经系统疾病(包括疼痛和多发性硬化症)的疗法,并将其商业化。
参考资料:
1.公司官网
2.药融云数据库
<END>
要解锁更多企业药品研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药品各国上市情况、药品批文信息、销售情况与各维度分析、市场竞争格局、一致性评价情况、集采中标情况、药企申报审批信息、最新动态与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!

















































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论