近日,中美华东(华东医药旗下子公司)的HDM1002片的新药临床试验(IND)申请获得美国FDA批准,同意开展I期临床试验,适应症为成人2型糖尿病。与此同时,药融云中国药品审评数据库显示,HDM1002片也于2023年5月15日获得CDE的获批临床(默示许可)。
HDM1002片是由中美华东自主研发并拥有全球知识产权的小分子药物,是具有口服活性、强效、高选择性的GLP-1受体小分子完全激动剂。截至目前,全球尚无口服小分子GLP-1受体激动剂药物上市。
临床前研究数据显示,HDM1002可强效激活GLP-1受体,诱导环磷酸腺苷(cAMP)产生,具有强效的改善糖耐受、降糖和减重作用并且显示出良好的安全性,是相对成熟稳定和安全的靶点。
据药融云数据库显示,目前在中国医院端市场的糖尿病用药TOP5生产企业排名前四的均为国外企业,分别是诺和诺德、赛诺菲、拜耳、礼来,中美华东排在第五位,稳居国内降糖药市场龙头地位。
医院端市场糖尿病用药TOP10生产企业

图片来源:药融云全国医院销售(全终端)数据库
中美华东有多个畅销的糖尿病化药,其中阿卡波糖片2015年的销售额已经接近15亿元关口,随后几年持续快速上涨,2019年的销售规模已达到37.72亿元,增长率为31.06%。但随着集采的逐步实施,对阿卡波糖片的原有医院市场影响较为明显,2020年阿卡波糖片在医院端的销售额为15.25亿元,同比下降59.6%。
一、糖尿病领域研发热点——GLP-1R激动剂
糖尿病领域是一个非常广阔的市场,药融云全国医院销售(全终端)数据库显示,我国医院端糖尿病药物市场一直保持稳步增长趋势,2021年销售规模达到591.19亿元,预计2024年各大终端或达到千亿级市场。在这一广阔市场中,GLP-1RA药物是增长速度较快的赛道。
GLP-1(胰高血糖素样肽-1)是人体胃肠道黏膜天然分泌的一种“肠促胰素”,GLP-1R是GLP-1的受体,在胰腺β细胞上表达。进食后,GLP-1通过激活GLP-1R,可以促进胰岛素的分泌,抑制胰高血糖素分泌,从而加快葡萄糖代谢,并能够延缓胃排空,通过中枢性的食欲抑制减少进食量,从而达到降低血糖、减重等作用。
但内源性GLP-1在血浆中的稳定性较差,容易被二肽基肽酶4(DPP-4)快速降解,半衰期不足2分钟,这就直接限制了天然GLP-1的应用场景。因此,催生了GLP-1类似物的研发。
全球GLP-1R靶点新药研发格局
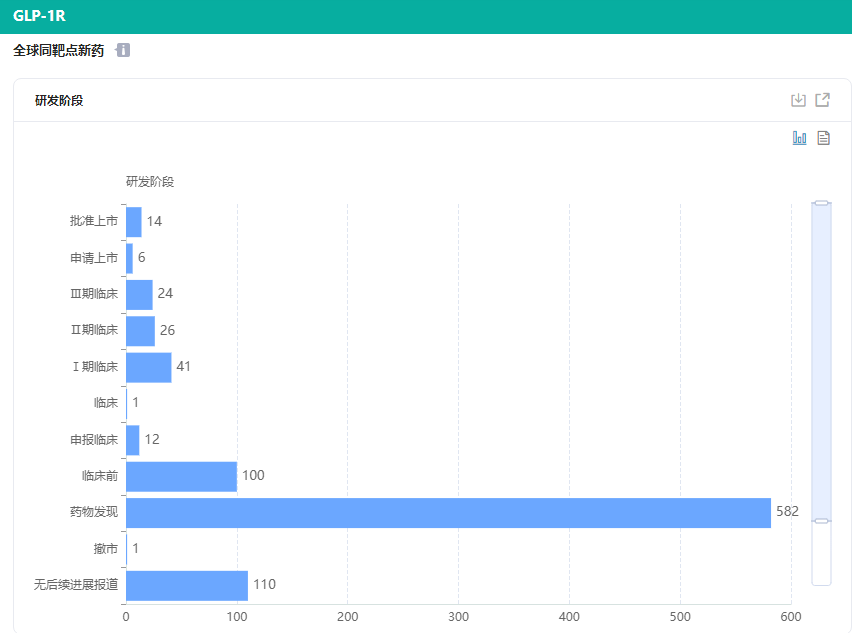
图片来源:药融云靶点格局数据库
多肽类GLP-1R激动剂通过模拟天然GLP-1来激活GLP-1受体,以葡萄糖浓度依赖的方式增强胰岛素分泌、抑制胰高糖素分泌。由于依赖葡萄糖浓度,其不仅具有显著的降糖疗效,同时又有低血糖发生率低的优点。
另外,由于GLP-1R不仅表达于胃肠和胰腺,因此GLP-1RA除了降糖、减少体重,还具有心血管保护的优势。优异的降糖效果以及明确的心血管获益,为长效GLP-1R激动剂赢得了最大的糖尿病市场份额。近年来其市场规模不断增长,2019年GLP-1RA的全球市场规模约109.7亿美元,占总体降糖药市场的21.5%;2020年GLP-1RA全球市场已超100亿美元,成为非胰岛素类降糖药中的第一大品种。
二、全球上市14款GLP-1R激动剂,口服制剂市场需求庞大
药融云全球药物研发数据库显示,截至目前,全球范围内已上市14款GLP-1R激动剂,包含10款创新药、2款改良型新药、2款生物类似药;在国内获批上市的有9款,包括每日1~2次的短效皮下注射剂(阿斯利康/礼来的艾塞那肽、诺和诺德利拉鲁肽等)以及每周1次的长效皮下注射剂(礼来的度拉糖肽、诺和诺德的司美格鲁肽等)。
全球获批上市的GLP-1R激动剂查询(部分,完整内容请登录“药融云数据库www.pharnexcloud.com/?mh”查看)

图片来源:药融云全球药物研发数据库
其中,国产的GLP-1R激动剂有2款,豪森药业的聚乙二醇洛塞那肽(长效)、仁会生物的贝那鲁肽(短效/速效)。
虽然已上市十余款GLP-1R激动剂,但是其市场却高度集中,最主要的三款GLP-1RA产品为诺和诺德的利拉鲁肽、司美格鲁肽以及礼来的度拉糖肽,占据着约90%的市场份额。
目前,除了诺和诺德的司美格鲁肽片/索马鲁肽(片剂,生物类似药)和阿斯利康的艾塞那肽(口服液体剂,改良型新药)为口服给药方式,其他均为注射给药。司美格鲁肽片,是全球首个GLP-1RA口服制剂(《糖尿病新药上市!首个国产利拉鲁肽获批,华东医药领跑GLP-1赛道》)。
GLP-1药物从短效迭代至长效,但每周1次的注射频率仍无法带来最佳的体验感。对于糖尿病、肥胖这类慢病,口服的便利性和依从性优势不言而喻。为了角逐庞大的GLP-1RA市场的口服地位,除了诺和诺德的多肽制剂改造,还有辉瑞、罗氏/礼来、VtvTherapeutics等口服小分子杂环GLP-1RA药物研发。
药融云数据库显示,目前小分子杂环GLP-1RA药物研发进度最快的是罗氏/礼来的orforglipron(LY3502970),现已开启了全球III期临床研究。
礼来LY3502970研发详情查询(部分展示)

图片来源:药融云全球药物研发数据库
除此之外,还有辉瑞的Danuglipron(PF-06882961)、VtvTherapeutics公司的TTP-273,均处于II期临床研究阶段。TTP273是vTv公司利用其小分子药物研发平台研发的非肽类、高选择性的全球创新口服小分子GLP-1受体激动剂。华东医药于2017年12月引进了TTP273在16个国家和地区的开发、生产及商业化独家授权许可,其中中国授权专利有效期到2030年。
在国内方面,目前已有9款口服小分子GLP-1RA创新化药在研,涉及的药企包括恒瑞医药、华东医药、信立泰、必贝特医药、先为达生物、诚益生物、安博生物等。
三、GLP-1R激动剂的研发方向——双靶点激动剂
除了口服制剂的研发方向,GLP-1RA目前研发方向还集中在双靶点激动剂方面。单一靶点激动剂在治疗糖尿病时存在一些限制,如其生物利用度低、耐受性下降等;因此,双靶点激动剂作为一种新的治疗策略被提出,其具有同时调节多个靶点的能力,从而可以取得更好的治疗效果。
目前,已有一些双靶点激动剂进入了临床试验阶段,并在糖尿病治疗领域取得了一定的成果。主要集中于GLP-1R/GIPR和GLP-1R/GCGR等双激动剂的研发。
1.GLP-1R/GIPR双靶点激动剂
GIPR(Glucose-dependent insulinotropic polypeptide receptor)是一种与胰岛素相关的G蛋白偶联受体,与GLP-1R具有相似的生物学功能。因此,开发同时作用于GLP-1R和GIPR的双靶点激动剂可以提高胰岛素分泌、抑制胰岛素分泌不足等作用,从而改善治疗效果。
目前,已有一些GLP-1R/GIPR双靶点激动剂进入了临床试验阶段,如Dual-agonist-1、RM-131,以及礼来的tirzepatide(奇普塔地)等。Tirzepatide是一种单分子,可激活人体GIP和GLP-1两种天然肠促胰素受体。礼来的Tirzepatide于2022年5月日在FDA 获批,适用于在饮食控制和运动基础上,改善成人2型糖尿病患者的血糖控制。
tirzepatide在研适应症查询
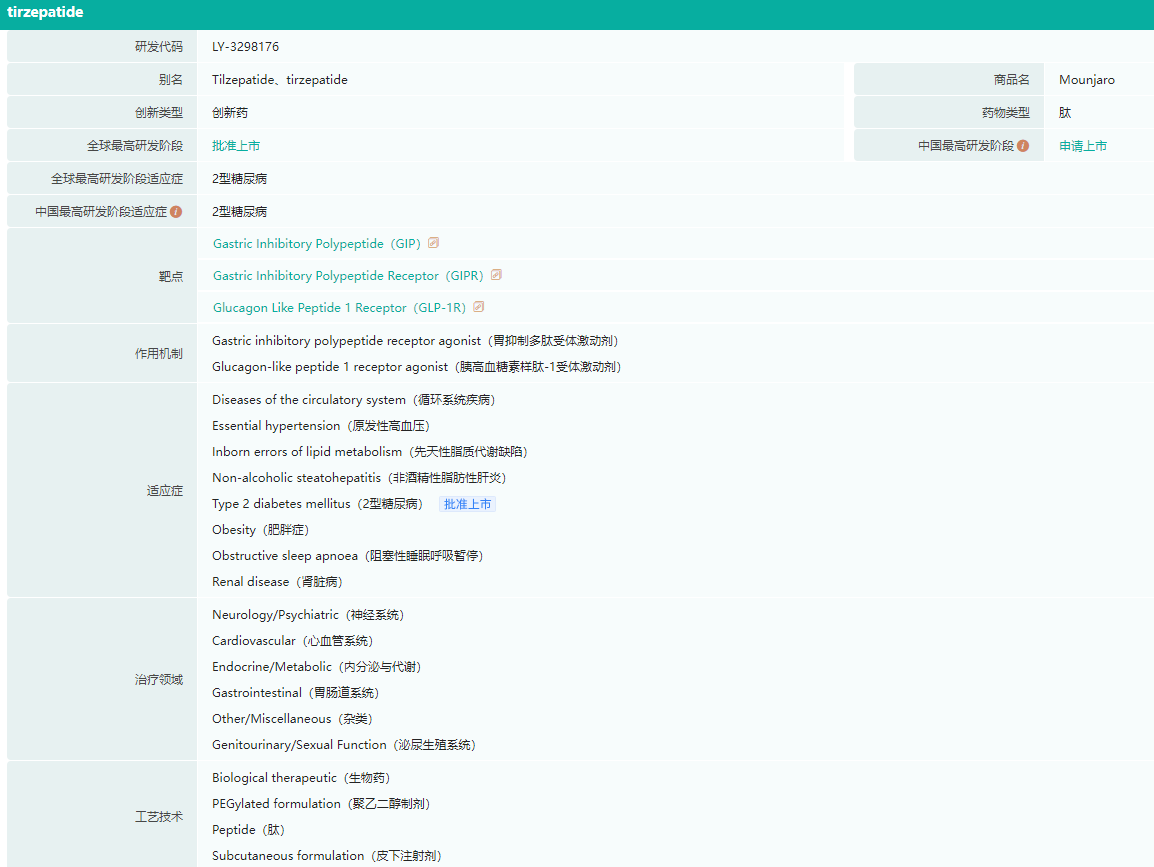
图片来源:药融云全球药物研发数据库
药融云数据库显示,Tirzepatide对超重伴有体重相关合并症或肥胖成人的治疗目前处于III期临床开发阶段;对于肥胖和/或超重伴有射血分数保留的心衰(HFpEF)、阻塞性睡眠呼吸暂停 (OSA) 和非酒精性脂肪性肝炎 (NASH) 患者的潜在治疗也在研究过程中。
国内企业也在积极布局,如华东医药、豪森药业、恒瑞医药等也有GLP-1R/GIPR双靶点激动剂的布局。
2.GLP-1R/GCGR双靶点激动剂
GCGR(Glucagon receptor)也是一种与GLP-1R相似的受体,在肝脏中通过调节糖原分解和糖异生来影响血糖水平。GLP-1R/GCGR双靶点激动剂可以同时抑制胰高血糖素的分泌和促进胰岛素的分泌,从而起到更好的降低血糖的作用。
目前,已经有一些GLP-1R/GCGR双靶点激动剂进入临床阶段,如阿斯利康的MEDI-0382(Cotadutide)、NGM生物制药的NGM313、赛诺菲公司的SAR425899等。
Cotadutide 2型糖尿病的全球研发进展
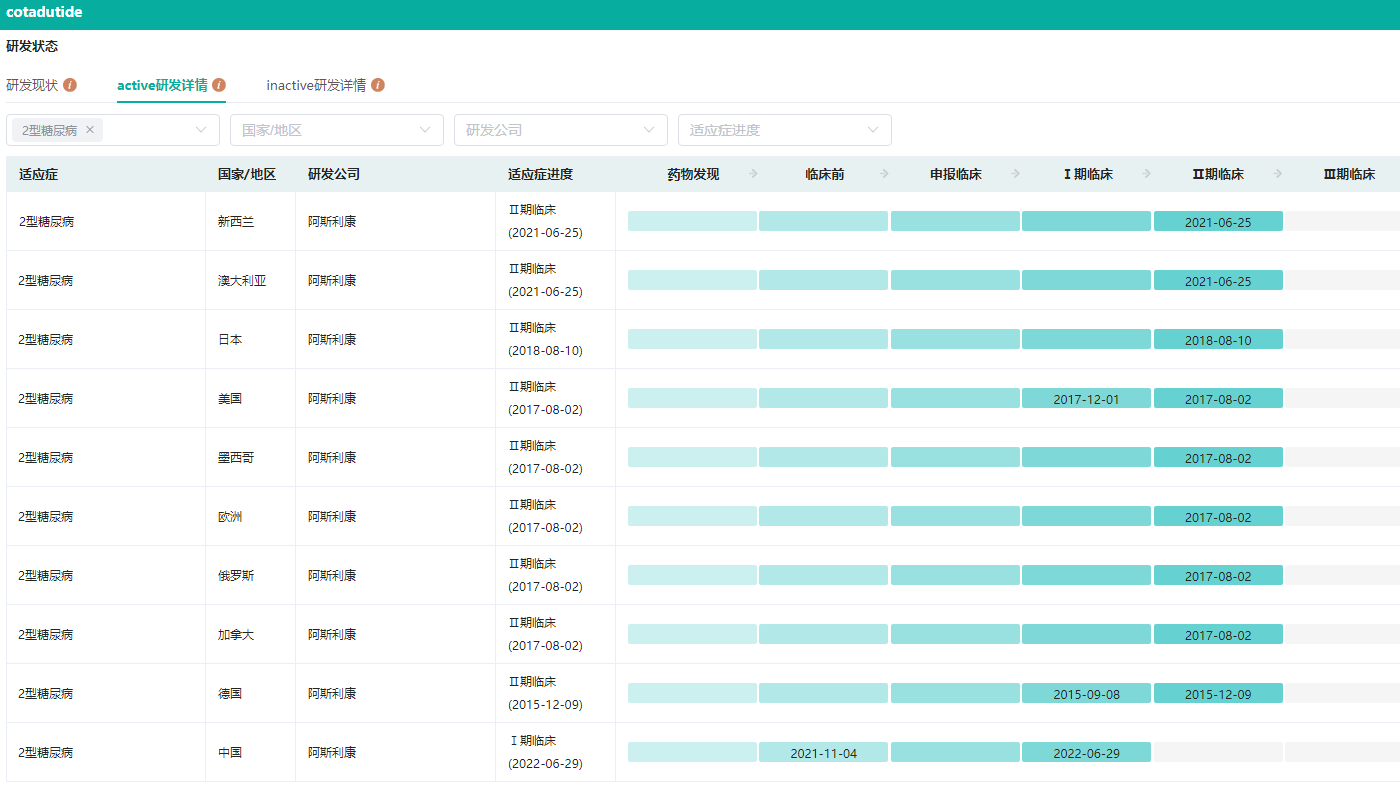
图片来源:药融云全球药物研发数据库
一些研究还发现,GLP-1R/GCGR双靶点激动剂可能对抗炎症反应和脂肪肝等代谢性疾病有益。因为GLP-1R/GCGR双激动剂已成为治疗糖尿病、肥胖、NASH(非酒精性脂肪肝)等疾病的一个新方向。
目前,阿斯利康、赛诺菲、礼来、默沙东、诺和诺德等均布局了GLP-1R/GCGR双激动剂的研发,国内的启赋药业、国药集团、辰欣药业、信达生物、信立泰等企业也有布局。
GLP-1R当下已成为全球热门靶点,除了治疗2型糖尿病,GLP-1R靶点在其他领域也有应用潜力,例如肥胖症、胰岛素抵抗、心血管疾病等。未来,GLP-1R靶点的研究可能会涉及到更多的领域和疾病类型,研发前景非常广阔。
想要解锁更多药物研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!

<END>












































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论