二十年等待
2023年3月6日,我国目前获批的首个靶向治疗EGFR 20号外显子插入突变(EGFR exon20 Insertion+)非小细胞肺癌的口服创新药物琥珀酸莫博赛替尼(mobocertinib)胶囊(以下简称“莫博赛替尼”)开出全国首张处方,莫博赛替尼在国内正式进入临床应用阶段,标志着中国EGFR 20号外显子插入突变的肺癌患者结束了二十年来“无特异性靶向治疗药可用”的困境,正式迎来靶向治疗新时代。

【商品名】:安卫力®
【通用名】:琥珀酸莫博赛替尼胶囊
【规格】:40mg*14S*8板
【适应症】:适用于含铂化疗期间或之后进展且携带表皮生长因子受体(EGFR)20号外显子插入突变的局部晚期或转移性非小细胞肺癌(NSCLC)成人患者
【价格】:药融云数据,www.pharnexcloud.com/?zmt-mhwz监测显示,本品定价37588元人民币/盒
EGFR 20号外显子插入突变是EGFR靶点的第三大突变。由于EGFR20号外显子插入突变形成的空间位阻,导致了药物结合口袋变小,且该突变同野生型的EGFR结构高度相似,使得该靶点药物研发困难重重。因此,在该靶点自发现以来的二十年来,始终没有靶向治疗方案,临床上针对这一疾病的治疗至今仍以化疗为主,且此前国内已获批的EGFR-TKI及免疫治疗对改善此类靶点突变患者的生存获益均效果不明显。
相对于常见EGFR突变,EGFR 20号外显子插入突变晚期非小细胞肺癌患者的生存预后更差。根据一项真实世界数据显示,在缺乏针对性有效治疗情况下,晚期EGFR 20号外显子插入突变患者二线及后线治疗客观缓解率(ORR)低于10%,PFS仅为3.7个月,OS仅为13.6个月。患者病情恶性程度高,预后差,5年生存率仅为8%,临床上对针对性的靶向治疗药物有着十分紧迫的未满足需求。
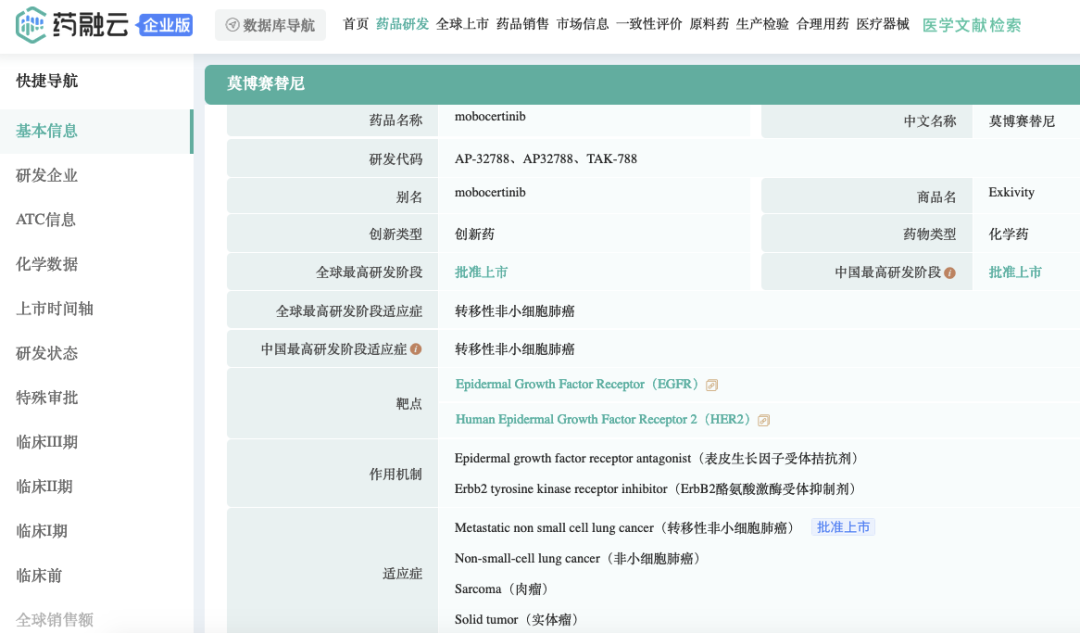
截图来源:药融云全球药物研发数据库
莫博赛替尼是武田制药研发并引进的全球首款也是目前唯一获批的治疗EGFR 20号外显子插入突变晚期非小细胞肺癌的口服靶向药物。本品AP32788/TAK-788,相关专利WO-2015195228;最早由Ariad Pharmaceuticals Inc研发。在2017年2月,武田制药以52亿美元高价收购Ariad Pharmaceuticals。

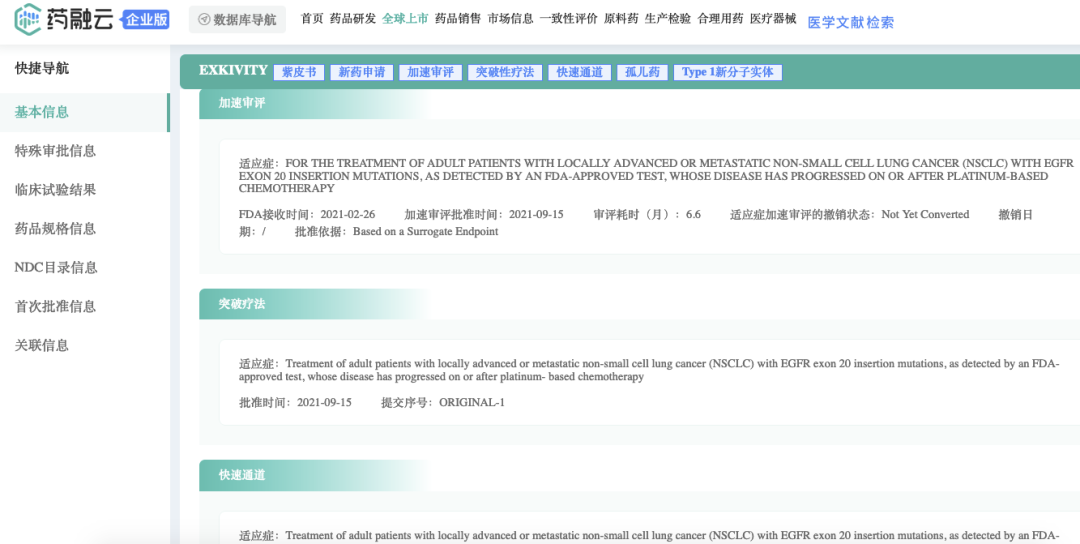
截图来源:药融云全球药物研发数据库
于2023年1月获得国家药品监督管理局(NMPA)批准正式进入中国(国药准字HJ20230001),适用于治疗含铂化疗期间或之后进展且携带表皮生长因子受体(EGFR)20号外显子插入突变的局部晚期或转移性非小细胞肺癌(NSCLC)成人患者(《 5款重磅新药获批上市,罗氏、诺华、百克为国内患者带来福音!》)。临床研究结果显示,经25.8个月的长期随访,莫博赛替尼可将含铂化疗经治患者的中位无进展生存期(mPFS)提高到7.3个月,中位总生存期(mOS)延长至20.2个月,填补了该领域临床治疗的长期空白。

同济大学附属上海市肺科医院肿瘤科主任周彩存表示:“在肺癌患者群体中,EGFR 20号外显子插入突变晚期非小细胞肺癌患者非常特殊。相较于敏感基因突变的肺癌患者能够实现五年甚至更长的生存期,该领域患者目前主要依赖化疗的治疗手段,其中位生存期仅有一年。随着莫博赛替尼正式进入临床应用阶段,患者对于针对性靶向药物的迫切需求得到填补。莫博赛替尼优异的临床研究成绩、所具有的突破性意义,为EGFR 20号外显子插入突变晚期非小细胞肺癌患者开启了新的靶向治疗时代。”
据药融云数据显示,国内部分表皮生长因子受体20号外显子插入突变(EGFR 20ins)在研新药有:迪哲医药的舒沃替尼、福沃药业FWD1509 MsOH、浦合医药、津曼特(石药集团)、艾力斯、再鼎医药CLN-081等等。
关于武田制药
武田制药(东京证券交易所股票代码:4502)(纽约证券交易所股票代码:TAK)是一家总部位于日本、以价值观为基础、以研发为驱动的全球生物制药公司。武田致力于将科学研发成果转化为高度创新药品,为患者的健康生活和美好未来保驾护航。武田专注于四大治疗领域的药物研发:肿瘤、消化、神经科学及罕见病领域,并针对血液制品及疫苗领域进行专项研发投入。我们始终专注于高度创新药物的研发,通过开拓全新治疗方案、增强合作研发引擎实力,打造一条稳健且形式多样的产品管线,助力改善人们的生活。
此文仅用于向医疗卫生专业人士提供科学信息,不代表平台立场
参考:
NMPA/CDE;
药融云数据,vip.pharnexcloud.com/?zmt-mhwz;
FDA/EMA/PMDA;https://www.takeda.com;
www.takeda.com/newsroom/newsreleases;
https://www.accessdata.fda.gov/scripts/cder/daf/index.cfm?event=BasicSearch.process&ApplNo=215310;
https://www.cancernetwork.com/view/mobocertinib-receives-fda-approval-for-previously-treated-nsclc-with-egfr-exon-20-insertion-mutations;
Mobocertinib: First Approval:https://pubmed.ncbi.nlm.nih.gov/34716908;
https://www.takeda.com/newsroom/newsreleases/2020/takeda-announces-u.s.-fda-breakthrough-therapy-designation-for-mobocertinib-tak-788-for-the-treatment-of-nsclc-patients-with-EGFR-exon-20-insertion-mutations;
2022年欧洲肿瘤内科学会(ESMO)年会:Ramalingam SS, Zhou C, Kim TM, et al. 2022ESMO,988P;
CSCO非小细胞肺癌诊疗指南2022;等等。
想要解锁更多药品信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药品各国上市情况、药品批文信息、销售情况与各维度分析、市场竞争格局、药企申报审批信息、最新动态与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!

<END>







































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论