
眨眼间,2022已到年底,相信今年大家都经历了很多事情,有自然而然的,也有在意料之外的,但总体来说应该是收获满满,硕果累累的一年。2022年生物医药领域喜报频传,据统计今年国家药品监督管理局(NMPA)共批准了50多款新药上市,其中在2022年的最后一个月,国内第二款GD2单抗卡点获批,为国内“儿童肿瘤之王”患儿送来“姗姗来迟”的福音。
一、国内第二款GD2单抗新药上市,神经母细胞瘤患儿迎来“福音”
根据NMPA发布的批准证明文件送达信息公示,赛生药业的那昔妥单抗注射液获批新药上市,与粒细胞-巨噬细胞集落刺激因子(GM-CSF)联合给药,适用于伴有骨或骨髓病变,对既往治疗表现为部分缓解、轻微缓解或疾病稳定的1岁及以上儿童或成年复发性或难治性高危神经母细胞瘤患者。
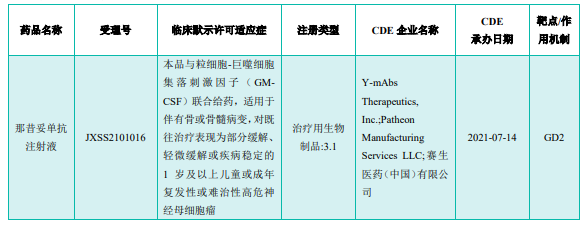
截图来源:药融云《医药行业观察周报》
神经母细胞瘤素有“儿童肿瘤之王”之称,顾名思义,是说这个病治疗难度大,治疗效果不好,生存率低。神经母细胞瘤是儿童最常见的颅外肿瘤,是1岁以下儿童最常见的实体恶性肿瘤,约占6-10%的儿童肿瘤,15%的儿童肿瘤死亡率。中国大概每年新确诊神经母细胞瘤患儿2500-2700例左右。这个病有一定年龄特点,约40%的患者在1岁前发病,中位发病年龄在17个月左右,年龄越大,发病率越低。首都儿科研究所附属儿童医院普通(新生儿)外科陈兴海表示,早发现、早诊断,及时接受系统的规范化的治疗是预防神经母细胞瘤的关键。
经药融数据库查询显示,那西妥单抗是一款靶向神经节苷脂GD2的人源化单克隆抗体,此次获批新药上市,是国内的第二款GD2单抗。GD2抗原表达在神经外胚层生成的肿瘤表面,包括神经母细胞瘤、黑色素瘤和骨肉瘤等肿瘤。那昔妥单抗通过与肿瘤细胞表面的GD2结合,能够引起抗体介导的细胞毒性反应并激活补体系统,从而达到杀伤肿瘤的效果。
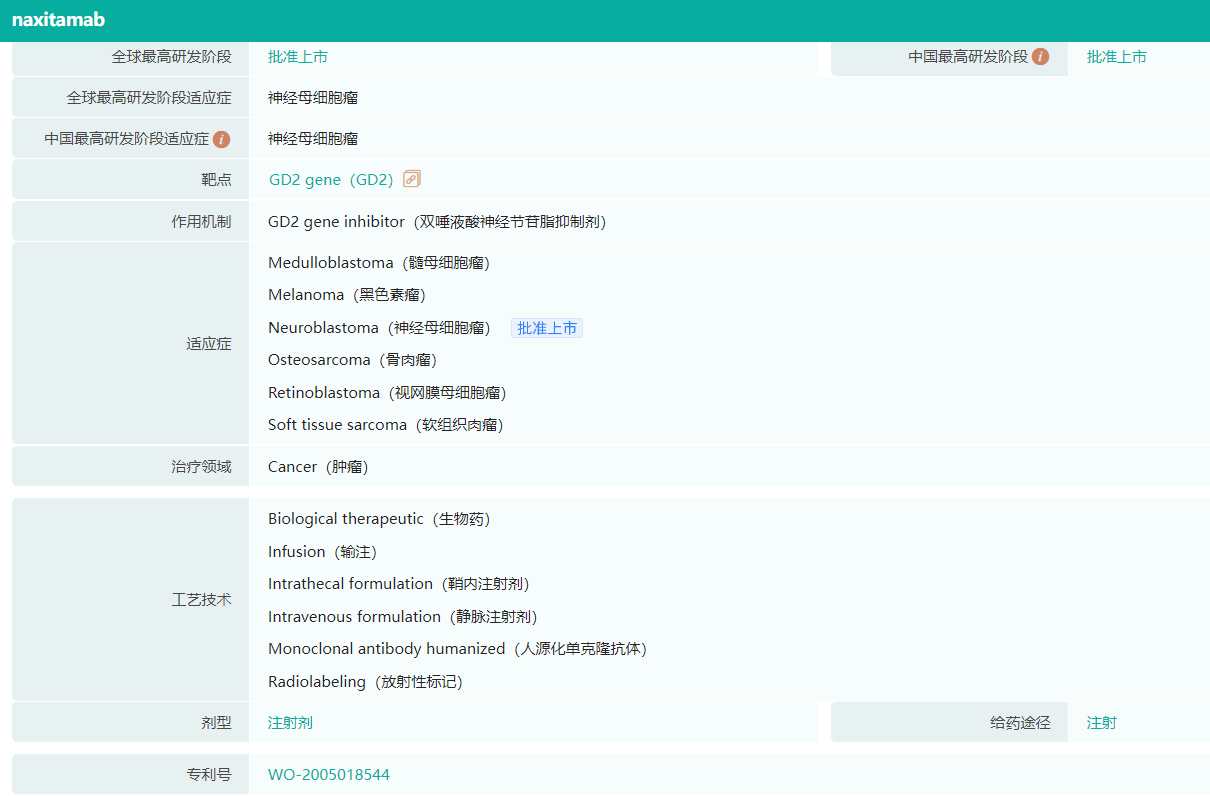
截图来源:药融云全球药物研发数据库
该GD2单抗早先已于2020年11月底在美国通过了新药上市申请,由Y-mAbs Therapeutics Inc申报,获得了FDA认证的突破性疗法、优先审评、罕见儿科疾病用药,以及加速审批上市。除此之外,该药还获得了在中国的“绿色通道”——优先审评认证。该“绿色通道”是国家为鼓励研究和创制新药、解决临床急需短缺药品、应对疫情突发状况等而设立的药品快速上市通道,是以临床价值为导向的,被纳入产品代表着当下医药的技术前沿以及未来产业发展的重点与方向。近年来,我国药品上市许可优先审评审批制度不断优化与完善,越来越多的重磅创新产品通过这一“绿色通道”加快了新药上市进程。
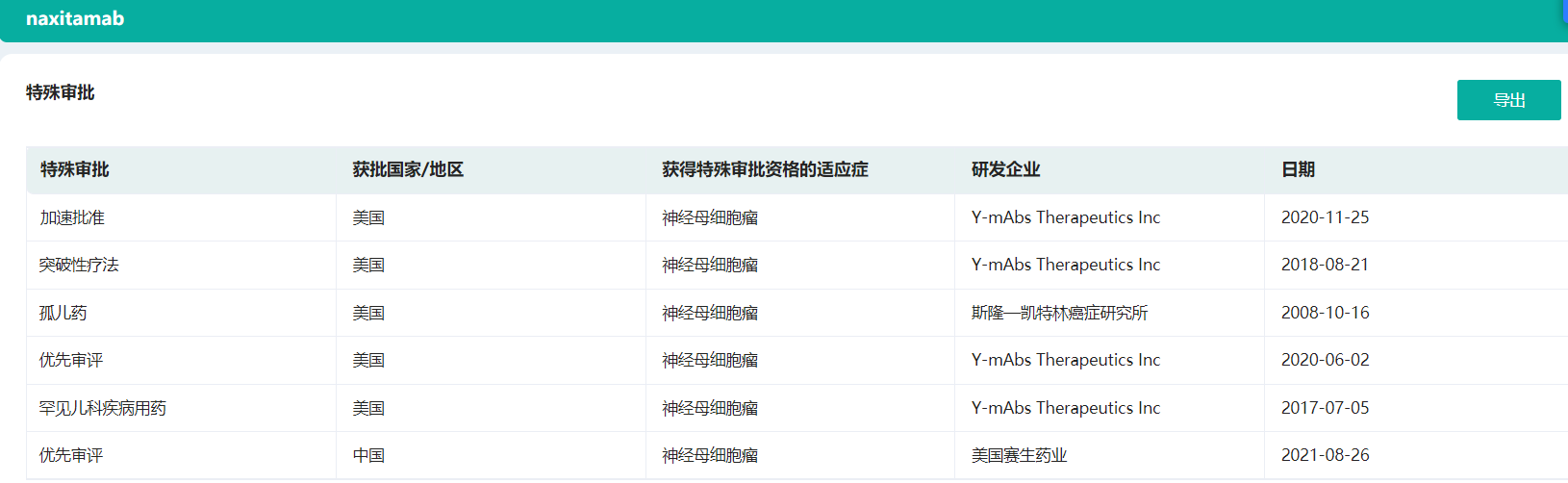
截图来源:药融云全球药物研发数据库
据药融云统计,赛生药业在中国递交的关于那昔妥单抗注射液进口生物药新药申请销售申请,从被药申中心(CDE)承办,到此次获批新药上市,共用时512天,重要节点事件如下:
2021年7月14日,赛生药业递交的那昔妥单抗注射液进口申请被CDE承办;
2021年8月26日,那昔妥单抗注射液正式被纳入优先审评,拟定适应症为:本品与粒细胞-巨噬细胞集落刺激因子(GM-CSF)联合给药,适用于伴有骨或骨髓病变,对既往治疗表现为部分缓解、轻微缓解或疾病稳定的1岁及以上儿童或成年复发性或难治性高危神经母细胞瘤患者;
2021年12月29日,CDE寄发通知;
2022年4月21日,进入补充资料任务;
2022年6月10日,CDE寄发通知;
2022年8月10日,进入第二轮补充资料任务;
2022年12月8日,CDE批准新药上市,国内可进口那昔妥单抗注射液,药品批文:国药准字SJ20220019
那昔妥单抗注射审评时间轴(部分,微信搜索"药融云小程序"查看更多)
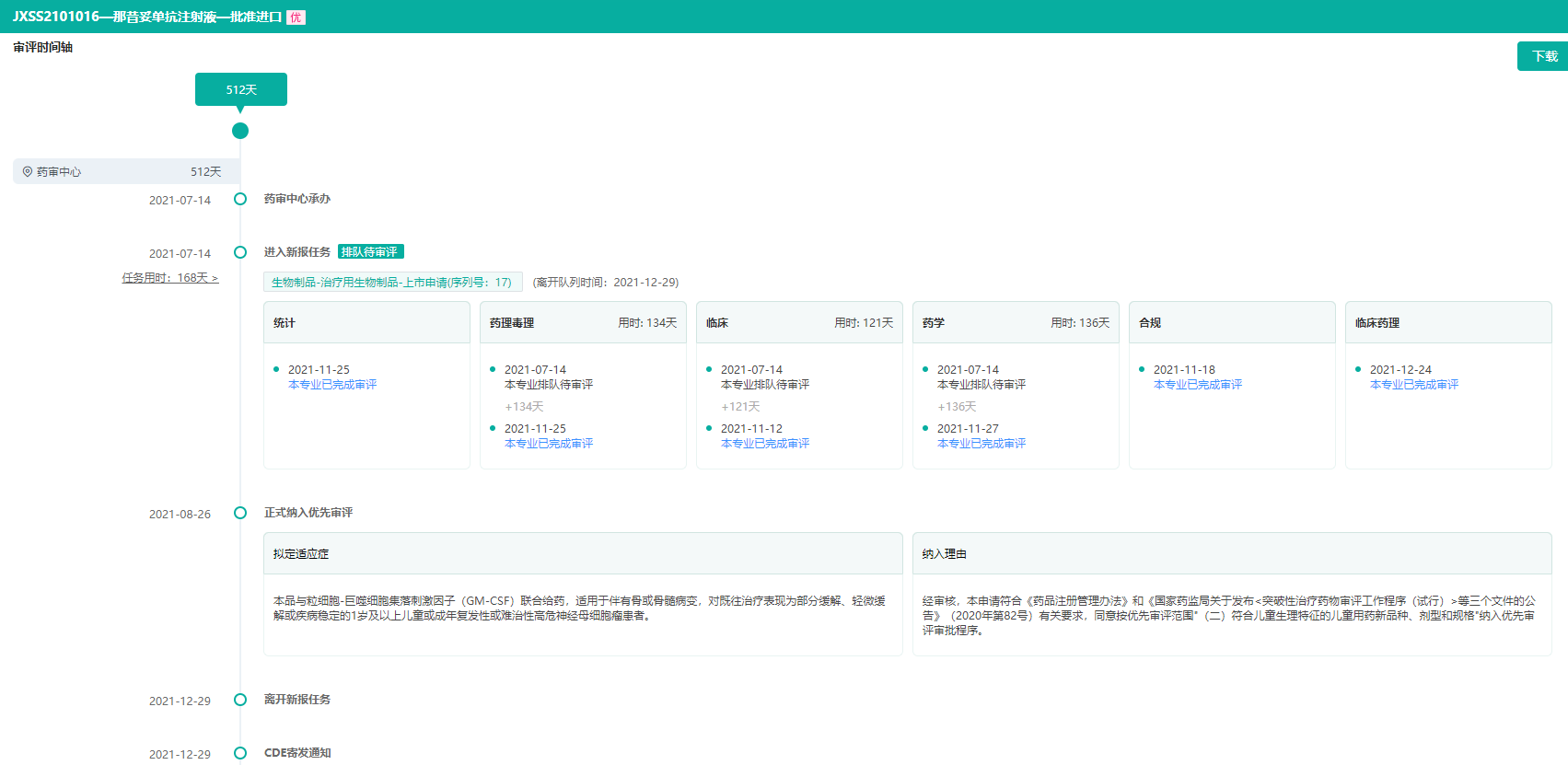
截图来源:药融云中国药品审评数据库
naxitamab最早是由Memorial Sloan Kettering Cancer Center(斯隆—凯特林癌症研究所)研发的GD2单抗,2015年8月授权给Y-mAbs Therapeutics Inc在全球的药物开发/商业化许可权。2020年12月18日,Y-mAbs Therapeutics Inc又将naxitamab在中国、中国香港、中国澳门、中国台湾的药物开发/商业化许可权授权给赛生药业,首付金额2000万,预计支付总金额1.2亿美元。
Y-mAbs Therapeutics与赛生药业关于naxitamab的医药交易信息(部分)
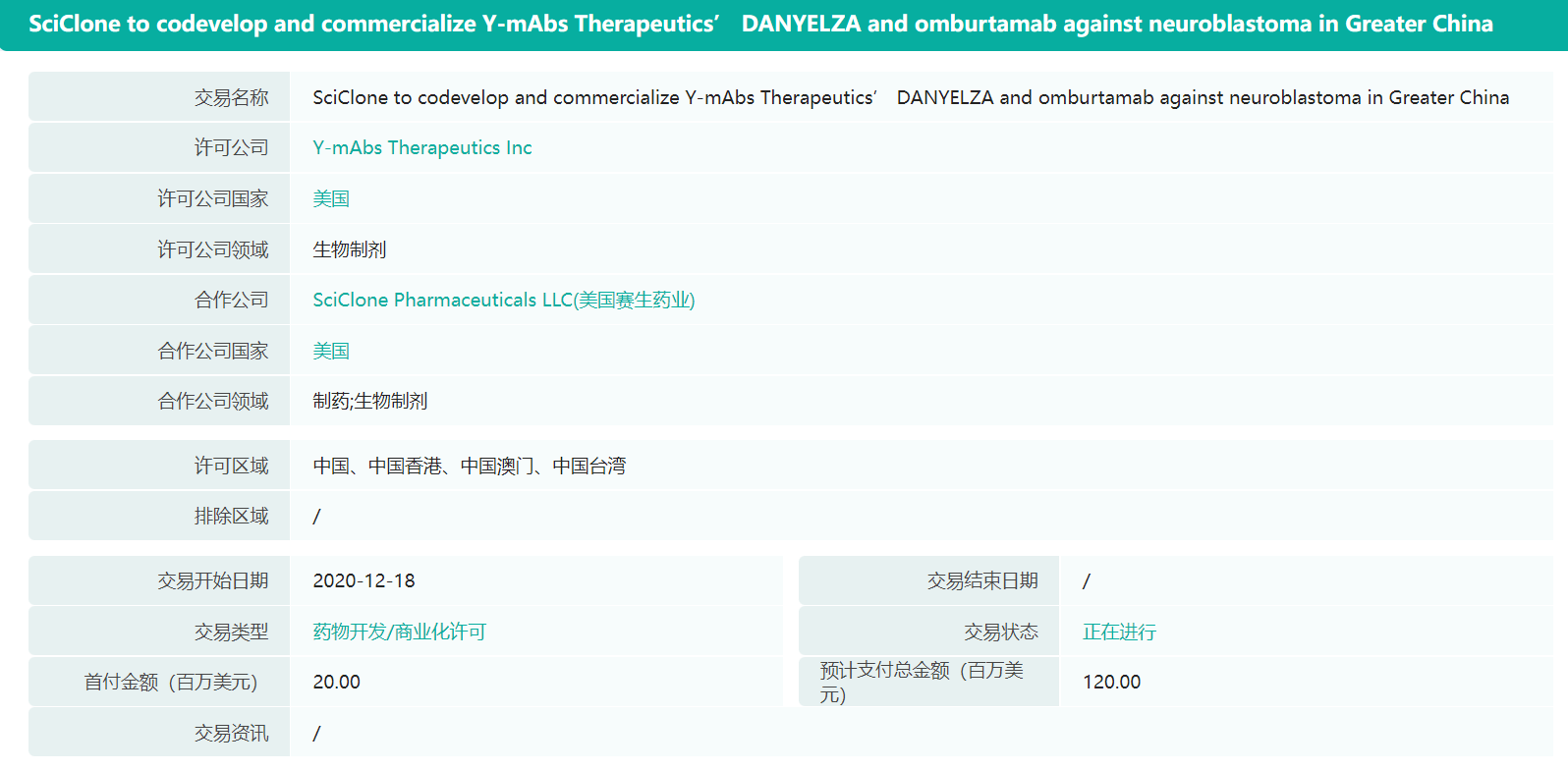
截图来源:药融云全球医药交易数据库
二、极具潜力的GD2单抗,达妥昔单抗领头
据药融云靶点格局数据库显示,目前布局GD2靶点的企业少之又少,在全世界范围内也只有三款新药上市,分别为达妥昔单抗、达妥昔单抗β、以及那昔妥单抗,且都为单抗产品。2021年8月,百济神州从EUSAPharma引进的达妥昔单抗β在国内获批新药上市。截至今日,国内共有两款GD2单抗获得批准进口。
GD2单抗全球新药上市情况
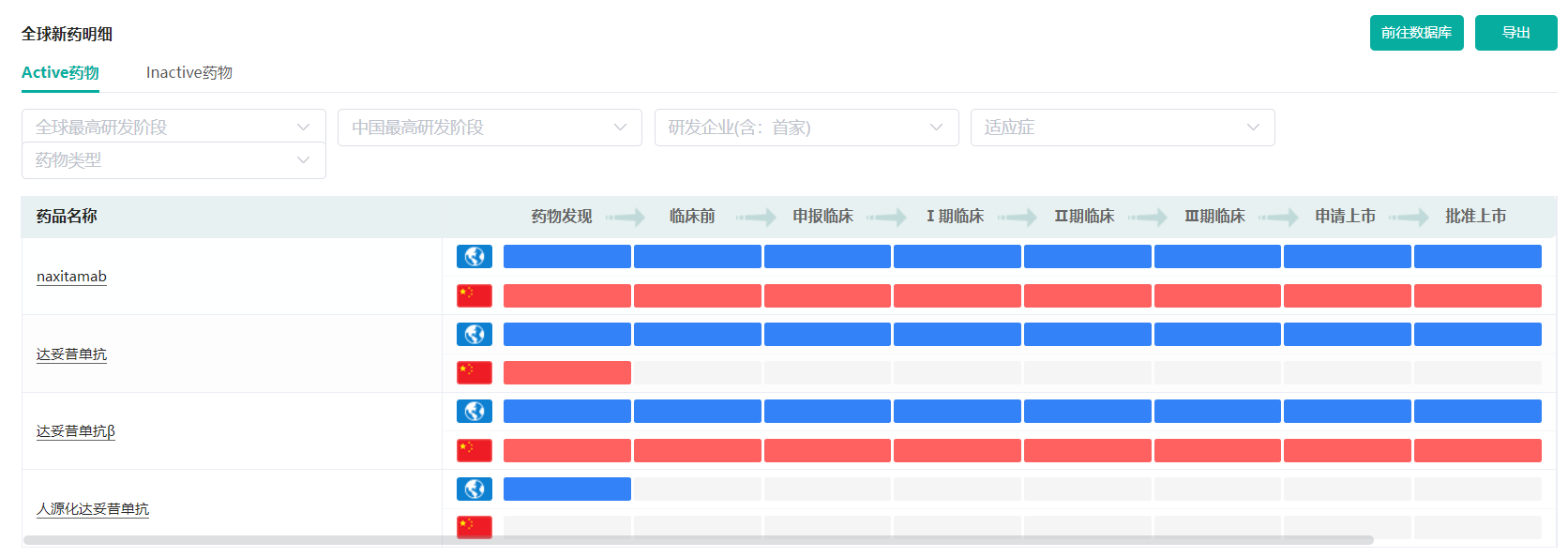
截图来源:药融云靶点格局数据库
据药融云统计,达妥昔单抗自从获批新药上市、正式销售以来,其销售额一路高歌猛进,保持着持续递增趋势。其中,在2019年首次突破亿元大关,2021年在全球的销售额同比增长了64.61%,达到2亿美元。总体来看,达妥昔单抗潜力巨大,很有发展前景,是GD2单抗药物的领头羊。
达妥昔单抗全球销售情况
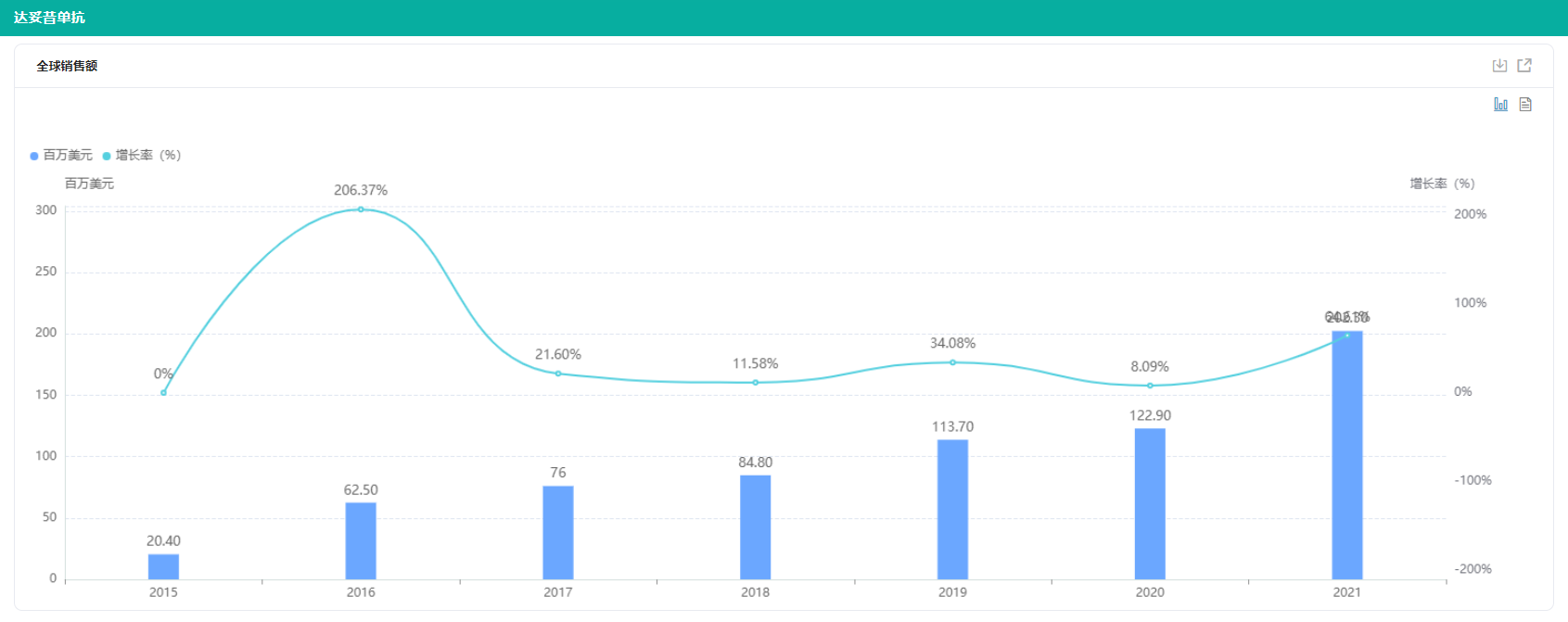
截图来源:药融云全球药物研发数据库
三、研发永不止步,为更多患者谋福音
在适应症方面,目前已上市的3款GD2单抗都是针对神经母细胞瘤的。不过,拿下新药上市并不意味着药物研发到达了终点,"永不止步,勇攀高峰”这句话也适用于药物研发,药企开发药物的主要目的是为了治疗更多的疾病,满足更多的临床需求,最终造福更多患者。
据药融云数据库显示,Y-mAbs Therapeutics Inc对其已取得新药上市的GD2单抗(那西妥单抗)还有在开展关于黑色素瘤、软组织肉瘤、视网膜母细胞瘤、骨肉瘤以及髓母细胞瘤的临床试验,目前在美国都已推进到2期。美国国家癌症研究所也还在对达妥昔单抗在澳大利亚、波多黎各、加拿大、新西兰等地开展关于骨肉瘤的2期临床试验。
GD2单抗适应症分析
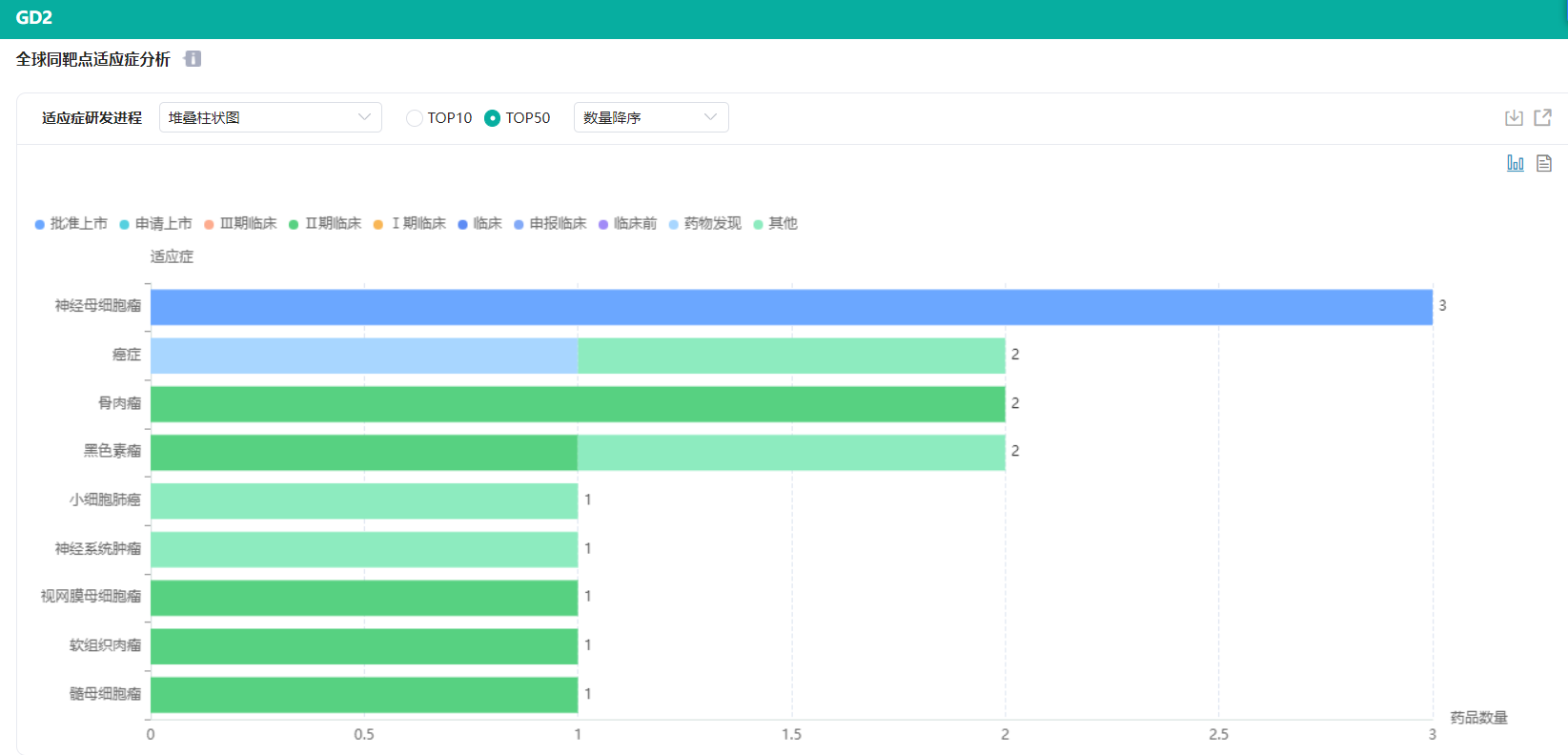
截图来源:药融云靶点格局数据库
想要解锁更多药物研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、申报审批情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!

<END>






















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论