
10月21日批准件:四川汇宇制药的乙酰半胱氨酸注射液以化药3类首家过评,规格30ml:6g。

这个品命运多舛,本号曾多次进行分析。
据摩熵医药(原药融云)数据库统计,自2016年以来,共30条一致性评价受理号,截至目前,仅汇宇一家过评,已累计有13家企业的14个一致性评价受理号先后被毙,剩余15条在审。
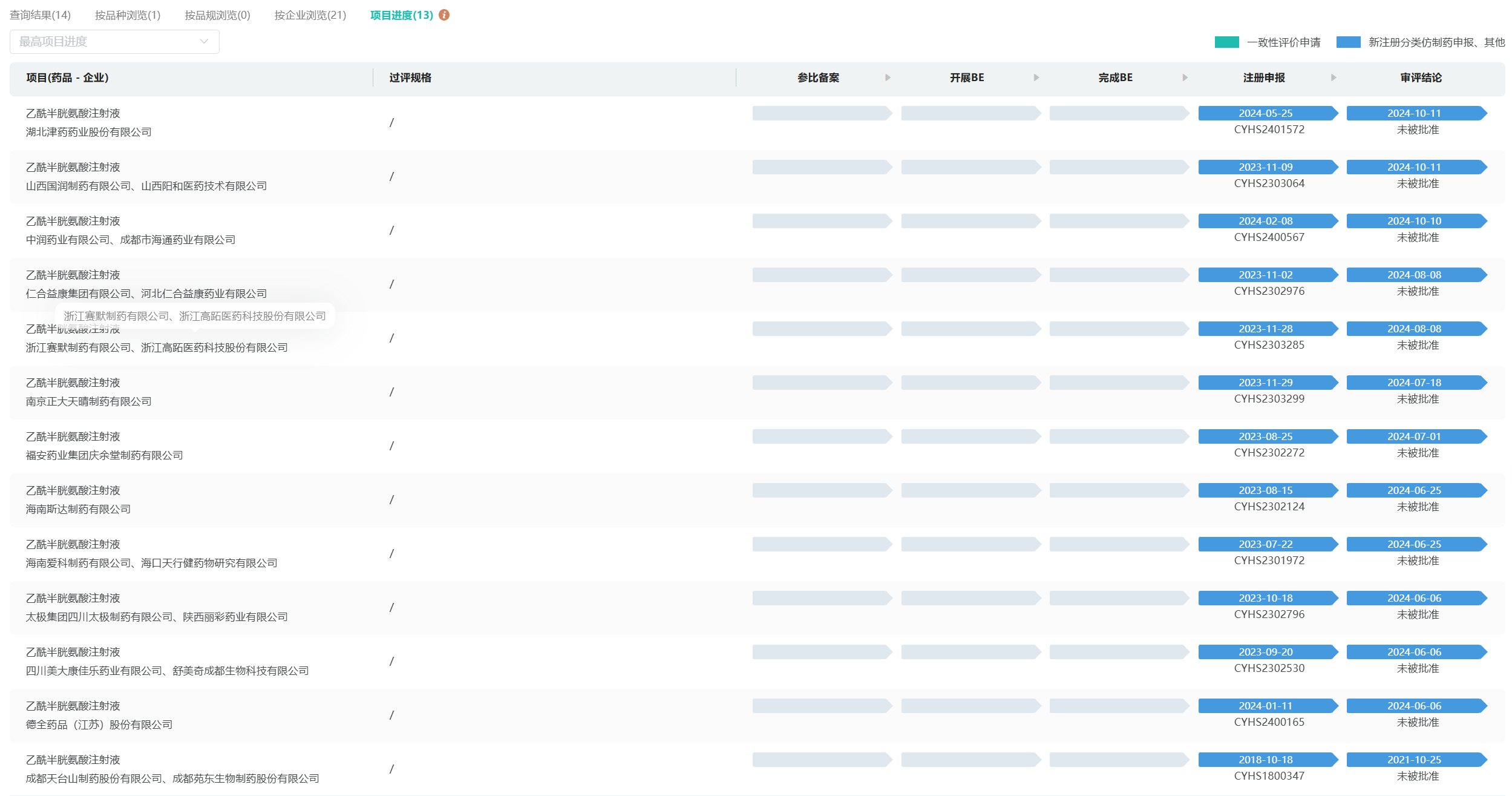
未被批准一致性受理号 | 图源:药融云数据库
在此之前,乙酰半胱氨酸注射液已有批准文号3家,均在新注册分类前批准,规格均为20ml:4g,适应症保肝类;无进口批准文号。
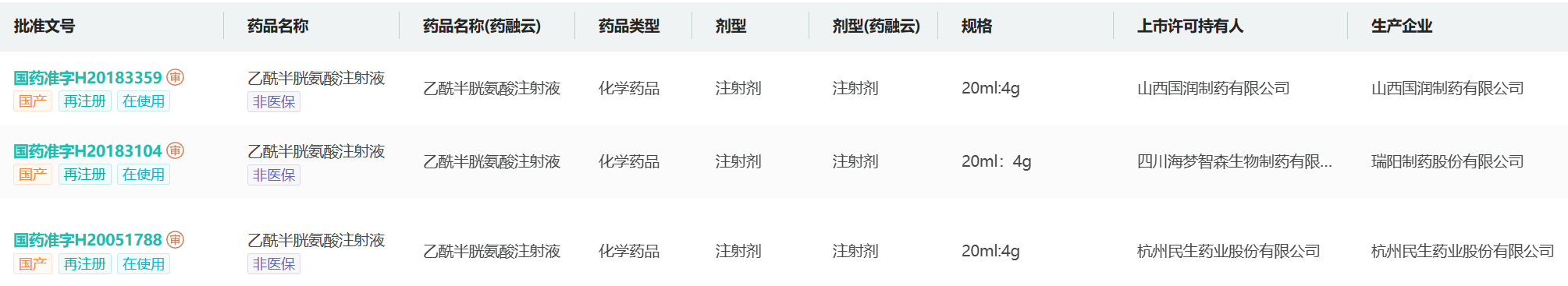
图源:药融云数据库
原研Zambon于2022年申请上市,完成一次发补目前仍在CDE排队审评中。
检索注册信息,原研Zambon(赞邦)于2018年申请临床,适应症为治疗浓稠粘液分泌物过多的呼吸道疾病如:急性支气管炎、慢性支气管炎及其病情恶化者、肺气肿、粘稠物阻塞症以及支气管扩张症。并已在中国完成I期和III期临床,试验结果已经发表,见《Intravenous N-acetylcysteine in respiratory disease with abnormal mucus secretion》,主要终点治疗7天后痰液粘稠度评分和咳痰困难度评分均优效于安慰剂且非劣效于盐酸氨溴索。
当时经专家Suzhou鱼分析,乙酰半胱氨酸注射液频繁被毙的可能原因有三:
1、全球上市制剂规格各不相同
该品列入CDE公示的参比制剂规格有25ml:5g和3ml:300mg,而中国已上市三家的规格均为20ml:4g,美国橙皮书规格30ml:6g。中国已上市三家的规格、适应症和用法用量均与国外参比有差异,故无论原研是否批准进口,仿制20ml:4g规格和保肝适应症都不太可能批准。
2、全球制剂适应症也各不相同
乙酰半胱氨酸注射液中国三家已批准适应症为:在综合治疗基础上用于肝衰竭早期治疗,以降低胆红素、提高凝血酶原活动度。
美国橙皮书适应症:对乙酰氨基酚过量解毒剂(该适应症在中国作为超说明书用药),用于预防或减轻急性摄入或反复超治疗摄入对乙酰氨基酚患者的肝损伤,且按照体重给药。
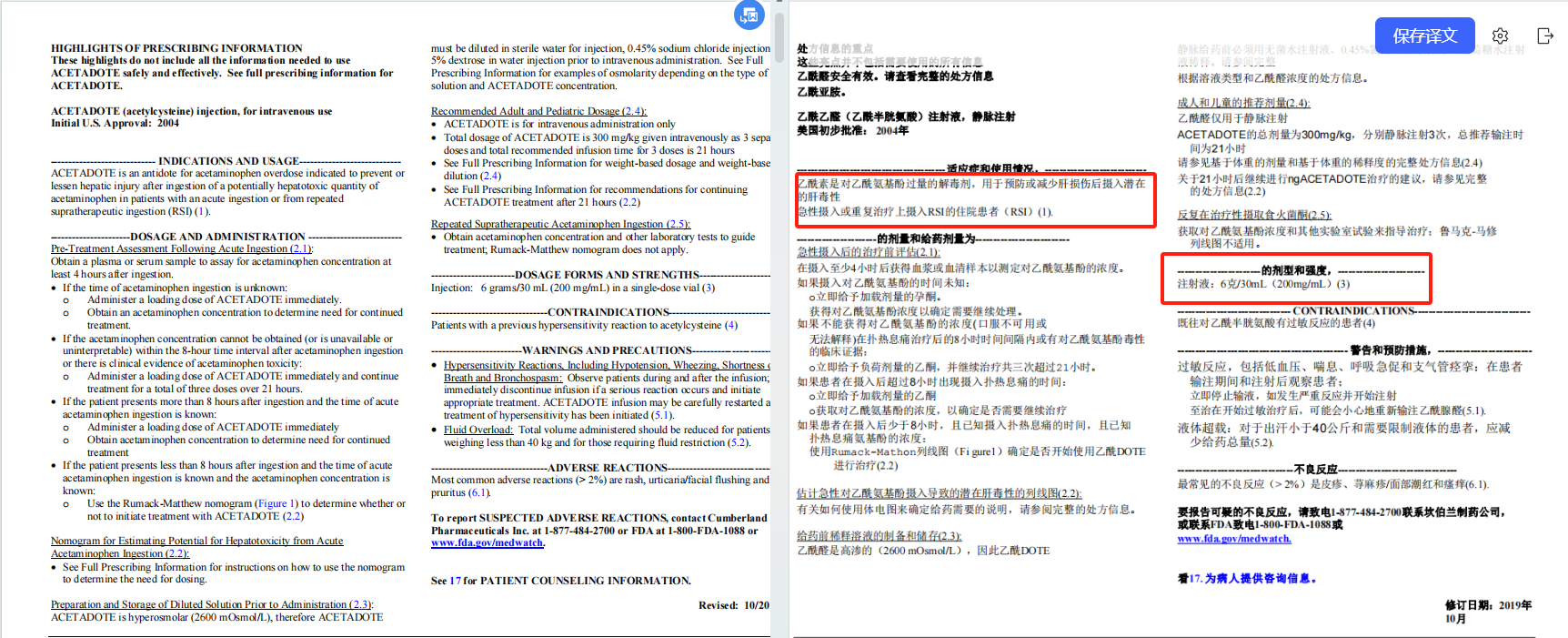
图:Cumberland Pharmaceuticals Inc公司原研产品“Acetadote“的说明书
原研Zambon(赞邦)在中国已完成三期临床的乙酰半胱氨酸注射液适应症:治疗浓稠粘液分泌物过多的呼吸道疾病如:急性支气管炎、慢性支气管炎及其病情恶化者、肺气肿、粘稠物阻塞症以及支气管扩张症。
目前多数申报企业仿制3ml:300mg规格,适应症应该属于呼吸道疾病,而不能是国内已批准的保肝适应症,若不进行验证性临床,相当于此适应症没有临床数据的支持。
3、制剂生产储存过程巯基不稳定
检索NMPA发现有两条抽检不合格的报道,不符合规定项目均为硫化氢。
硫化氢系生产或储存过程中乙酰半胱氨酸的巯基不稳定,不合格检出率高,制剂安全性稳定性待考量。
由此推断,仿制20ml:4g规格、3ml:300mg规格;国内已上市产品的保肝适应症和原研未在国内上市的呼吸系统适应症,未进行验证性临床,应是无法批的。
而此次汇宇以30ml:6g规格成为首家通过一致性评价的企业,合理猜测应当是按美国橙皮书原研“解毒剂”适应症进行申报的。
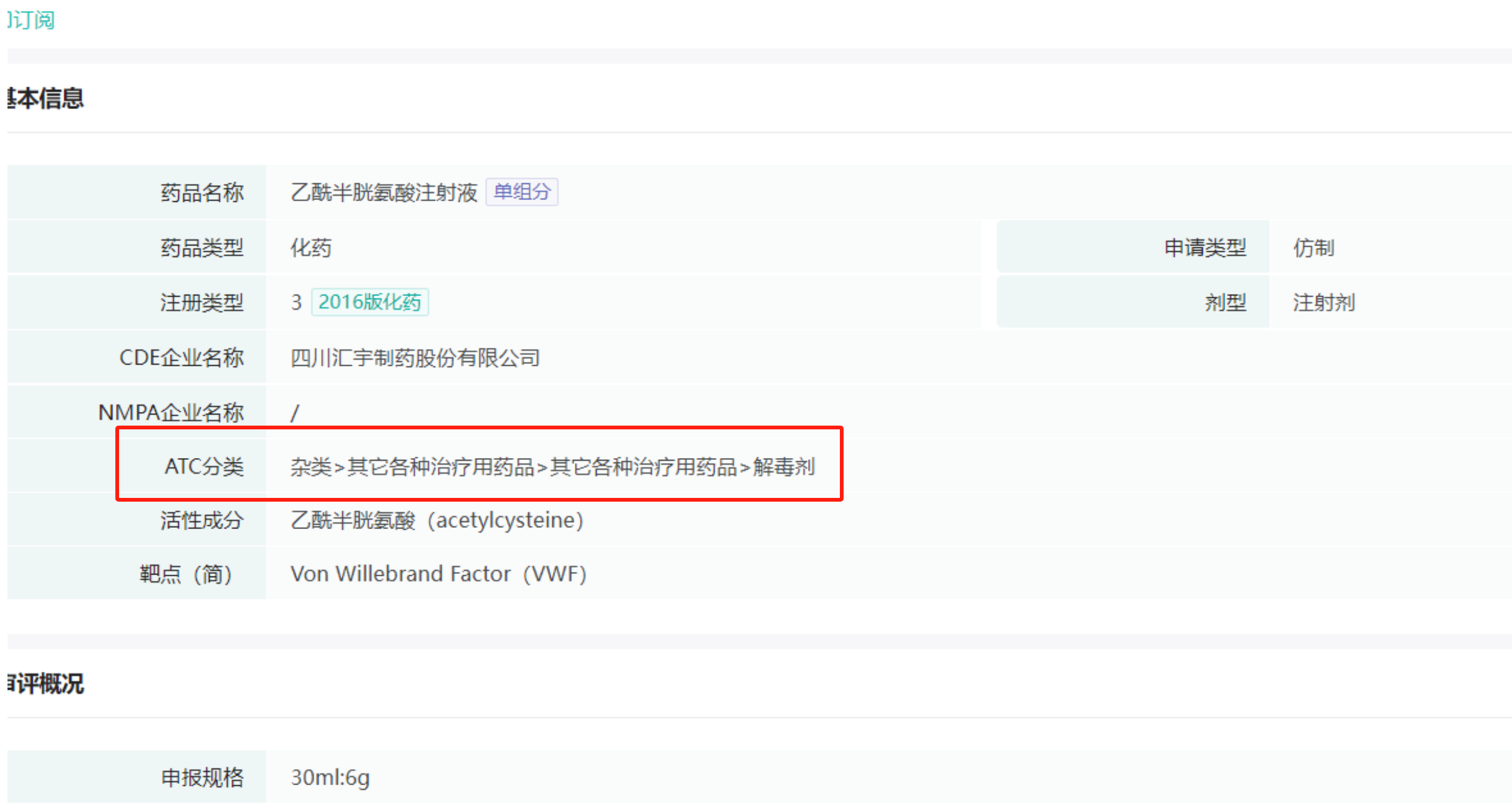
图源:药融云数据库
加之,汇宇此次获批30ml:6g规格较大,依据国内超适应症用药记录,乙酰氨基酚过量解毒一般用量,首次使用在9g左右(按照正常体重60kg)计算,也侧面印证此次汇宇获批适应症应为“解毒剂”。

图源:丁香园
然而据查询,美国橙皮书规格仅被遴选为第四十五批参比制剂目录(征求意见稿)。
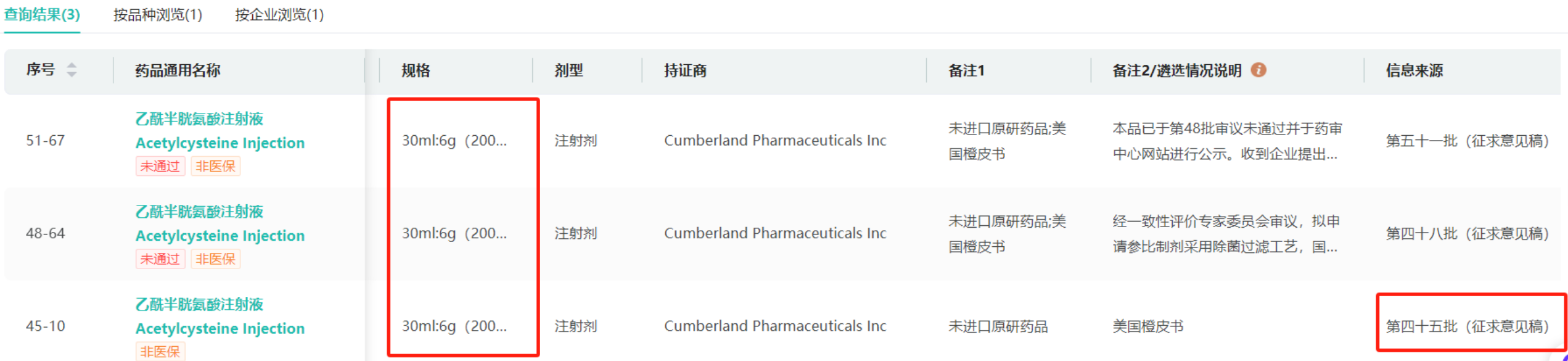
图源:药融云数据库
汇宇此次若确实按照解毒剂适应症过评,也给国内仿制药企业提供了新思路,若呼吸系统小规格适应症无法获批,可仿制大规格。
<END>
想要解锁更多药物研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!


















































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论