
10月18日,据CDE官网公示,信达生物1类新药IBI3001获得临床试验默示许可,拟开发治疗实体瘤。

截图来源:CDE官网
IBI3001是一款糖基化定点偶联、针对B7-H3和EGFR的双特异性抗体偶联药物(ADC)。B7-H3(亦称CD276),作为B7家族的一员,是一种跨膜蛋白,其在多种癌症中的过度表达常与不良预后紧密相关。EGFR,即表皮生长因子受体酪氨酸激酶,在诸如非小细胞肺癌、转移性结直肠癌、胶质母细胞瘤、头颈癌、胰腺癌及乳腺癌等多种癌症中呈现上调状态,这些EGFR的异常变化会过度激活下游的致癌信号通路,例如RAS-RAF-MEK-ERK和AKT-PI3K-mTOR等,进而促进癌细胞的增殖。
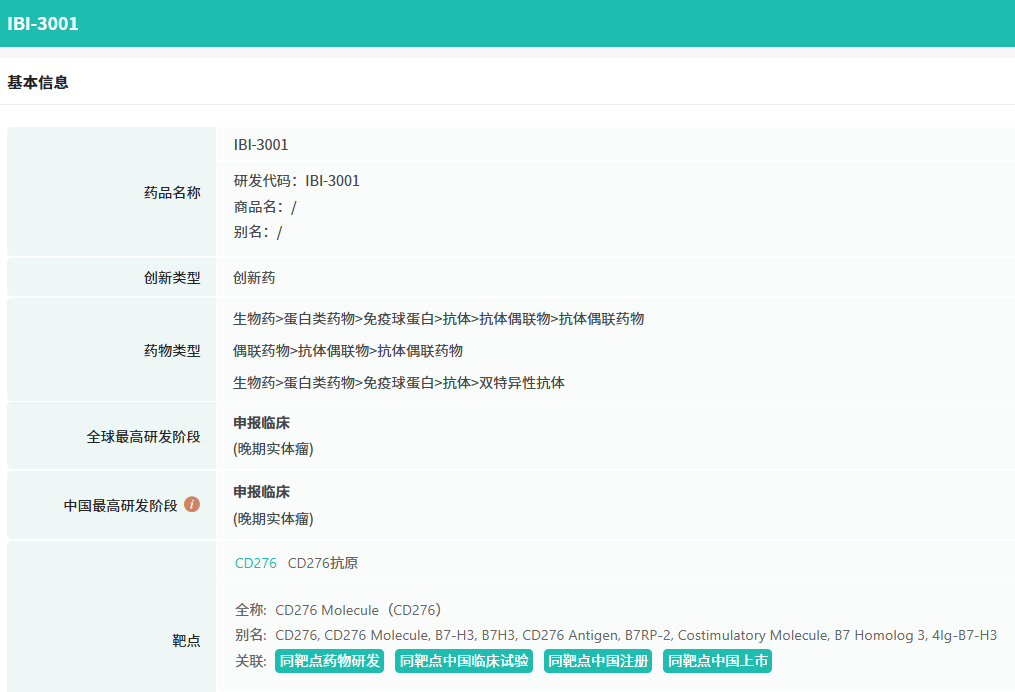
截图来源:药融云数据库(全球药物研发数据库)
值得注意的是,信达生物研发的双特异性抗体IBI334(针对B7-H3/EGFR)经过进一步优化,并结合临床验证的SyntecanE平台,与exatecan特异性偶联,成功诞生了潜在的“同类首创”B7-H3/EGFR双特异性抗体偶联药物(ADC)——IBI3001。这一研究成果因其创新性,入选了2024年美国癌症研究协会(AACR)年会的Late-Breaking Research环节。
研究表明,IBI3001展现了多重抗肿瘤机制,不仅显著增强了EGFR信号的阻断效果,还通过EGFR与B7-H3介导的药物内吞作用实现了细胞杀伤,并表现出强大的ADC旁观效应。此外,经过优化的B7-H3臂在提升EGFR信号通路阻断效能的同时,也有效降低了EGFR靶向治疗可能带来的毒性。此外,IBI3001于2024年8月9日,在国内申请临床。
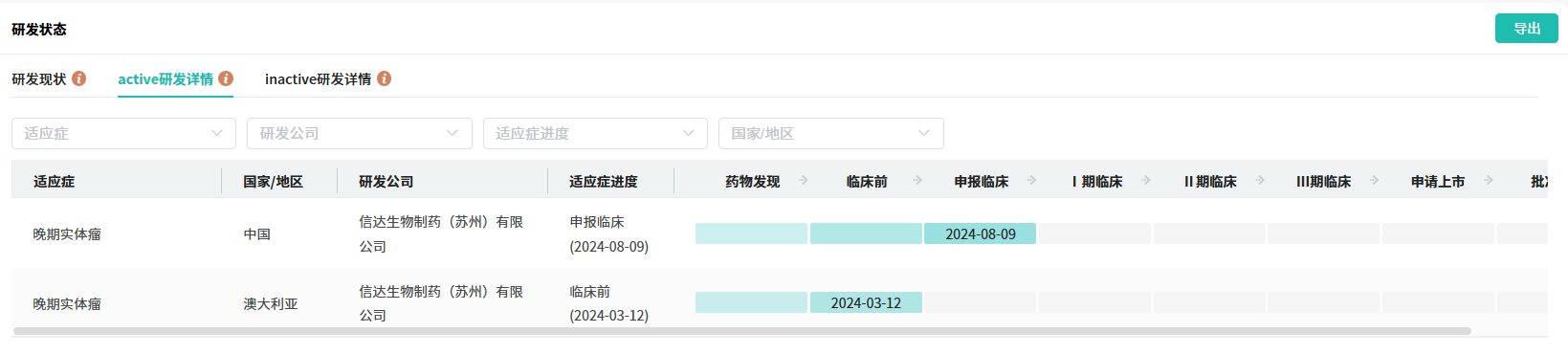
截图来源:药融云全球药物研发数据库
此次,IBI3001已在中国获得临床试验批准,标志着该药物即将在中国开展深入的临床研究,为患者带来新的治疗希望。
参考来源:
[1] CDE官网
[2] 药融云数据库
<END>
想要解锁更多药物研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!






















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论