注:本文不构成任何投资意见和建议,以官方/公司公告为准;本文仅作医疗健康相关药物介绍,非治疗方案推荐(若涉及)。因水平有限,错误不可避免,或有些信息非最及时,欢迎留言指出。
联拓生物(LianBio)由美国生物医药投资基金Perceptive Advisors孵化的生物科技公司,最早成立于2019年。联拓生物(LianBio)是一家跨国Biotech,其使命是为中国和亚洲患者带来颠覆性药物, 改变本地区缺少创新药物的历史状况。通过与全球高度创新的生物制药公司合作,联拓生物正在推进其多样化的临床候选药物产品管线,有可能推动心血管、肿瘤、眼科、炎症疾病和呼吸系统不同适应症的新治疗标准。联拓生物正在建立国际化的基础设施,从而将公司定位为首选的合作对象,并为合作伙伴提供进入中国和其他亚洲市场的平台。
高管团队

Konstantin Poukalov
Perceptive Advisors 董事总经理
联拓生物执行董事长
Konstantin Poukalov专注于Perceptive平台的各种策略制定。除联拓生物外,Poukalov先生还在Lyra Therapeutics(纳斯达克股票代码: LYRA)、Landos Biopharma, Inc. (纳斯达克股票代码: LABP)的董事会任职。在加入Perceptive前,Poukalov先生于2014年至2018年担任Kadmon Holdings(纽交所股票代码:KDMN)的执行副总裁兼首席财务官。

王轶喆博士
担任CEO
加入联拓生物之前,王轶喆博士任职于礼来公司,任礼来抗肿瘤产品全球研发负责人。2020年,王博士在礼来研究实验室担任抗新冠病毒治疗项目的全球平台负责人,负责管理集发现、研发和产品上市于一体的全新运营模式,助力礼来的新冠抗体药物bamlanivimab获得FDA的紧急使用授权(EUA)。在此之前,王博士曾任礼来中国高级副总裁、跨生化产品及抗肿瘤产品事业部负责人,并担任礼来中国管委会、全球跨生化产品领导团队、全球抗肿瘤产品领导团队成员。

余久筠博士
总裁兼首席战略官
加入联拓生物之前,余久筠博士在华兴证券(美国)任董事总经理和跨境医疗投资银行业务负责人,也曾担任Labrador Advisors的董事总经理,为众多跨境合作和许可交易提供专业咨询;曾任药明康德(Wuxi Apptec)战略副总裁,帮助组建并共同领导辉瑞的风险投资团队,也是辉瑞全球业务发展组织的主要成员。余久筠博士曾在美国旧金山湾区担任过多年的风险投资人,曾任Delphi Ventures的普通合伙人和Bay City Capital的董事总经理。

钱江博士
担任中国总经理
加入联拓生物之前,钱先生任礼来中国抗肿瘤事业部副总裁,管理超过700名团队成员,并负责该部门的盈亏和组织发展。在加入礼来之前,钱先生于2012年至2018年就职于诺华肿瘤(中国),并最终担任执行总监、实体瘤事业部负责人。2005年至2012年,他曾在辉瑞公司担任多个重要职位,包括辉瑞总部全球临床发展与医学事务团队业务联络负责人、中国抗肿瘤事业部总经理等。
产品管线(pipeline)以及交易(BD deals)
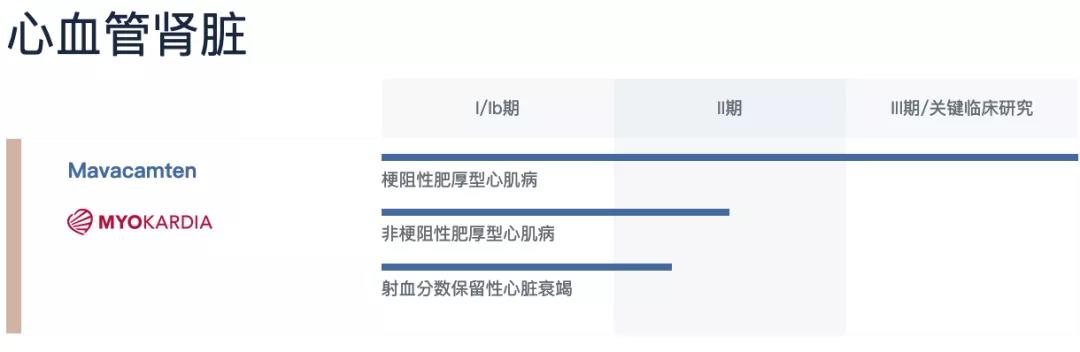


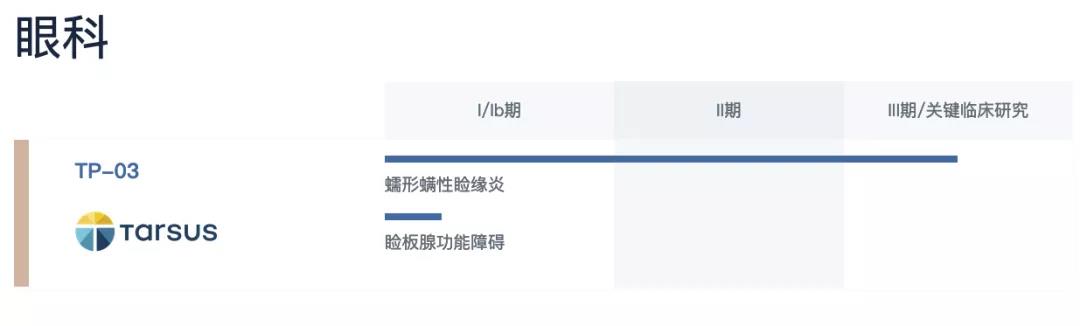
▲联拓生物产品线/平台
联拓生物2020年研发费用(R&D)为1.2亿美元,2021年上半年研发费用为1.46亿美元。
BridgeBio Pharma研发的两款肿瘤产品,包括选择性FGFR抑制剂infigratinib,以及治疗因RAS和酪氨酸激酶受体导致的实体肿瘤的SHP2抑制剂BBP-398授予联拓生物。
TRUSELTIQ™ (infigratinib) 是一种口服FGFR1-3选择性抑制剂,在美国已被批准用于既往接受过治疗的、不可切除的局部晚期或转移性胆管癌,且患者需经FDA批准的检测方法确认带有FGFR2融合或FGFR2重排。Infigratinib 正在进行对伴有FGFR3基因变异的晚期尿路上皮癌患者的临床试验,以验证其在该患者中疗效。联拓生物获得BridgeBio Pharma授权,拥有在中国大陆、香港和澳门对infigratinib 进行开发和商业化的权利。
2021年8月,Infiglatinib在用于胃癌及其他晚期实体瘤的2a期临床试验中完成中国首例患者给药。
2021年6月:Lyra Therapeutics, Inc.(纳斯达克:LYRA)达成战略合作和独家许可协议,双方将携手在大中华区(中国大陆以及港澳台地区)、韩国、新加坡和泰国,对LYR-210进行开发和商业化。LYR-210是一款处于临床晚期开发阶段的鼻内抗炎药物基质,旨在治疗慢性鼻窦炎(CRS),一种削弱鼻腔功能的炎症疾病。根据协议条款, Lyra将获得1200万美元的首付款,并有资格获得最高可达1.35亿美元的开发、监管和商业化里程碑付款。商业化启动后,根据LYR-210在各个授权地区的净销售情况,Lyra还可获得低两位数的分层销售分成。LYR-210在合作区域内的全部开发和商业化费用将由联拓生物承担,而Lyra仍将拥有LYR-210在合作区域外的一切权利。作为协议的一部分,联拓生物还将获得在许可区域内开发和商业化Lyra的LYR-220的优先权利。LYR-220是一种鼻内抗炎药物基质,用于治疗既往接受过鼻窦手术但仍有持续性鼻窦炎的患者。

2021年5月17日 , Landos Biopharma, Inc.(纳斯达克:LABP)与联拓生物达成独家合作和许可协议,双方将携手在大中华区(中国大陆以及港澳台地区)和亚洲特定市场,对新药Omilancor(BT-11)和NX-13进行开发和商业化。Omilancor是一款在研的新型口服肠道限制性LANCL2通路激动剂,用于治疗溃疡性结肠炎(UC)、克罗恩病(CD)和嗜酸性食管炎(EoE)。NX-13是另一款在研的新型口服肠道限制性药物,其作用靶点为NLRX1通路,用于治疗溃疡性结肠炎和克罗恩病。根据合作条款,联拓生物将获得在大中华区、韩国、新加坡、泰国、越南、缅甸、柬埔寨、印尼和菲律宾开发和商业化omilancor和NX-13的独家授权;而Landos将获得1800万美元的首付款,并有资格获得最高可达2亿美元的开发和商业化里程碑付款。根据omilancor和NX-13在授权区域内的净销售情况,Landos还可获得低两位数的分层销售分成。联拓生物将参加omilancor和NX-13的全球三期临床试验,招募一定数量的患者参与相关研究。合作区域内的全部开发和商业化费用将由联拓生物承担,而合作区域外的费用则由Landos承担。
2021年5月11日,NANOBIOTIX (泛欧交易所:NANO;纳斯达克:NBTX)与联拓生物宣布建立合作伙伴关系,双方将携手在大中华区(中国大陆以及港澳台地区)、韩国、新加坡和泰国,对Nanobiotix的主要候选产品NBTXR3 —— 一款潜在首创性放射增强剂—— 进行开发和商业化。根据协议条款,联拓生物将获得在大中华区、韩国、新加坡和泰国开发和商业化NBTXR3的独家授权;而Nanobiotix将获得2000万美元的首付款,并有资格获得最高可达2.2亿美元潜在的开发和商业化里程碑付款。根据NBTXR3在授权区域内的净销售情况,Nanobiotix还可获得低两位数的分层销售分成。联拓生物将参加全球三期头颈癌的注册研究,在中国招募100名患者,以评估NBTXR3对局部晚期头颈部鳞状细胞癌(HNSCC;头颈癌)患者的疗效。除参与全球三期头颈癌研究外,联拓生物还承诺参与另外四项由Nanobiotix主导的注册研究的患者招募工作,这些研究涉及不同肿瘤适应症以及可能包括免疫疗法在内的不同联合治疗方案。合作区域内的全部开发和商业化费用将由联拓生物承担,而合作区域外的费用则由Nanobiotix承担。

2021年3月2日,ReViral与联拓生物宣布达成独家合作和许可协议,将在中国大陆、香港、澳门和新加坡地区共同开发和商业化Sisunatovir。作为ReViral的领先候选药物,Sisunatovir是一种用于治疗RSV的小分子药物,目前正在儿童和成人免疫功能低下的患者中进行2期临床试验。根据协议条款,ReViral将获得1,400万美元的现金首付款,并有资格获得高达1.05亿美元的开发和商业里程碑付款。此外,ReViral在许可地区售出药物的净销售额中可获得低两位数的分层销售分成。联拓生物将负责Sisunatovir在许可地区的开发和商业化,同时ReViral将在其他地区继续负责Sisunatovir的开发和商业化。

即将登陆纳斯达克
近期,联拓生物已经向美国证券交易委员会(“SEC”)提交了S-1表格注册声明书,向公众发售20,312,500股美国存托股票。此外,联拓生物拟授予承销商30天的超额配售权,最多可额外购买3,046,875股美国存托股票。首次公开发行价格预计在每股15.00美元至17.00美元之间。联拓生物已经申请10月28日在纳斯达克全球市场挂牌上市,股票代码为 “LIAN”。
2020年11月,联拓生物完成3.1亿美元的交叉轮融资,该轮融资由美国生物医药投资领域知名投资机构RA Capital和Venrock Healthcare Capital Partners以及中国私募股权管理机构国投招商共同领投。该轮的其他生物医药投资者还包括:贝莱德资产旗下的基金, Casdin Capital, Farallon, Logos Capital, Perceptive Advisors, 辉瑞, Sphera Healthcare, T. Rowe Price Associates, Inc旗下的基金, Tybourne Capital Management, Vida Ventures, Viking Global Investors 和Wellington Management。

IPO前,Perceptive Advisors持股为62.4%,RA Capital持股为7.2%,BridgeBio Pharma持股为5.8%。静观上市后,业绩、股价以及产品进展。若License in 优质资产,无疑将是对中国乃至亚洲医药市场很好的补给。
推广:面对当前未被满足的临床用药需求,该如何寻到符合立足中国、面向全球的特色化发展的创新之路?以临床价值为导向的新药研究/开发需要多方参与,为了更好的与更易获得的治疗方式。将于2021年11月25-26日于上海召开的第三届(上海)生物医药创新者峰会将给予行业和参与者们一些答案。本次峰会由药融圈策划组织,旨在为生物医药上下游搭建一个交流趋势及创新的平台,拟邀请50+位生物医药领域研究、开发及运营与BD/投资方面的实战专家亲临现场,将与千余位与会嘉宾共论趋势,技术及经验。点击1000+行业同仁已加盟,第三届(上海)生物医药创新者峰会限时免费倒计时,报名!
参考:
NMPA/CDE;
药融云数据,www.pharnexcloud.com;
FDA/EMA;
相关公司公开披露;
https://www.lianbio.com/cn/news/myokardia-and-lianbio-form-strategic-partnership/;
https://www.lianbio.com/cn/news/bridgebio-pharma-lianbio-announce-first-patient-treated-in-phase-2a-trial-of-infigratinib-in-patients-with-gastric-cancer-and-other-advanced-solid-tumors/;
www.bridgebio.com;等等。
<END>






















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论