
7月19日,据NMPA官网最新公示,礼来(Eli Lilly and Company)公司申报的替尔泊肽注射液(tirzepatide)新适应症上市申请已获得批准。用于在低热量饮食和增加运动基础上改善成人肥胖或伴有至少一种体重相关合并症的超重患者长期体重管理。
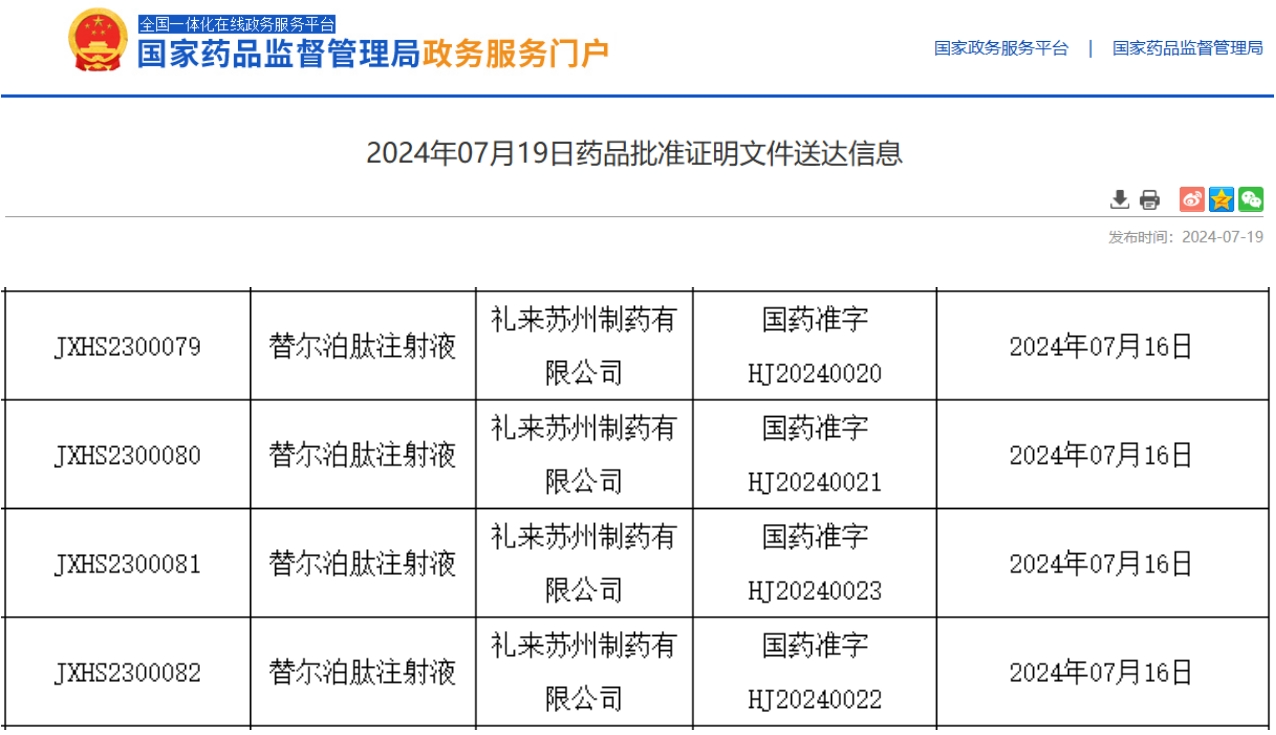
截图来源:NMPA
据药融云数据库显示,替尔泊肽是一款每周注射一次的GIPR和GLP-1R激动剂。2022年5月,Tirzepatide首次获FDA批准上市,用于治疗2型糖尿病。今年,替尔泊肽注射液在华获批上市,用于治疗2型糖尿病。它是一种单分子多肽,可结合并激活人体天然肠促胰素受体GIP受体和GLP-1受体。GIP受体和GLP-1受体均表达于大脑中调节食欲的重要区域。替尔泊肽通过减少热量摄入和调节食欲来减少食物摄入、降低体重并降低脂肪含量。此外,该产品已被证实可调节脂质利用。
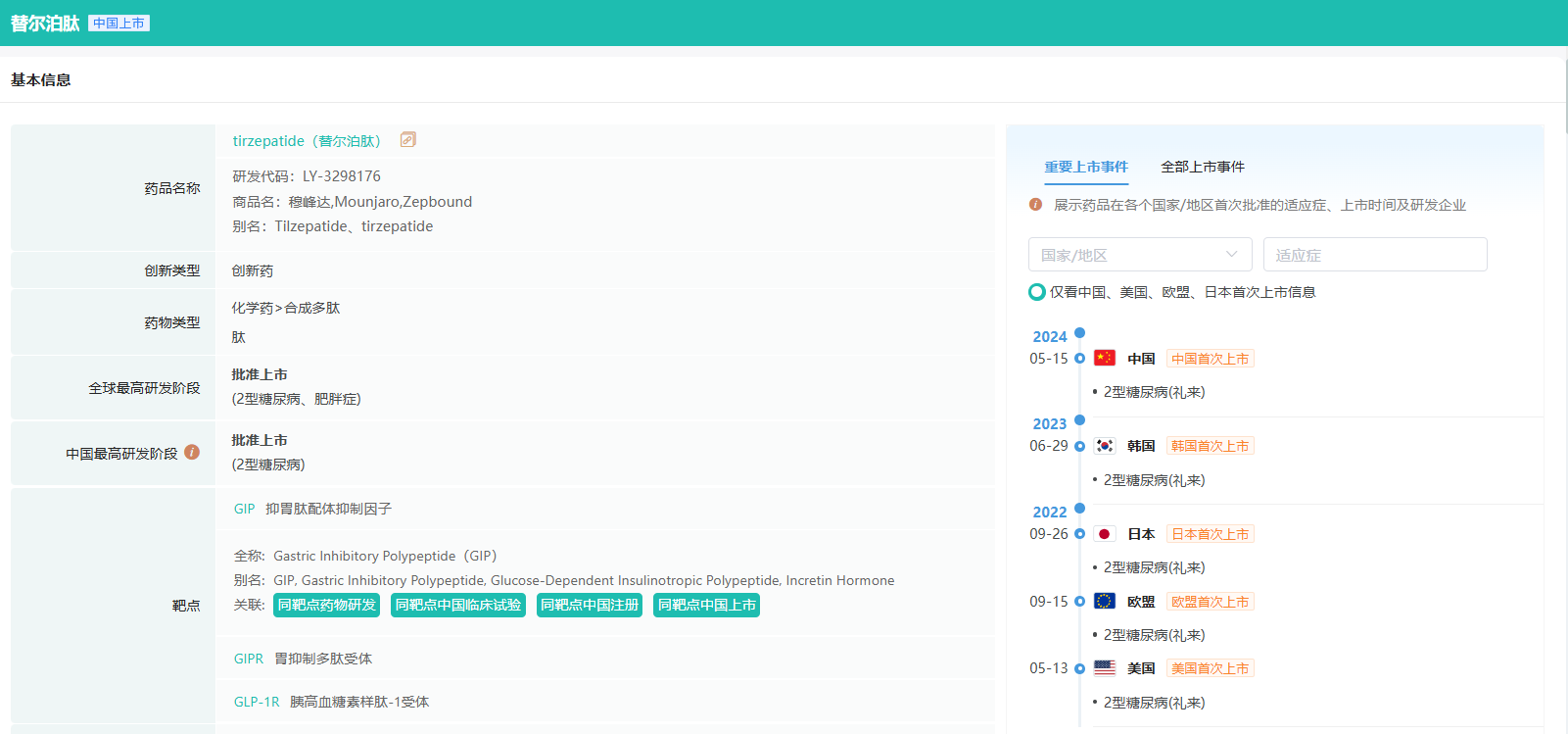
截图来源:药融云全球药物研发数据库
2022年5月,Tirzepatide首次获FDA批准上市,用于治疗2型糖尿病。今年,替尔泊肽在华获批上市,用于治疗2型糖尿病。
2023年2月,礼来宣布,替尔泊肽用于肥胖或超重成人患者的中国III期SURMOUNT-CN研究取得积极结果,达到主要终点和所有关键次要终点,且未出现新的安全性信号。
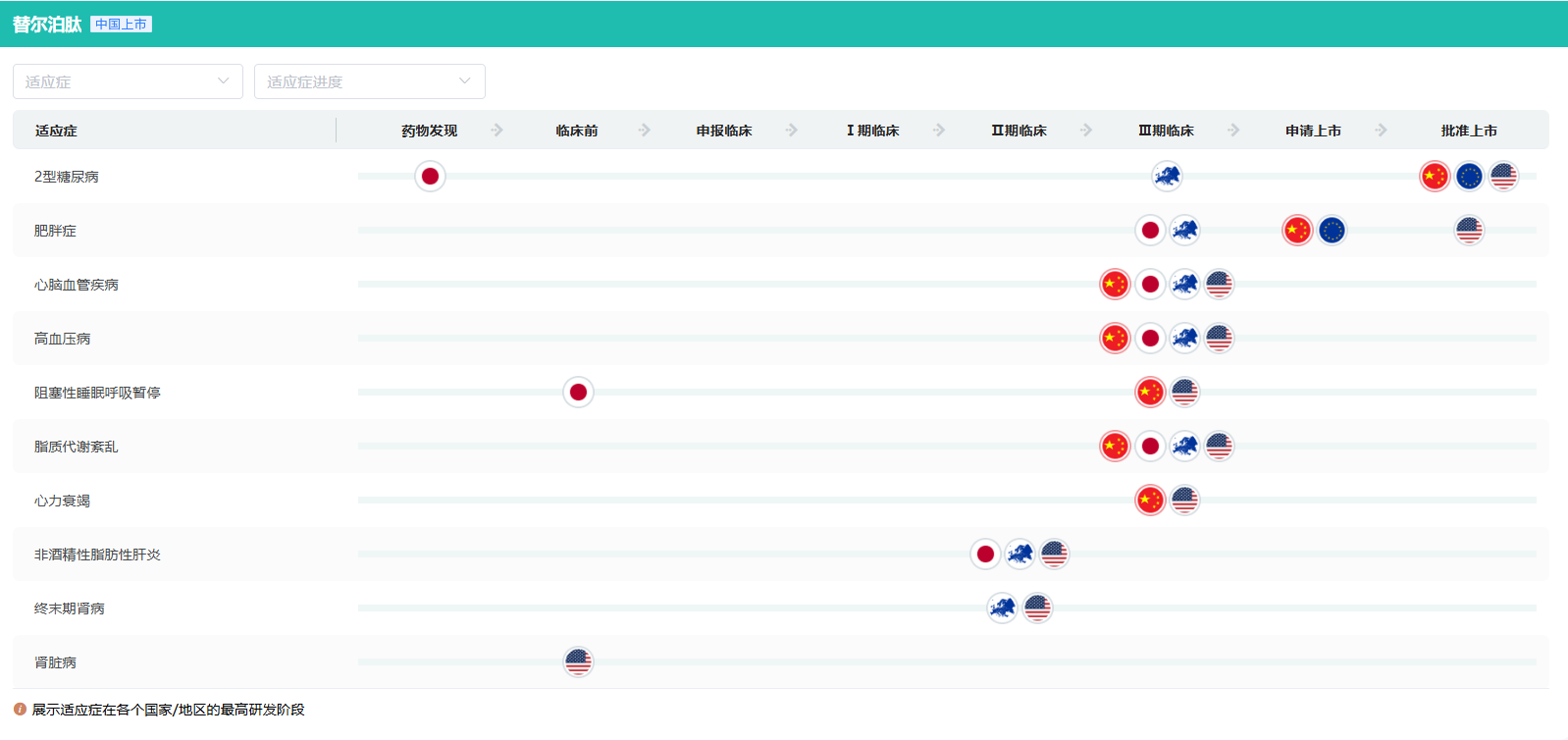
截图来源:药融云全球药物研发数据库
礼来针对替尔泊肽长期体重管理的SURMOUNT系列III期全球临床开发计划于2019年底开始,在6项临床注册研究中招募了超过5,000名肥胖或超重患者,其中4项为全球研究。目前,SURMOUNT-1/2/3/4在内的4项研究数据均已公布。其中,SURMOUNT-1主要研究结果及SURMOUNT-2研究结果已分别发表于《新英格兰医学杂志》及《柳叶刀》。此外,研究人员还正在成人肥胖或超重患者中进一步开展3b期临床试验SURMOUNT-5研究,旨在对比替尔泊肽与司美格鲁肽2.4mg治疗72周的有效性和安全性。
参考来源:
[1] NMPA官网
[2] 药融云数据库
<END>
想要解锁更多药物研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!






















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论