
7月12日,据clinicaltrials.gov网站显示,礼来终止了BTLA单抗LY3361237治疗中度活动型系统性红斑狼疮(SLE)的一项II期研究(NCT05123586),原因为缺乏疗效。

LY3361237是一种BTLA激动剂,旨在通过激活免疫系统中的BTLA受体,来重新平衡免疫系统,阻止其攻击自身组织。该药物正在至少患有中度活动性系统性红斑狼疮的患者中进行测试。
礼来公司发言人表示,公司计划在适当的科学论坛上报告完整数据。

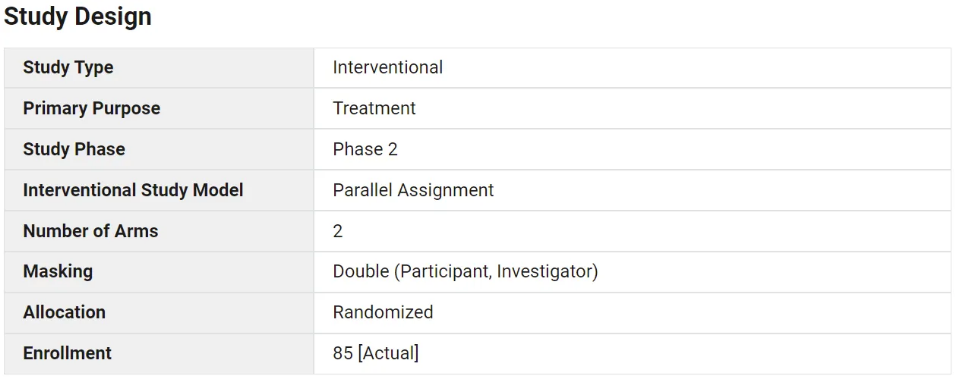
该II期临床从2022年3月启动,实际入组85例至少中度活动的系统性红斑狼疮患者。根据礼来去年Q3财报显示,LY3361237治疗SLE的管线就已被剔除,但当时该试验仍在进行中。根据早前的更新,这项涉及 85 人的试验于 2024 年 2 月完成,但尚未公开报道该药物的安全性或有效性。

礼来医学免疫学副总裁 Paul Klekotka 表示,公司仍在投资SLE治疗领域。尽管之前的试验失败,但该疾病仍然在公司研发管线中。
其实,这不是礼来第一次在SLE的尝试中遭遇失败。
2014年10月,礼来公司宣布停止开发针对BAFF的单克隆抗体Tabalumab在SLE 治疗上的研发,并不再继续寻求上市申请。这一决定是基于两项关键的III期临床试验结果。在这两项试验中,Tabalumab未能显示出比标准治疗更优的疗效。
2022年1月,礼来决定停止JAK抑制剂Olumiant在治疗SLE方面的开发工作,此决定是根据两项关键的III期试验的结果。
2022年1月,礼来与Nektar Therapeutics合作开发的IL-2Rβ激动剂rezpegaldesleukin(rezpeg)在治疗SLE的II期临床试验ISLAND研究中未达到其主要研究目标。因此,礼来决定不继续推进rezpeg进入III期研究,并终止了与Nektar的合作关系。
尽管礼来在SLE新疗法的研究上不断遭遇挫折,但礼来并未放弃探索。
参考来源:
[1] 礼来官网
[2] clinicaltrials.gov
<END>
想要解锁更多药物研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!






























![医药高地:核药!恒瑞医药镥[177Lu]氧奥曲肽注射液获批临床](https://yaorongyun-public.oss-cn-shanghai.aliyuncs.com/images/covers/202302/09/e3938ad9f1d23e2fd043611c4a98c02a.png)










 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论