
4月30日,由知名基因编辑专家刘如谦教授创立的领先基因编辑公司Prime Medicine宣布,该公司为在研先导编辑(prime editing)疗法PM359递交的IND申请已经获得美国FDA的许可,用于治疗慢性肉芽肿病(CGD)。这使该公司能够启动全球性的1/2期临床试验。

新闻稿指出,这是先导编辑技术首个获得许可的IND,标着新一代基因编辑技术临床转化的重要里程碑。
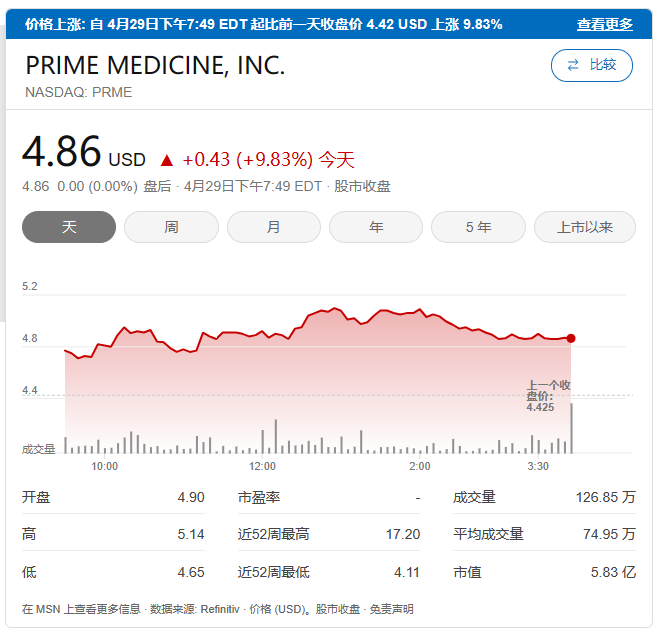
受此消息的影响,公司股价大涨9.83%,目前市值5.83亿美元。
PM359是Prime Medicine在血液学和免疫学领域的首个候选疗法,针对的是慢性肉芽肿病的p47phox变体。PM359通过先导编辑器在体外修改自体造血干细胞(HSCs)。临床前研究显示,这些编辑器可以高效率纠正携带病因突变细胞的DNA。PM359已获得美国FDA授予的罕见儿科药物认定和孤儿药资格。
该1/2期临床试验旨在评估PM359在成人和儿科研究参与者中的安全性、生物活性和初步疗效。最初的研究参与者将是病情稳定的成人。如果在这一队列中展示出安全性和生物活性,该研究计划招募有活动性感染或严重炎症的参与者,以及青少年和儿科参与者。Prime Medicine预计将在2025年公布来自该研究的初步临床数据。

Prime Medicine总裁兼首席执行官Keith Gottesdiener医学博士说,我们很高兴我们的首个候选产品PM359取得了这一重要的里程碑,这代表了首个Prime Editor候选产品的IND批准,也是下一代基因编辑领域的重大进步,基于我们临床前研究的数据,我们相信PM359有潜力充分改善CGD的流行致病突变,从而改善这些患者的疾病。我们期待按计划启动我们的1/2期试验,并进一步确定PM359对这种疾病患者的潜在治疗效果。
今年3月,Prime Medicine成功完成了22,560,001股普通股的公开发行,其中包括承销商全面行使选择权购买的3,360,000股,以及以预融资认股权证形式取代部分投资者普通股的3,200,0005股。此次发行在扣除相关费用前,为Prime Medicine带来了约1.61亿美元的收益。
在上市之前,Prime Medicine 曾通过两轮融资筹集了超3亿美元,并在2022年的首次公开募股中募集了1.75亿美元。今年1月,该公司还从囊性纤维化基金会(CFF)获得了1500万美元的资金,用于启动囊性纤维化的基因编辑计划。
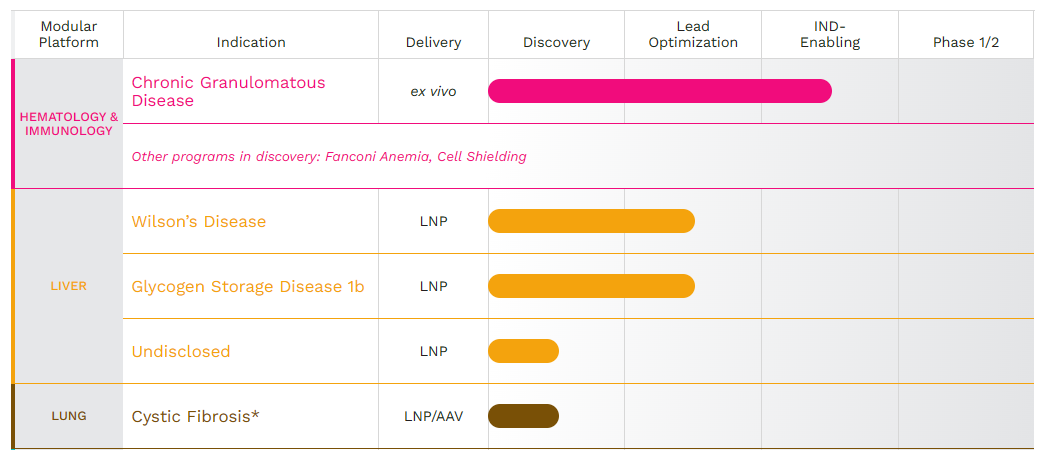
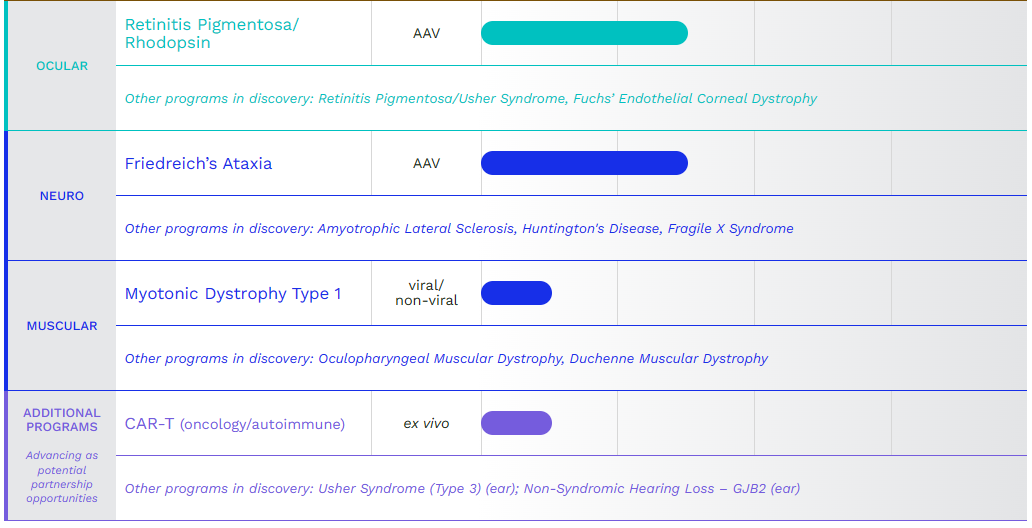
目前,Prime Medicine正围绕核心重点领域推进多样化的研究治疗项目组合:血液学和免疫学、肝脏、肺、眼科和神经肌肉。
公司在研管线
<END>
要解锁更多企业药品研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药品各国上市情况、药品批文信息、销售情况与各维度分析、市场竞争格局、一致性评价情况、集采中标情况、药企申报审批信息、最新动态与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论