
不知不觉2023年已经接近尾声,我国创新药在2023年也迎来了新的突破,中国创新药从量变到质变,跻身国际第二梯队,目前创新药企重磅新药收入高速放量,研发和销售费用指标改善,盈利能力提升,商业化进入加速收获期。据不完全统计,受新冠疫情影响,近4年的创新药获批情况有所波动,截至目前,2023年NMPA批准的创新药数量是98个,较去年大幅提升。
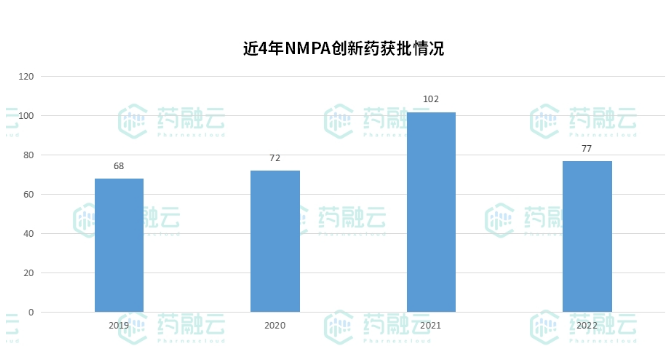
截图来源:药融云中国药品审评数据库
当前,随着国内创新药的不断崛起,国内创新药领域利好政策不断发布,各大药企研发技术也不断提升,创新药市场迎来高速发展契机。根据相关数据显示,2022年我国创新药市场规模达6785亿元,预计2023年中国创新药市场规模将增长至7789亿元。目前预计2024年有望在中国获批的国产创新药有18款,其中两家明星药企强势布局,恒瑞有4款,康方生物有3款。
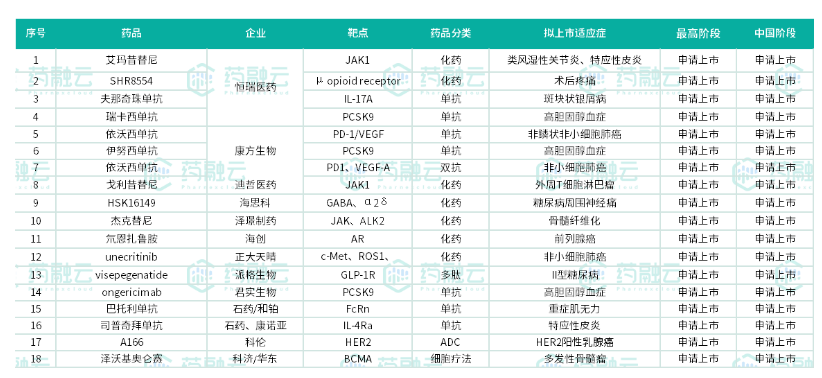
1.艾玛昔替尼
艾玛昔替尼(SHR0302)是由恒瑞医药自主研发的高选择性的JAK1抑制剂,国家1类新药,是国内自主研发的具有一类知识产权的口服小分子创新药物,可通过抑制JAK1信号传导发挥抗炎和抑制免疫的生物学效应。

截图来源:药融云全球药物研发数据库
SHR0302目前已开展了包括类风湿性关节炎、溃疡性结肠炎、特应性皮炎、斑秃、银屑病关节炎等多领域的临床研究。2021年1月,SHR0302片被国家药监局授予了突破性疗法,用于治疗成人及12岁以上青少年的中重度特应性皮炎,目前Ill期临床结果已经达到了共同主要终点及次要终点,恒瑞已于2023年6月递交了该适应症的上市申请。
2.SHR8554
SHR8554注射液是由恒瑞医药研发的一款偏向性的μ阿片受体(MOR)激动剂,拟用于疼痛的治疗。2022年7月,SHR8554注射液的新药上市申请获得CDE受理,用于治疗腹部手术后中重度疼痛。
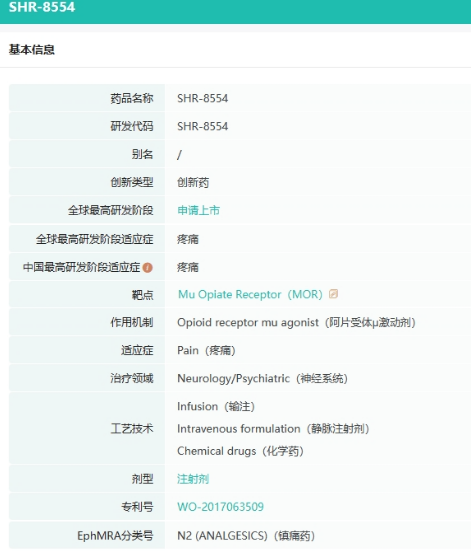
截图来源:药融云全球药物研发数据库
据公开资料显示,阿片类药物是治疗中重度急慢性疼痛最常用的药物之一,MOR激动剂是阿片类药物中镇痛作用较强的一类。与经典的MOR激动剂相比,SHR8554在产生类似的中枢镇痛作用的同时,还能降低常见的胃肠道不良反应发生率。
3.夫那奇珠单抗
夫那奇珠单抗(SHR-1314)是由恒瑞医药研发的一种重组的人源化 IgG1单克隆抗体,可以靶向IL-17A并抑制其与IL-17受体的相互作用。

截图来源:药融云全球药物研发数据库
2023年4月,夫那奇珠单抗的药品上市许可申请获国家药监局受理,这是一种靶向人IL-17A的重组人源化单克隆抗体,拟用于治疗与IL-17通路相关的自身免疫疾病,如斑块状银屑病、银屑病关节炎和强直性脊柱炎等。
4.瑞卡西单抗
瑞卡西单抗(SHR-1209)是恒瑞医药自主研发的抗人类枯草溶菌素转化酶9(PCSK9)人源化单克隆抗体。主要通过与循环中的PCSK9结合,增加肝细胞表面LDLR的表达,促进LDL-C清除,从而达到降低血清LDL-C水平的目的。
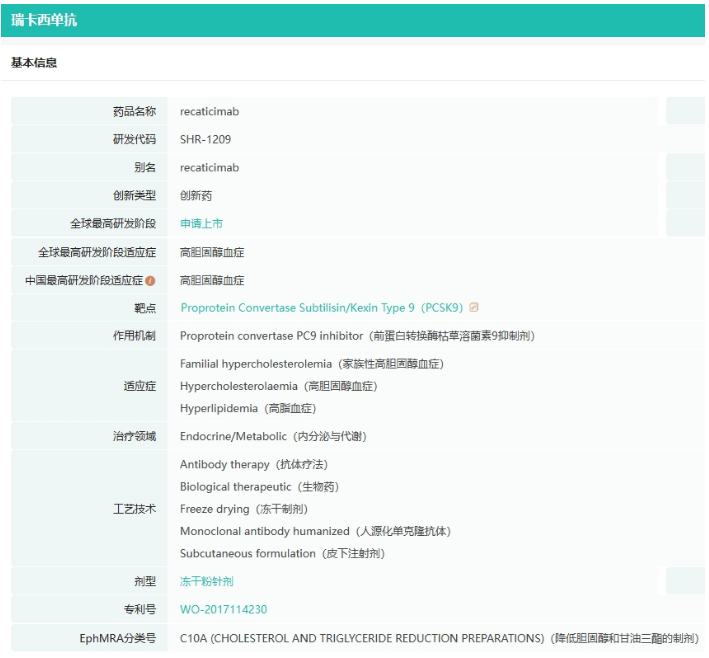
截图来源:药融云全球药物研发数据库
瑞卡西单抗给药频率更灵活,可为患者提供新的治疗选择。REMAIN-1研究旨在探讨瑞卡西单抗单药治疗非家族性高胆固醇血症和混合型高脂血症患者的有效性和安全性。
5.依沃西单抗
依沃西单抗(AK112)是康方生物研发的PD-1/VEGF双特异性抗体。基于该公司Tetrabody技术设计,依沃西单抗可阻断PD-1与PD-L1和PD-L2的结合,并同时阻断VEGF与VEGF受体的结合。
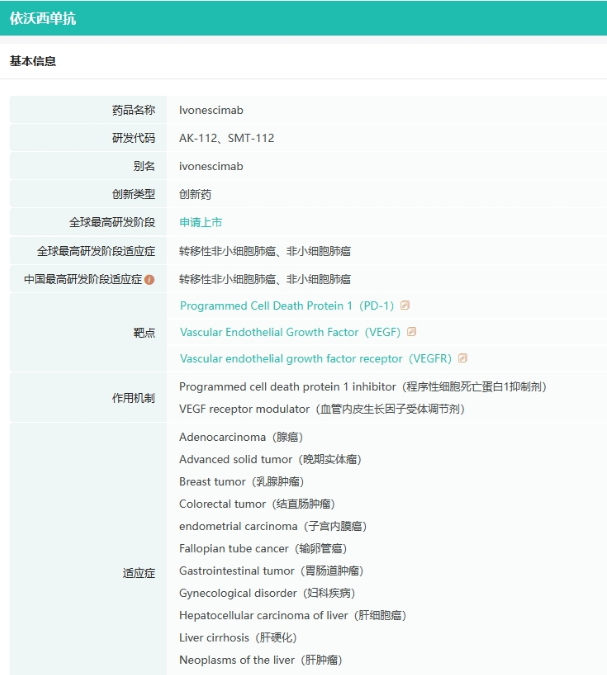
截图来源:药融云全球药物研发数据库
鉴于VEGF和PD-1在肿瘤微环境中的共表达,与联合疗法相比,该产品作为单一药物同时阻断这两个靶点,可能会更有效地阻断这两个通路,增强抗肿瘤活性;与联合疗法相比,依沃西单抗安全性优势显著,与VEGF靶点相关的毒副作用大幅度降低。
6.伊努西单抗
伊努西单抗(AK102)是康方生物与东瑞制药合资公司康融东方开发的创新PCSK9单克隆抗体,用于治疗原发型高胆固醇血症和混合型高脂血症,包括HoFH、HeFH及同时患有动脉粥样硬化性心血管疾病的高胆固醇血症患者。
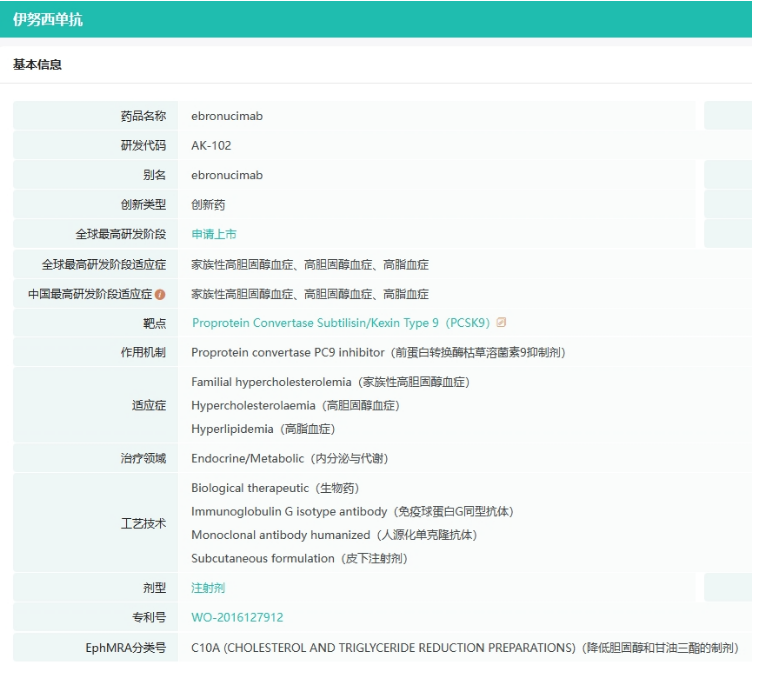
截图来源:药融云全球药物研发数据库
2023年6月,公司宣布伊努西单抗注射液的上市许可申请已经获CDE受理,用于两项适应症的治疗:原发性高胆固醇血症和混合型高脂血症,以及杂合子型家族性高胆固醇血症(HeFH)。
7.依沃西单抗
依沃西单抗(AK112)是康方生物研发的PD-1/VEGF双特异性抗体。基于其Tetrabody技术设计的人源化抗PD-1/VEGF双抗药物,可阻断PD-1与PD-L1和PD-L2的结合,并同时阻断 VEGF与VEGFR的结合。

截图来源:药融云全球药物研发数据库
其抗 PD-1端采用派安普利单抗的结构,抗VEGF 端则采用贝伐珠单抗结构。该公司于2022年年12月份将依沃西单抗的美国、加拿大、欧洲和日本权益出让给 Summit Therapeutics 公司,康方生物将获得5亿美元首付款,总交易额高达50亿美元和销售净额低双位数比例提成的合作方案,授予Summit Therapeutics于美国、加拿大、欧洲和日本对依沃西单抗的开发和商业化独家许可权。
8.戈利昔替尼
戈利昔替尼(golidocitinib)是由迪哲医药自主研发的新一代、强效且高选择性JAK1 抑制剂,是全球首个且唯一针对T细胞淋巴瘤的高选择性JAK1抑制剂,可有效抑制JAK/STAT信号通路,目前正在中国、美国、韩国和澳大利亚等国家开展关键性临床试验。
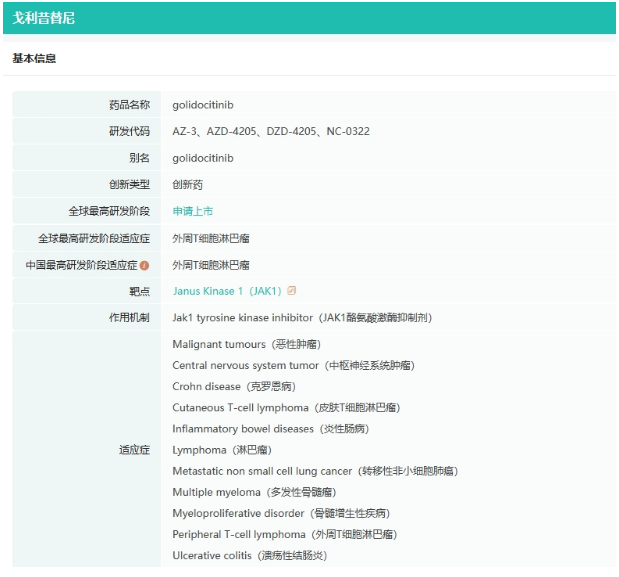
截图来源:药融云全球药物研发数据库
于今年9月获药品监督管理局(NMPA)受理并纳入优先审评。戈利昔替尼是全球首个且唯一针对PTCL的高选择性JAK1抑制剂,也是首个且唯一获FDA“快速通道认定”的PTCL国创新药。
9.HSK16149
HSK16149(Crisugabalin)是由海思科自主研发的新型电压门控钙离子通道α2δ亚基配体,可以α2-δ辅助蛋白结合发挥镇痛作用。

截图来源:药融云全球药物研发数据库
临床前研究表明 HSK16149 具有强效镇痛、长效镇痛、中枢副作用小等特点,有望替代普瑞巴林、加巴喷丁,具有成为慢性神经性疼痛首选用药的潜力。HSK16149 于 2018 年 11 月首次获批临床。2023年9月,HSK16149胶囊新适应症申报上市并获得受理,拟用于带状疱疹后神经痛。根据公开资料显示,HSK16149未来在临床应用中可能具有药效更显著、安全性更好等优势,具有成为慢性神经性疼痛首选用药的潜力。
10.杰克替尼
杰克替尼是由泽璟制药研发的一种广谱JAK抑制剂类小分子1类新药,对Janus激酶包括JAK1、JAK2、JAK3和TYK2具有显著的抑制作用。其在包括骨髓纤维化、重症斑秃等多个适应症表现出了广阔的前景。
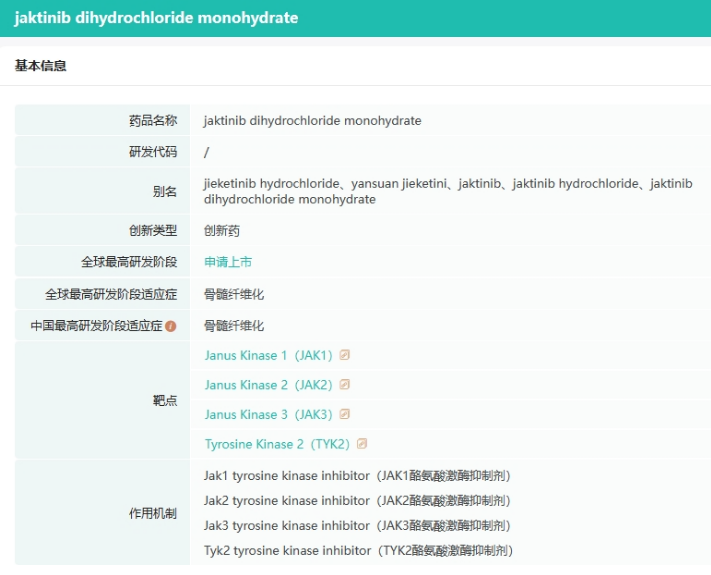
截图来源:药融云全球药物研发数据库
该公司在杰克替尼倾注了大量的资源,总投资规模达到11.6亿元(多纳非尼2.45亿元),开发的适应症包括:骨髓纤维化、重症斑秃、中重度特应性皮炎、强直性脊柱炎、特发性肺纤维化、中重度斑块状银屑病等,并且同时开发了片剂和乳膏剂两种剂型。其中,治疗中高危骨髓纤维化的新药上市申请已于2022年10月获国家药监局受理,成为第一个提交新药上市申请的国产JAK抑制剂类创新药物。
11.氘恩扎鲁胺
氘恩扎鲁胺(HC-1119)是海创药业研发用于治疗mCRPC的1类新药,是第二代雄激素受体(AR)拮抗剂恩扎卢胺的氘代药物,作为海创药业自主研发的 AR 抑制剂,拟用于治疗转移性去势抵抗性前列腺癌,是前列腺癌领域首个氘代机制的创新药物,优化了药物的PK/PD特性,药物安全性更佳。

截图来源:药融云全球药物研发数据库
该产品是该公司首个申请上市许可的新药,能够竞争性抑制雄激素与AR结合,阻断AR信号通路的传递,抑制前列腺癌细胞增殖,诱导前列腺癌细胞凋亡。2023年3月,德恩鲁胺的NDA已获NMPA受理,用于经醋酸阿比特龙或多西他赛治疗失败,不可耐受或不适合多西他赛治疗的转移性去势抵抗性前列腺癌(mCRPC)患者。
12.安奈克替尼
unecritinib(TQ-B3101)是由正大天晴研发的1类创新药,作为新型小分子受体酪氨酸激酶抑制剂,对ALK、ROS1和MET基因突变均有较强的抑制作用。

截图来源:药融云全球药物研发数据库
2022年,unecritinib的多中心、2期单臂临床研究首次亮相于欧洲肺癌大会(ELCC)大会,研究显示该药可突破现有ROS1靶向治疗药物易耐药、脑转移难治、眼毒性和肝毒性高发等局限性,为ROS1融合阳性晚期NSCLC患者治疗再添出路。安奈克替尼的上市申请于2022年6月递交中国国家药监局(NMPA)并获得受理,申报的适应症为ROS1阳性的非小细胞肺癌。
13.visepegenatide
visepegenatide(PB-119 )是派格生物自主研发的 1 类创新药物,为派格生物的首发管线,属胰高血糖素样肽-1 (GLP-1)受体激动剂,也是一款周制剂聚乙二醇化艾塞那肽。

截图来源:药融云全球药物研发数据库
属胰高血糖素样肽-1 (GLP-1)受体激动剂,也是一款周制剂聚乙二醇化艾塞那肽。经聚乙二醇定点修饰的PB-119充分保留了GLP-1受体激动剂的作用,包括改善胰岛β细胞功能,葡萄糖依赖性促进胰岛素分泌,低血糖风险低;诱导胰岛β细胞新生和增殖,并抑制细胞凋亡,从而增加胰岛β细胞数量。该类药物可作用于胰腺发挥葡萄糖浓度依赖性降低血糖作用,低血糖风险低;同时还作用于大脑、胃肠道、肝脏、心脏等多个重要器官和组织,有效控制食欲、延缓胃排空、减重、降压、调脂。
14.ongericimab
ongericimab(JS002)是君实生物自主研发的注射用重组人源化抗PCSK9单克隆抗体,用于治疗原发性高胆固醇血症和混合型血脂异常。君实生物是国内首家获得该靶点药物临床试验批件的中国企业。

截图来源:药融云全球药物研发数据库
2023年4月,国家药品监督管理局(NMPA)受理了昂戈瑞西单抗两项适应症的上市申请,用于治疗:1)原发性高胆固醇血症(包括杂合子型家族性和非家族性)和混合型血脂异常;2)用于成人或12岁以上青少年的纯合子型家族性高胆固醇血症。此外,本品在杂合子型家族性高胆固醇血症患者中的III期临床研究已完成入组。
15.巴托利单抗
巴托利单抗(HBM9161,batoclimab)是HanAll Biopharma开发的一种抗FcRn全人源单克隆抗体,同样是一款靶向FcRn的全人源单克隆抗体,可阻断FcRn-IgG相互结合,加速体内IgG的清除,从而达到有效治疗致病性IgG介导的自身免疫性疾病的效果。

截图来源:药融云全球药物研发数据库
早期研究表明,巴托利单抗具有良好耐受性,可迅速降低多种自身免疫疾病患者体内IgG水平。2017年9月,和铂与HanAll签署战略合作协议,获得了巴托利单抗在大中华地区,包括中国大陆、香港、澳门和台湾开发的授权。2022年10月,和铂医药与石药集团全资子公司恩必普药业达成协议,在大中华区共同开发巴托利单抗。
16.司普奇拜单抗
司普奇拜单抗(CM310)是康诺亚研发的一种抗 IL-4Rα 重组人源化单抗,通过与人白细胞介素 4 受体 α 亚基特异性结合,从而抑制炎症反应,用于中重度哮喘、COPD、特应性皮炎等适应症。作为国产IL-4Rα抗体药物,它是首个获得国家药监局批准进行临床试验的药物。

截图来源:药融云全球药物研发数据库
该药也是国内首个申报上市的IL-4R抗体药物,也是全球第二个。目前国内唯一获批上市的IL-4Rα单抗是赛诺菲/再生元联合开发的度普利尤单抗。
17.A166
A166(trastuzumab botidotin)是科伦博泰的核心产品,是科伦首个 ADC 项目,2017 年首次申请临床,首项临床试验在 2018 年度启动,2023年 5 月申报上市(受理号:CXSS2300034),是一款用于治疗晚期HER2阳性实体瘤的差异化NDA注册阶段HER2 ADC,由赖氨酸定点定量偶联、具有创新连接子和高活性毒素小分子组成。

截图来源:药融云全球药物研发数据库
A166是处于在上市申报阶段的差异化HER2 ADC,用于治疗晚期HER2+实体瘤,其定位为聚焦高患病率及大量医疗需求的多种癌症适应症,有望成为国内首款治疗HER2阳性(HER2+)BC的国产ADC。
18.泽沃基奥仑赛
泽沃基奥仑赛(CT053)是一种用于治疗复发/难治多发性骨髓瘤的全人抗自体BCMA CAR-T细胞疗法。2023年1月16日,华东医药宣布与科济药业就其BCMA CAR-T细胞产品泽沃基奥仑赛注射液(zevorcabtagene autoleucel,CT053),达成在中国大陆地区的商业化合作。

图片截图来源:药融云全球药物研发数据库
泽沃基奥仑赛是一款用于治疗复发/难治多发性骨髓瘤的自体CAR-T细胞产品,2022年10月已在中国申报上市。
总结
创新药物研发是漫长而复杂的历程,离不开持久投入与不懈努力。尽管中国在创新药物研发上取得显著进展,为未来发展带来诸多希望与机遇,但与发达国家仍有一定差距。不断提升中国创新药物研发成果与技术水平,将增强中国在国际医药领域的影响力与地位,加速实现由“药物制造大国”向“药物创新大国”的跨越。
<END>
要解锁更多企业药品研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药品各国上市情况、药品批文信息、销售情况与各维度分析、市场竞争格局、一致性评价情况、集采中标情况、药企申报审批信息、最新动态与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论