
近日,据CDE网站显示,复星医药子公司锦州奥鸿药业的 CDK4/6 抑制剂 FCN-437c 申报上市获受理。该品种是国内第 8 个申报上市的 CDK4/6 抑制剂,也是第 3 款报上市的国产药。FCN-437c是复星医药核心管线之一,探索用于一线和二线治疗HR+/HER2-乳腺癌。据药融云数据统计,目前抗肿瘤药(化药+生物药)在全国院内销售峰值超800亿。
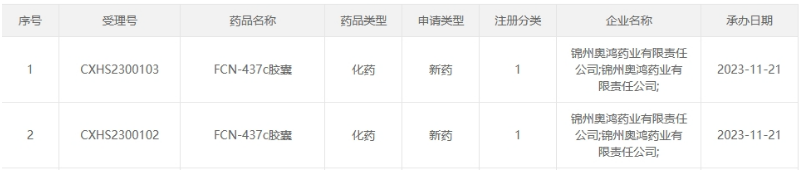
截图来源:CDE官网
FCN-437c胶囊 是 复星医药 研发的一款创新型口服小分子药物,具有强效、高选择性特点,它是一种全新结构的CDK4/6抑制剂。推测此次申报的适应症为激素受体阳性/人表皮生长因子受体2阴性 (HR+/HER2-) 晚期乳腺癌。
31款肿瘤药猛攻千亿市场!FCN-437c上市可期
在中国药物市场当中,抗肿瘤药物市场销售近些年来一直呈现稳步增长趋势。2019年,中国癌症新发病人数达到440.0万,约占全球癌症发病人数的四分之一。受人口老龄化、环境污染和不健康生活方式的普遍影响,预计到2024年中国癌症新发病人数将进一步增长到498.6万,预示着抗肿瘤药物需求的不断增长。
据药融云数据统计,抗肿瘤药物院内市场销售峰值超800亿元(在全国各省市二级及以上医院,≧100床位),所有医院抗肿瘤药物市场全年销售额将超千亿。
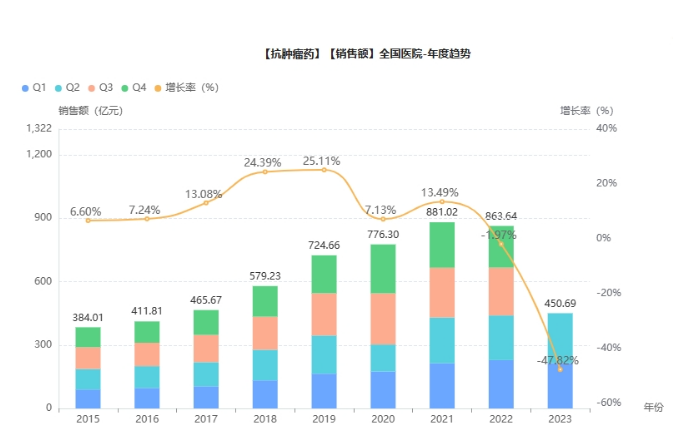
截图来源:药融云全国医院销售数据库
目前,复星医药有31款抗肿瘤药(化学或生物药)获批,其中复星医药旗下的上海复宏汉霖生物制药在2022年3月拿下了生物药1类新药斯鲁利单抗注射液,而FCN-437c胶囊是集团首款进入申报生产的抗肿瘤化学药1类新药,若顺利获批,将可能成为复星医药在抗肿瘤药物领域的又一突破。
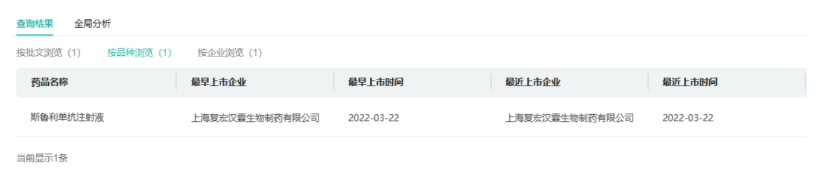
截图来源:药融云中国药品批文数据库
此外,全球范围内已批准上市的CDK4/6抑制剂有5款,包括哌柏西利(辉瑞)、达尔西利(恒瑞医药)、曲拉西利(先声药业/勃林格殷格翰)、瑞波西利(诺华)和阿贝西利(礼来)。其中,恒瑞的达尔西利当前也进入医保目录内,今年将谈判一线适应症。此外,嘉和生物的来罗西利以及轩竹生物的吡罗西尼也已申报上市,复星医药本次申报的 FCN-437c 也已获CDE受理,这一靶点即将面临更激烈的市场竞争。
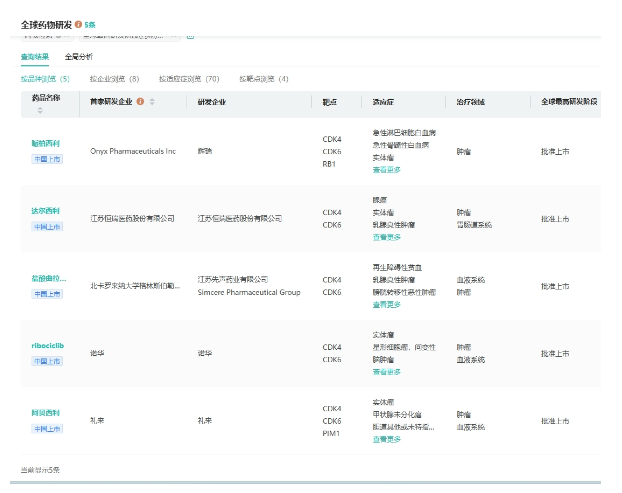
截图来源:药融云全球药物研发数据库
7款1类新药获批临床,涵盖肿瘤、心血管、眼科等领域
2023年至今,复星医药有7款1类新药获批临床。其中涵盖片剂、注射剂、胶囊剂等剂型。
复星医药7款1类新药获批临床数据表
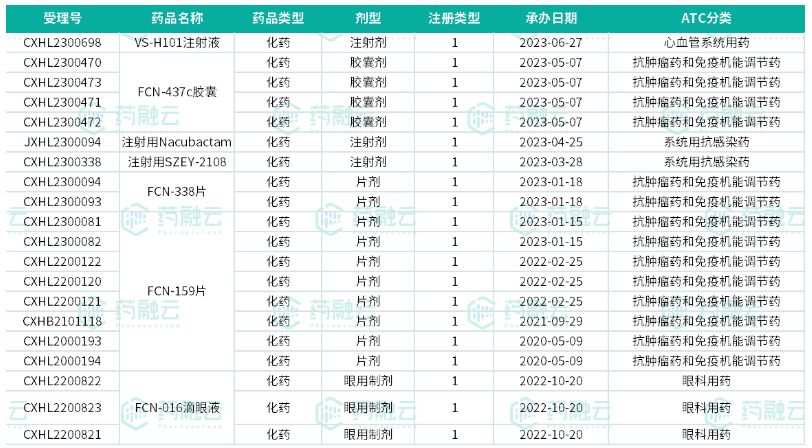
截图来源:药融云中国药品审评数据库
此外,复星医药在仿制药领域也非常发力,目前提交了70个品种(92品规)仿制申请,均在审评审评中。在抗肿瘤领域,已有4款药物过评,包含甲磺酸奥希替尼片、哌柏西利胶囊、甲磺酸伊马替尼片、甲苯磺酸索拉非尼片。
<END>
要解锁更多企业药品研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药品各国上市情况、药品批文信息、销售情况与各维度分析、市场竞争格局、一致性评价情况、集采中标情况、药企申报审批信息、最新动态与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!





























![医药高地:核药!恒瑞医药镥[177Lu]氧奥曲肽注射液获批临床](https://yaorongyun-public.oss-cn-shanghai.aliyuncs.com/images/covers/202302/09/e3938ad9f1d23e2fd043611c4a98c02a.png)










 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论