
近期,广东瑞顺生物技术有限公司(下称“瑞顺生物”,Wyze Biotech. Co., Ltd.)宣布其全资子公司—浙江瑞加美生物科技有限公司递交的“RJMty19注射液治疗复发/难治性自身免疫性疾病”IND申请得到国家药品监督管理局(NMPA)药品审评中心(CDE)正式受理(受理号:CXSL2300661)。

自身免疫性疾病 (Autoimmune Disease, AID),简称“自免“,是指机体对自身抗原发生免疫反应导致自身组织损害所引起的疾病。AID会累及皮肤、关节、肾脏、中枢神经系统等多个人体器官系统,对人体健康造成极大的伤害,严重影响患者的生活质量和寿命。AID总体发病率占全球人口的5-9%,其中美国约5%-8%,中国约2-3%。
近年来,B细胞清除治疗被广泛应用于自身免疫性疾病的治疗。已有国内外临床研究报道证明,以CD19为靶点的自体CAR-T细胞(嵌合抗原受体T细胞)能特异性与B细胞表面的CD19抗原结合,通过抗体依赖或补体依赖的细胞毒作用清除B细胞,继而有效降低体内炎症介质水平,特异性发挥免疫抑制的治疗效果,有效治疗系统性红斑狼疮(SLE)、系统性硬化症 (SSc)、特发性炎性肌病(IIM)等自身免疫性疾病。
针对自体来源CD19-CAR-T细胞治疗产品在制备周期长、价格昂贵、无法即时使用等方面的不足,瑞顺生物研发了现货通用型RJMty19注射液。该产品已在治疗r/r B-NHL的研究者发起的临床研究中获得了很好的安全性和初步有效性数据,在治疗AID中的临床效果值得期待。
此次RJMty19注射液AID适应症IND申请获得CDE受理,意味着RJMty19注射液作为全球首款现货通用型CD19-CAR-DNT免疫细胞治疗产品向正式注册临床试验又迈进了一步。
RJMty19注射液
RJMty19注射液(主要活性成分为CD19-CAR-DNT细胞)是由广东瑞顺生物技术有限公司基于人源化CD19-CAR全球专利开发的一款全球创新现货通用型DNT细胞治疗产品。与目前已上市6款CD19-CAR-T细胞治疗产品相比,CD19-CAR-DNT细胞具有可实现标准化制备、制备成本低、患者即时可用等诸多优点,未来市场竞争潜力巨大,可突破目前自体CAR-T细胞产品商业化推广的瓶颈。
RJMty19注射液审评详情
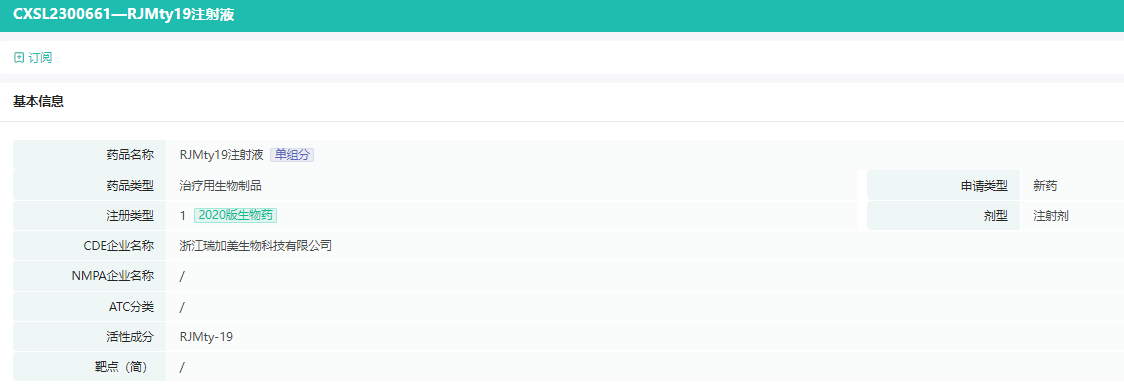
截图来源:药融云中国药品审评数据库
瑞顺生物
广东瑞顺生物技术有限公司以“关爱生命,造福人类”为愿景,以“做老百姓用得起的创新细胞药”为使命,专注于研发以DNT细胞为核心技术平台的现货通用型免疫细胞产品,是全球范围内DNT细胞免疫疗法的开创者,已开发了多款基于DNT细胞技术平台的现货通用型细胞治疗产品,包括RC1012注射液、RJMty19注射液等,目前正在开展针对血液肿瘤的两个注册IND临床试验和两个研究者发起的临床试验。
<END>
要解锁更多企业药品研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药品各国上市情况、药品批文信息、销售情况与各维度分析、市场竞争格局、一致性评价情况、集采中标情况、药企申报审批信息、最新动态与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!








































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论