该试验纳入了对现有疗法进展或无法耐受的多发性骨髓瘤(MM)患者,QLS32015的剂量范围设定为2-800微克/公斤(皮下注射,每周或每两周一次)。主要的研究终点包括剂量限制性毒性(DLT)、最大耐受剂量(MTD)、推荐2期临床剂量(RP2D)以及安全性评估。
截至2024年5月31日,已有11名患者入组该试验。这些患者的既往治疗中位线数为3(范围1-8),其中63.6%的患者至少接受过三类药物的治疗(包括蛋白酶体抑制剂、免疫调节剂和抗CD38抗体),54.5%的患者接受过一次自体干细胞移植(ASCT),18.2%的患者则接受过BCMA-CART治疗。

截图来源:摩熵医药全球药物研发数据库
QLS32015于2023年8月16日正式在国内启动了1期临床试验阶段。RRMM患者中展现出了可耐受的安全性和令人鼓舞的缓解率,这一结论为后续的剂量递增试验提供了有力支持。目前,DLT、MTD和RP2D仍有待进一步确定。
值得一提的是,GPRC5D作为多发性骨髓瘤细胞上高表达的细胞表面蛋白,已成为近年来新兴的治疗靶点。除了双抗外,针对该靶点的在研药物还包括CAR-T疗法、单抗和三抗等。
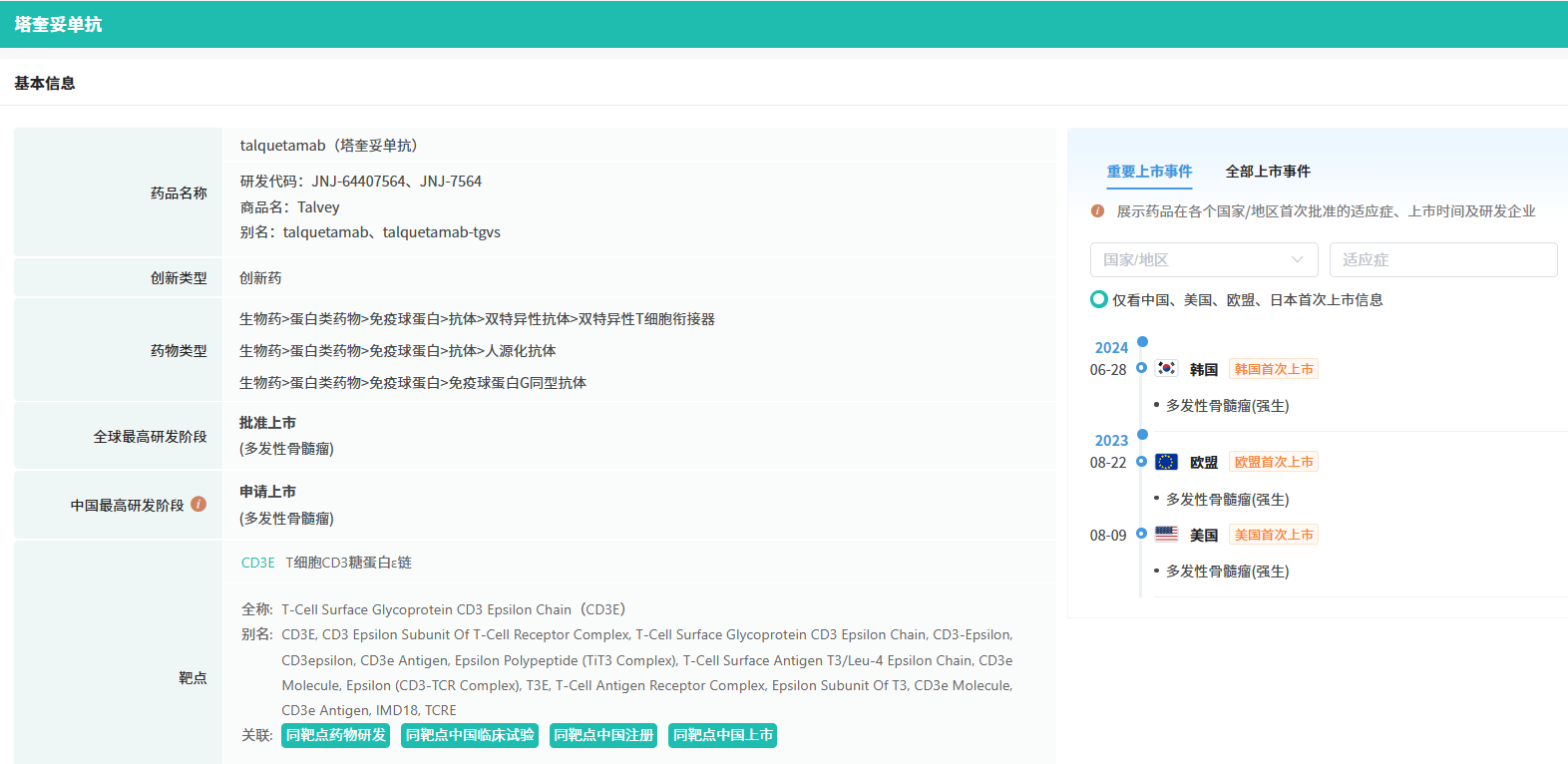
截图来源:摩熵医药全球药物研发数据库
目前全球在研的GPRC5D双抗超10款,其中仅有一款药物——强生的塔奎妥单抗已获批上市。其余在研项目中,罗氏的Forimtamig和维立志博的LBL-034已进展至I/II期临床,但值得注意的是,罗氏最新财报显示Forimtamig已从管线中移除。此外,正大天晴的TQB2029也已进入临床阶段,而康诺亚的CM380和CM559则分别在国内处于获批临床和申请临床阶段。其余在研的双抗均处于临床前阶段。
随着ASH年会的临近,QLS32015的初步研究结果无疑将为多发性骨髓瘤的治疗带来新的希望和期待。
想要解锁更多药物研发信息吗?查询摩熵医药(原药融云)数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!























































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论